
POTENZIAMENTO ASSE SCIENTIFICO TECNOLOGICO
A tutti i docenti di S. dell’infanzia, elementare e media
dell’I.C. via Cassia km 18,700
OGGETTO :l’ACQUA come costituente essenziale per la vita
Scheda N° 1 : PROPRIETA’ FISICHE E CHIMICHE
a cura della Funzione Strumentale Angela Nardi
La breve trattazione sull’acqua vuole essere uno strumento funzionale all’attività didattica per tutti
i docenti. I contenuti espongono in sintesi alcune tematiche che vanno dalla proprietà fisiche e
chimiche di questa sostanza ( contenuto della prima scheda) all’importanza che essa riveste per la
nostra esistenza e quindi all’esigenza di un suo utilizzo consapevole. ( seconda scheda)
Caratteristiche chimiche e fisiche
Si scrive H2O e si chiama monossido di idrogeno perché la molecola è formata da un atomo di
ossigeno e due di idrogeno ma tutti la chiamiamo acqua. E’ una sostanza davvero strana, perché
l’idrogeno è altamente infiammabile e l’ossigeno alimenta la fiamma, eppure… l’acqua spegne il
fuoco. Sul nostro pianeta il 97,2% dell’acqua si trova negli oceani e solo il 2,8 % sulla terraferma;
la maggior parte dell’acqua dolce è però imprigionata nelle calotte polari, nei ghiacciai e nel
sottosuolo : SOLO lo 0.025% del totale è direttamente utilizzabile da parte dell’uomo .
Se tutta l’acqua presente sul nostro pianeta fosse distribuita in modo uniforme attorno al pianeta
otterremmo involucri di diverso spessore : uno di 2750 m con le acque salate,uno di 250 m con
l’acqua dei ghiacciai e calotte polari, uno di 15 m con le acque del sottosuolo, un altro di 40 cm con
l’acqua superficiali di laghi e fiumi ed infine uno di 3 cm con l’acqua dell’atmosfera.
L’acqua è l’unica sostanza che si presenta in natura contemporaneamente nei tre strati di
aggregazione: solido, liquido e gassoso.
L’acqua è peraltro presente in modo abbondante negli essseri viventi, uomo compreso.
L'acqua, in condizioni di temperatura e pressione standard, è un liquido incolore e insapore, con
punto di fusione a 0 °C e punto di ebollizione a 100 °C.
A differenza della maggior parte delle altre sostanze, per le quali la forma solida è più densa di
quella liquida, il ghiaccio è meno denso dell'acqua liquida. La densità dell'acqua è infatti massima a
4 °C. Ciò è dovuto al fatto che il volume dell'acqua aumenta all'abbassarsi della temperatura, con
conseguente diminuzione della densità, e galleggiamento per spinta di Archimede.
Questa insolita espansione dell'acqua a basse temperature costituisce un vantaggio importante per
tutte le creature che vivono in ambienti di acqua dolce d'inverno. L'acqua, raffreddandosi in
superficie, aumenta di densità e scende verso il fondo innescando correnti convettive che
raffreddano uniformemente l'intero bacino. Quando la temperatura in superficie scende sotto i 4 °C
questo processo si arresta; e per la spinta di archimede, l'acqua più fredda rimane in superficie, dove
forma poi, con un ulteriore calo della temperatura, uno strato di ghiaccio. Se l'acqua non avesse
questa particolarità, i laghi ghiaccerebbero interamente, facendo morire tutte le forma di vita
presenti.
La situazione nelle acque marine è in qualche modo diversa. Il sale contenuto nell'acqua fa sì che
l'acqua congeli a circa −1,9 °C. Il ghiaccio che si forma è sostanzialmente privo di sale ed ha
densità paragonabile a quella del ghiaccio di acqua dolce. Questo ghiaccio galleggia sulla
superficie, mentre il sale che ne è stato "espulso" va ad aumentare salinità e densità dell'acqua
vicina, la quale scende per convezione verso il fondo.
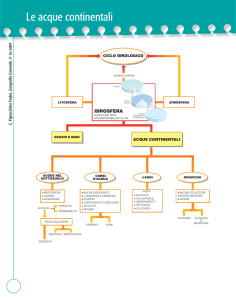
A seconda della loro provenienza, le acque naturali si classificano in:
acque meteoriche (pioggia, neve, grandine); acque sotterranee (falde profonde o freatiche);
acque superficiali (mari, fiumi, laghi, sorgenti).
Le acque meteoriche contengono gas normalmente presenti nell'atmosfera quelli localmente
presenti per via di attività industriali o di centri abitati e quelli che provengono dalla
decomposizione di sostanze organiche naturali . L'acqua meteorica può reagire con tali sostanze. Un
esempio è la pioggia acida.
A volte le acque sotterranee fuoriescono spontaneamente diventando acque sorgive (notevolmente
pregiate per l'uso potabile per la mancanza di organismi patogeni ma spesso la qualità viene
minacciata da erbicidi e pesticidi che sono estremamente dannosi ).
Le acque superficiali hanno composizione estremamente variabile a seconda delle condizioni
climatiche ed ambientali.
L'acqua è una molecola polare
Dato che l'ossigeno ha una elettronegatività maggiore, il vertice della molecola ospita una parziale
carica elettrica negativa, mentre le estremità recano una parziale carica elettrica positiva. Una
molecola che presenta questo squilibrio di cariche elettriche è detta essere un dipolo elettrico. Le
cariche fanno sì che le molecole vengano attratte reciprocamente l'una all'altra. Questa attrazione
nell'acqua è particolarmente intensa, prende il nome di legame idrogeno e spiega molte delle
proprietà fisiche tipiche dell'acqua.
Benché il legame idrogeno sia molto più debole dei legami covalenti interni alla molecola stessa,
questi è responsabile di molte delle proprietà fisiche dell'acqua. Due di esse sono i relativamente alti
punto di fusione e punto di ebollizione, è infatti richiesta una maggiore energia (rispetto a sostanze
meno polari) per rompere i legami idrogeno che tengono unite le molecole le une alle altre. Sempre
al legame idrogeno è da attribuire l'elevata capacità termica specifica.
Il legame idrogeno spiega anche l'insolito comportamento dell'acqua quando questa congela. A
causa sua, quando la temperatura si abbassa fino al punto di congelamento, le molecole di acqua si
organizzano nella struttura cristallina dalla simmetria esagonale tipica del ghiaccio che risulta essere
meno densa dell'acqua liquida. .
L'acqua come solvente
La sua polarità rende l'acqua anche un buon solvente. Quando un composto ionico o polare viene
messo in acqua, viene circondato dalle molecole di acqua le quali, per via delle loro piccole
dimensioni, si inseriscono tra uno ione e l'altro o tra una molecola e l'altra di soluto orientandosi in
modo da presentare ad ogni ione (o estremità polare) del soluto la parte di sé che reca la carica
opposta; questo indebolisce l'attrazione tra gli ioni (o tra le molecole polari) e rompe la struttura
cristallina. Ogni ione (o ogni molecola polare) si ritrova quindi circondato completamente da
molecole d'acqua. Un esempio di soluto ionico è il comune sale da cucina (cloruro di sodio), un
esempio di soluto molecolare polare è lo zucchero.
Le proprietà solventi dell'acqua sono essenziali per gli esseri viventi, dato che consentono lo
svolgersi delle complesse reazioni chimiche che costituiscono le basi della vita stessa (ad esempio,
quelle che avvengono nel sangue o nel citoplasma della cellula).
L'acqua possiede un'elevata tensione superficiale, osservabile tramite la formazione di gocce,
proprietà anch'essa importante per la vita. Un esempio è il trasporto dell'acqua negli xilemi degli
steli delle piante; la tensione superficiale mantiene la colonna d'acqua unita e forze adesive
mantengono l'acqua aderente allo xilema. Colonne altrettanto alte e sottili di liquidi meno coesi e
meno aderenti andrebbero a spezzarsi formando sacche d'aria o di vapore, rendendo inefficiente
fino all'impossibilità il trasporto del liquido attraverso lo xilema.
L'acqua pura è un buon isolante elettrico (cioè un cattivo conduttore). Ma, essendo anche un
buon solvente, spesso reca in sé tracce di sali disciolti in essa, che, con i loro ioni la rendono un
buon conduttore di elettricità. In tal caso, tramite un processo chiamato elettrolisi, l'acqua può
essere scomposta nei suoi componenti elementari, l'idrogeno e l'ossigeno sotto forma di ioni OH- e
H+, acquisendo così questa proprietà.
Queste sopra elencate sono le caratteristiche chimiche e fisiche fondamentali della sostanza acqua.
SITI CONSULTATI: www.greencrossitalia.it , www.wikipedia.org
POTENZIAMENTO ASSE SCIENTIFICO TECNOLOGICO
A tutti i docenti di S. dell’infanzia, elementare e media
dell’I.C. via Cassia km 18,700
OGGETTO :l’ACQUA come costituente essenziale per la vita
Scheda N°2 : Le problematiche legate all’acqua come risorsa esauribile
a cura della Funzione Strumentale Angela Nardi
La breve trattazione sull’acqua vuole essere uno strumento funzionale all’attività didattica per tutti
i docenti. I contenuti espongono in sintesi alcune tematiche che vanno dalla proprietà fisiche e
chimiche di questa sostanza ( contenuto della prima scheda) all’importanza che essa riveste per la
nostra esistenza e quindi all’esigenza di un suo utilizzo consapevole. ( seconda scheda)
L'acqua nell'universo
L'acqua è stata trovata nelle nubi interstellari della nostra galassia, la Via Lattea. Si presume che
l'acqua sia abbondante anche in altre galassie, dato che i suoi componenti elementari, idrogeno e
ossigeno, sono tra i più abbondanti elementi dell'universo.
L'acqua sulla Terra
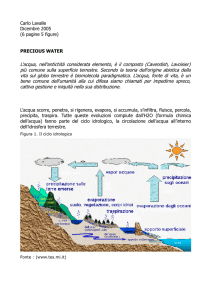
Il ciclo dell'acqua descrive il continuo scambio di acqua nell'idrosfera tra l'atmosfera, il suolo, le
acque di superficie, le acque profonde e gli esseri viventi. L'acqua compie un ciclo continuo: grazie
all'evaporazione delle acque superficiali per effetto dell'irraggiamento solare ed alla traspirazione
delle piante, si formano le nubi negli strati più freddi dell'atmosfera. Queste vengono trasportate dai
venti ed al variare di temperatura e/o pressione, ritornano al suolo ( anche se non in modo uniforme
in tutte le parti del pianeta) sotto forma di acque meteoriche arricchendo di nuovo le acque
superficiali ed in parte (filtrando nel terreno) quelle sotterranee. Poiché moltissime sostanze hanno
una qualche solubilità in acqua, in natura praticamente non esistono acque pure.
I ghiacciai dell'Artide sono la principale riserva di acqua dolce nel nostro pianeta. La loro fusione a
causa dell'effetto serra e dell'aumento delle temperature ha un forte impatto ambientale, per
l'innalzamento del livello dei mari, ma anche per la scomparsa di tale riserva. Durante la fusione dei
ghiacci, l'acqua dolce si mescola a quella salata del mare, divenendo inutilizzabile dall'uomo.
L'acqua nell'industria
L'acqua è usata anche in numerosi processi ed apparecchiature industriali , nonché nei processi
dell'industria chimica. Infatti, grazie alle sue proprietà chimiche, l'acqua costituisce l'ambiente di
reazione e dissoluzione di molte sostanze,e, per le sue caratteristiche termiche, è un ottimo fluido
trasportatore di calore.
Una forma di inquinamento è rappresentata dallo scarico nell'ambiente di acque residue di processi
industriali non opportunamente trattate (i. chimico) o di acque di raffreddamento (inq. termico) .
La politica dell'acqua
A differenza di altri beni di primaria importanza, come il petrolio, il rame o il grano, l'acqua non è
sostituibile nella maggior parte dei suoi impieghi e non è economicamente conveniente il suo
trasporto a distanze superiori a qualche centinaio di chilometri.
A causa della crescita della popolazione mondiale e altri fattori, la disponibilità di acqua potabile
per persona sta diminuendo. Il problema delle riserve acquifere può essere risolto con un deciso
aumento della produzione, una migliore distribuzione e un minore spreco. Per questo motivo,
l'acqua è una risorsa strategica per molti paesi. Tanti stati sono stati coinvolti in una lunga
successione di conflitti, armati e politici, per l'usufrutto d'acqua, per l'accesso alla stessa e tensioni
governano alcuni rapporti diplomatici proprio per il controllo sulle riserve.
L'acqua pulita è quotata come il petrolio del futuro, facendo del Canada, con la sua naturale
abbondanza d'acqua, la potenza più grande del mondo. L'acqua dolce, sta pian piano acquisendo
l'attenzione della gente per una gestione più intelligente e un uso sostenibile.
Tuttavia, l'acqua salata non è adatta a nessuna delle suddette applicazioni. Il sale elimina la fertilità
dei terreni, incrosta le turbine e le pale di una centrale, e in generale tutti i componenti meccanici .
L'acqua del mare è presente in una quantità pressoché infinita sulla Terra, e potrebbe risolvere
definitivamente il problema della siccità nel mondo, se si riuscisse a ricavarne acqua dolce.
L'acqua dolce rappresenta solo il 2,5% del volume totale presente sulla Terra, e più dei 2/3
dell'acqua dolce si trovano in pochi ghiacciai, in particolare nell'Artide. Un ulteriore 30% si trova in
riserve sotterranee e solo meno dell'1% dell'acqua dolce si trova in laghi, fiumi o bacini ed è quindi
facilmente accessibile
Il World Water Development Report dell'UNESCO nel 2003 indica chiaramente che nei prossimi
vent'anni la quantità d'acqua disponibile per ogni persona diminuirà del 30%. Il 40% della
popolazione mondiale non può permettersi il lusso dell'acqua dolce per una minima igiene.
I governi di molti Paesi hanno programmato di distribuire l'acqua ai bisognosi gratuitamente. Altri s
il meccanismo del mercato libero.
L'80% dell'acqua dolce è destinata all'agricoltura per l'irrigazione e all'industria, mentre solo una
minima parte serve le utenze civili. Gli impianti di irrigazione a microgoccia sono una tecnologia
che consente di abbattere di alcuni ordini di grandezza i consumi idrici in agricoltura .
L'utilizzo di questi impianti può essere completato con canalizzazioni per la microirrigazione
interrate, che portano l'acqua direttamente alle radici delle piante, evitando le perdite per
evaporazione e la dispersione nel terreno. Oltre all'acqua, arrivano micronutirienti e fosfati,
abbattendo i rischi d’inquinamento dei terreni e i costi di concimazione.
Anche nel caso dell'industria, vi sono margini di efficienza attraverso la depurazione degli scarichi e
il riutilizzo delle acque reflue negli stessi impianti industriali o per l'irrigazione, contenendo le
emissioni inquinanti nelle falde acquifere, dalle quali si attinge l'acqua potabile.
Alcune ulteriori fonti di risparmio idrico sono rappresentate dalla raccolta di acqua piovana in
apposite cisterne, in particolare per l'irrigazione, dall'utilizzo di acqua di condensa ottenuta tramite
deumidificatori o di altri sistemi in grado ad esempio di ricavare acqua dolce dalla condensa della
nebbia.
Il mercato dell' acqua minerale
Il mercato è molto remunerativo, se si considera che un litro di acqua in bottiglia costa circa quanto
1000 litri di acqua del rubinetto .
All'acqua minerale sono talora attribuite particolari proprietà nutritive o terapeutiche che l'acqua del
rubinetto non dovrebbe possedere, tali da giustificare il costo molto maggiore dell'acqua in bottiglia.
In realtà, l'acqua è incolore, inodore e insapore, anche se in natura non è acqua pura e contiene dei
sali minerali o altre sostanze importanti per l'organismo, ma che andrebbero ingerite tramite il cibo
piuttosto che con le bevande.
La legge italiana impone per l'acqua potabile controlli a frequenza quotidiana garantendo una
migliore qualità all'acqua del rubinetto. La principale voce di costo nel prezzo dell'acqua è quello
del trasporto. Le acque meno costose sono quindi quelle imbottigliate a livello locale.
L'acqua nelle culture umane
Per la maggior parte delle religioni, l'acqua è considerata un elemento purificatore. Esempi sono il
battesimo cristiano ed i bagni rituali dell'ebraismo e dell'islam. Anche nello scintoismo l'acqua è
usata nei rituali di purificazione di persone o luoghi.
All'acqua vengono spesso attribuiti poteri spirituali; molte religioni venerano dei legati all'acqua o i
corsi d'acqua stessi (esempio, il Gange per l'induismo). Ancora, divinità particolari sono posti a
patroni di particolari fonti d'acqua.
SITI CONSULTATI: www.greencrossitalia.it , www.wikipedia.org







![Lord Byron, 1812-1818, poeta […] Rimbombo di acque! Dalla](http://s1.studylibit.com/store/data/004489654_1-4bb17c51794561741fad69d9434b633b-300x300.png)

