LE IDEE DELLA TERMODINAMICA
M. Vicentini
1. Introduzione
E’ indubbio che il concetto fondamentale della Termodinamica (nel seguito TD),
l’entropia, con la sua introduzione nella fisica tra l’ottocento e il novecento, segni una
rivoluzione scientifica che stabilì l’assetto della TD classica.
Ciò tuttavia non significa che con tale assetto si sia giunti al termine dello sviluppo
della ricerca nel campo: restavano problemi da risolvere, fenomeni già noti da spiegare e
fenomeni nuovi da ricercare. Troppo spesso, nella didattica e nella divulgazione, sembra
emergere il messaggio che, con i postulati di Kelvin e Clausius e l’interpretazione statistica
di Boltzmann, la TD macroscopica abbia terminato il suo ruolo nella ricerca per lasciare il
campo alla TD statistica.
Al fine di correggere il tiro voglio qui indicare gli sviluppi delle idee della TD nel
corso del 900. Premetto che non sono né una storica né una epistemologa delle scienze. Le
mie parziali competenze sia di storia che di epistemologia si sono formate in stretto
collegamento con il mio attuale campo di ricerca, la didattica della fisica, e con particolare
attenzione alla TD in quanto nella mia precedente attività di ricerca mi ero vista
impegnata in studi che richiedevano la conoscenza della TD moderna.
Chiedo pertanto venia di eventuali approssimazioni e interpretazioni personali in
ambito storico-epistemologico. Voglio però anche notare la carenza di studi storici sullo
sviluppo della TD dal periodo classico alla fine dello scorso secolo.
Il quadro di sviluppo delle idee della TD che tenterò di presentare sarà illustrato
con riferimento alla mappa di sviluppo della conoscenza scientifica in generale riportata in
fig.1, sottolineando in particolare lo stato dell’universo di conoscenza condivisa in un dato
periodo storico e i problemi di ricerca teorica o sperimentale che trovano la loro
collocazione e ragion d’essere in tale universo.
Pur se altre conferenze dedicheranno maggior attenzione e approfondimento allo
sviluppo del periodo classico ritengo utile partire anche io dagli inizi.
La presentazione sarà quindi focalizzata su cinque fasi: l’universo preTD classica
(par.2), la definizione della TD classica (par.3), Assiomatizzazioni e generalizzazioni
(par.4), TD dei processi stazionari (par.5), TD estesa (par.6).
Concluderanno
la
presentazione
alcuni
suggerimenti
per
una
didattica/divulgazione attuale.
1
L’universo
della
conoscenza
condivisa
(teoria, modelli, dati,
tecnologia)
guida lo sviluppo di
Idee
che possono mettere a fuoco
Problemi
da risolvere con
Ricerca
teorica
Ricerca
sperimentale
da confrontare con
che possono
stimolare
che produce
Risultati
sperimentali
che può stimolare
nuova
Tecnologia
portano a
Una nuova definizione dell’universo di conoscenza condivisa
Fig. 1
2
2. L’universo di conoscenze preTD classica
A livello teorico si ha da un lato, ovviamente, la meccanica newtoniana (più o meno
nella forma in cui oggi viene insegnata) applicata ai modelli di punto materiale e sistema
rigido con i concetti di forze conservative e dissipative (necessarie per il raggiungimento
dell’equilibrio), la dinamica dei fluidi e naturalmente i concetti di energia( cinetica e
potenziale) e lavoro.
Per quanto riguarda l’assetto teorico dei fenomeni puramente termici si ha la teoria
del calorico con la differenziazione tra i concetti di calore e temperatura, la definizione
operativa di calore Q = mcT e quindi la definizione dei calori specifici e dei calori
latenti necessari alla spiegazione dei passaggi di stato già noti sperimentalmente1.
Anche l’elettromagnetismo classico forniva idee teoriche già sistematizzate per
spiegare i fenomeni elettrici e magnetici.
A livello fenomenologico sono inoltre note alcune equazioni di stato (in particolare
quelle utili per il funzionamento dei termometri) e alcune equazioni di trasporto. Per
queste ultime è importante ricordare quelle relative alla conduzione termica (Fourier), alla
diffusione (Fick) e alla conduzione elettrica (Ohm).
E’ importante ricordare che la conoscenza dei coefficienti di conduzione termica dei
diversi materiali insieme a quella sui processi di convezione e irraggiamento permette la
costruzione di apparati con alta capacità di isolamento termico (materiali adiabatici) o di
trasmissione rapida del calore (materiali diatermici).
Sono empiricamente noti inoltre, anche se scarsamente formalizzati, gli effetti di
riscaldamento dovuti all’attrito localizzato e connessi con i fenomeni elettrici (effetto
Joule) e chimici (reazioni endo/esotermiche).
A livello tecnologico, oltre ai termometri, si ha lo sviluppo delle macchine termiche
che, con i problemi di rendimento, contribuiscono, anche per spinta sociale, a stimolare lo
sviluppo teorico. E’ ben vero tuttavia che molti problemi rimangono ostici alla
investigazione empirica per la mancanza di adeguati sussidi tecnologici (vedi pompe da
alto vuoto, tecniche per abbassare la temperatura e per purificare i materiali).
Non vanno inoltre dimenticate le conoscenze in ambito medico, biologico e chimico
e, naturalmente, l’utilità di un modello atomico.
Quali sono dunque i problemi che la comunità scientifica tenta di affrontare, vuoi
con ricerche teoriche vuoi con investigazioni empiriche?
Ovviamente un primo problema è quello di capire il funzionamento delle macchine
termiche per migliorarne, se possibile, il rendimento. Ciò implica lo studio di un
collegamento tra i concetti di calore (dalla teoria del calorico) e di lavoro (dalla meccanica).
E’ d’altra parte necessario focalizzare l’attenzione sulle proprietà di equilibrio dei
sistemi termodinamici per la cui descrizione si conoscono empiricamente molte variabili
ma nessuna di esse è in grado di fornire una spiegazione ragionevole del raggiungimento
e stabilità degli stati di equilibrio.
Da un punto di vista più filosofico possiamo anche formulare una domanda
aggiuntiva: sino a che punto i fenomeni termici sono spiegabili mediante le leggi della
meccanica? (Bellone).
E’ utile notare che tali definizioni, nate in un contesto in cui il calore veniva considerato come posseduto dai
corpi, sopravvivono linguisticamente anche oggi nonostante il calore non sia più considerato una funzione di
stato mentre i calori aggettivati lo rimangono.
1
3
3. La definizione della Termodinamica classica
Per risolvere i problemi è necessario da un lato mettere da parte alcune conoscenze
che vengono riconosciute come accessorie ai problemi stessi e dall’altro scegliere, tra i tanti
possibili sistemi termodinamici, il sistema più semplice dotato di proprietà facilmente
misurabili.
L’accessorio sono i processi nel loro reale svolgimento (ma la cui conoscenza è
fondamentale per la costruzione di strumenti e apparati) e il sistema semplice adatto allo
studio è un fluido omogeneo, più precisamente un gas privo di altre proprietà che non
l’espansività. Si studieranno quindi le macchine termiche con cicli basati sulle proprietà
dei fluidi.
L’universo di conoscenze raggiunto al termine del processo di ricerca è ben
riassunto nelle due formule che vanno sotto il nome di 1° e 2° principio della TD:
U = Q – L
(1)
dQ
R T
2
S
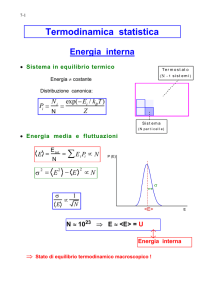
Le due relazioni infatti introducono le due variabili fondamentali del discorso:
l’energia interna che unifica i concetti di calore e lavoro come “forme di energia” e
l’entropia che giustifica, con l’essere prodotta durante ogni processo reale, l’esistenza degli
stati di equilibrio.
La focalizzazione sugli stati di equilibrio permette la trattazione dei processi
attraverso le trasformazioni quasistatiche e la valutazione dei cambiamenti nelle variabili
di stato come differenze fra stato iniziale e finale.
Siamo in un mondo ideale senza tempo (Truesdell) con macchine termiche che
funzionano non funzionando e in cui la concessione ai processi reali è manifesta solo nel
segno di disuguaglianza nella formulazione analitica del 2° principio.
Una proprietà dell’entropia viene poi specificata dal 3° principio mentre il modello
atomico gioca il suo ruolo per interpretare le grandezze termodinamiche in termini
meccanici.
L’universo di conoscenze così definito è ben riassunto nel manuale di Maxwell
(vedi fig.2).
4
I fenomeni
termici o
del calore
1.
2.
3.
4.
sono
Invenzione
di
termometri
connessi
con
definizione e
misura
temperatura
aspetti
dinamici
permettono
di definire
senzazioni
variazioni di proprietà (dilatazione)
cambiamenti di stato (colori latenti)
trasmissione di calore (cond., conv., irrag.)
invenzione
di
calorimetri
Conducibilià
termica
Fourier
luce
modello
particellare
definizione
e misura
del calore
che
soddisfa
energia di
un corpo
Principio di
conservazione
generalizzato
permettono la
descrizione
degli stati con
isoterme, T=cost
diagrammi
indicatori
studiati per
situazioni
adiabatiche, senza Q
che
applicati
alla
macchina
immaginaria
di Carnot
permettono di
-
dare la scala assoluta di T
legare Q a L e definire U
definire S (superfici di Gibbs)
enunciare il II principio
Fig. 2 – Schema del manuale di Maxwell
5
Assiomatizzazioni e generalizzazioni
Nella prima assiomatizzazione (Caratheodory) sembra evidente l’intenzione di
relegare il concetto di calore al ruolo di concetto spurio: si ha quindi una riformulazione
dei principi dando il ruolo guida alle trasformazioni adiabatiche e al concetto di lavoro.
Più interessante per gli sviluppi della TD è l’assiomatizzazione proposta da Tisza e
Callen (Tisza
, Callen
).
In primo luogo viene qui riconosciuto che la TD classica è in realtà una
Termostatica in quanto si limita allo studio degli stati di equilibrio.
In secondo luogo, mentre le relazioni 33.1 e 3.2 vengono riconosciute come le
relazioni necessarie al collegamento tra le proprietà interne al sistema (U, S) e le azioni
esterne (Q, L), ci si pone il problema di esprimere formalmente le relazioni tra le variabili
interne al sistema, qualsiasi esso sia.
Vengono così formulati dei nuovi postulati che coinvolgono solo le variabili
estensive caratterizzanti il sistema (vedi riquadro 1).
6
Postulato I – Per ogni sistema termodinamico semplice esistono degli stati, detti stati di
equilibrio che, dal punto di vista macroscopico sono completamente caratterizzati dai
valori dell’energia interna U, del volume V e dei numeri di moli N1…Nn dei componenti
chimici.
Un secondo postulato invoca come criterio per il raggiungimento dell’equilibrio un
principio di estremo per una ulteriore variabile estensiva, che è introdotta nella
formulazione stessa del postulato.
Postulato II – Per ogni sistema composto in uno stato di equilibrio esiste una funzione delle
variabili estensive, chiamata entropia e indicata dal simbolo S. Questa funzione ha la
proprietà che i valori assunti dalle variabili estensive nella assenza di un vincolo interno
sono quelli, tra la possibile varietà degli stati di equilibrio vincolati, per i quali l’entropia è
massima.
Introdotta formalmente la variabile entropia, due ulteriori postulati ne precisano la
dipendenza dalle variabili estensive del sistema.
Postulato III – L’entropia di un sistema composto è additiva rispetto ai sistemi componenti.
L’entropia è una funzione continua, differenziabile e monotonicamente crescente rispetto
all’energia.
Postulato IV – L’entropia di qualsiasi sistema si annulla nello stato per il quale:
U
S
V,N
0
Riquadro 1 – I postulati della Termostatica
7
Si giunge così ad affermare che la conoscenza completa di un sistema
termodinamico omogeneo e privo di proprietà elettriche magnetiche e chimiche si ha nella
equazione fondamentale della Termostatica:
o
U = U (S V N)
S = S (U V N)
in linguaggio energetico
in linguaggio entropico
Dalle 3.1 e 3.2 si ricavano le relazioni di Gibbs e di Gibbs Duhem per le variabili
interne al sistema:
dU = TdS – pdV + dN
O = SdT – Vdp + Nd
che permettono l’introduzione delle variabili intensive T, p, in funzione delle variabili
estensive
T
U
S VN
p
U
V SN
U
N SV
e la definizione del numero di equazioni di stato (relazioni che legano variabili intensive a
variabili estensive) equivalenti alla equazione fondamentale.
Non è questo il luogo per scendere nei dettagli formali della teoria di cui è utile
sottolineare la potenzialità di generalizzazione da un lato verso un generico sistema
termodinamico e dall’altro verso lo studio dei processi.
La generalizzazione a tutti i sistemi termodinamici è facilmente ottenuta con
l’aggiunta di nuove variabili estensive, siano Xj , e il riconoscimento che il contributo
energetico di tali variabili è sempre esprimibile dal prodotto Y jdXj dove Yj è la variabile
Yj
U
X j
SUN
intensiva coniugata a Xj
8
Mentre l’assetto teorico viene così riformulato la ricerca prosegue in ambito
sperimentale anche avvantaggiandosi degli sviluppi tecnologici.
Si sviluppa la fisica delle basse temperature con la scoperta della superfluidità e
superconduttività. Si eseguono misure precise delle transizioni di fase con punti critici
(fluidi e magneti). Si propongono nuove formulazioni analitiche delle equazioni di stato
(van der Waals e Langevin Weiss).
La meccanica statistica acquista un ruolo di campo di ricerca autonomo sia pure con
strette relazioni con la TD macroscopica.
E… frigoriferi e automobili diventano oggetti di consumo. Ma forse non si è capito
fino in fondo il problema della crisi energetica (Kelvin e la pompa di calore).
4. Termodinamica dei processi stazionari vicini all’equilibrio
Il problema ora è: come inserire i processi reali nel quadro della TD e come valutare
la produzione di entropia nel loro svolgimento.
Vengono quindi recuperate le conoscenze sulla descrizione dei processi di
conduzione del calore, di diffusione e del trasporto elettrico.
A queste si aggiungono le conoscenze sui processi incrociati, in particolare gli effetti
termoelettrici mentre appaiono dati sperimentali sul cosiddetto “ordine fuori
dall’equilibrio” (le celle di Benard, le clock reactions).
Il punto di partenza sono nuovamente le relazioni di Gibbs ora espresse
esplicitando la variazione temporale e con l’uso del linguaggio entropico
dS 1 dU i dXi
Yi
dt T dt
T
dt
che per un sistema omogeneo privo di proprietà elettriche, magnetiche e chimiche si
riduce a
dS I dU pdV
dN
dt T dt
dt
dt
Si continua quindi a pensare ad una equazione fondamentale in cui le variabili
indipendenti sono le sole variabili estensive.
La variazione totale di entropia in un processo viene ora espressa eliminando la
disuguaglianza attraverso la definizione di un contributo di flusso e uno di produzione.
Il flusso di entropia Js è legato al flusso di calore
Js
dJ
d dQ
Q
dt T
T
Si tratta quindi di trovare una espressione per la produzione di entropia in termini
di flussi (tutti) e delle forze generalizzate che descrivono i processi.
9
Ji
dX i
dt
F i = Yi
Il formalismo matematico da adottare è quello della fisica del continuo e si assume
l’ipotesi dell’equilibrio locale: in una particella di fluido le variabili termodinamiche hanno
i valori dell’equilibrio.
Si ottiene quindi per la produzione di entropia
N
s J i Fi
I
i
Naturalmente è necessario per valutarla effettivamente conoscere la dipendenza dei
flussi dalle forze generalizzate.
In prima approssimazione e per flussi stazionari si assume una dipendenza lineare
(in accordo con le equazioni di trasporto note in casi specifici) ma lasciando la possibilità
che il flusso di una qualsiasi variabile estensiva possa dipendere da tutte le forze
generalizzate presenti nel sistema
Ji = Lik Fk
con Lik = Lki
(relazioni di Onsager)
E’ facile capire che tale relazione è in grado di spiegare gli effetti incrociati e di
calcolare in un qualsiasi processo la produzione di entropia.
Un piccolo semplice esempio: se un conduttore elettrico è tenuto a una differenza di
potenziale V, in assenza di passaggio di corrente si può generare una differenza di
temperatura T.
E’ interessante notare che, sempre nel caso elettrico del passaggio di corrente
attraverso una resistenza R la produzione di entropia è:
S = iV
ovvero l’effetto Joule.
Ma… vi sono problemi per i casi di flusso non stazionario e per la velocità di
trasmissione dei segnali.
Nel frattempo l’universo di conoscenze condiviso è cambiato. Forse il cambiamento
più importante è quello dovuto al suo spezzettamento in tanti universi legati ai diversi
campi di ricerca.
L’attenzione ai problemi della TD si può considerare ristretta a quelli che lavorano
nel campo o in domini strettamente affini. Tra questi possiamo ricordare la fisica delle
basse temperature che intreccia nella superfluidità e nella superconduttività concetti
termodinamici quantistici e statistici.
Può essere utile ricordare che la stabilità della fase liquida di He3 e He4 allo zero
assoluto è spiegabile in termini termodinamici. Ancora è da ricordare la ricerca sulle
transizioni di fase con punto critico in cui la prima derivazione delle leggi di scala è
formulata in termini puramente termodinamici.
10
5. La termodinamica estesa
Nello scorso secolo due linee di ricerca, dette rispettivamente TD estesa e TD
razionale, hanno proseguito lo studio dei processi per estendere la trattazione dal caso
stazionario al caso di flussi variabili nel tempo e per risolvere il problema della
trasmissione dei segnali. Un punto comune alle due trattazioni è l’abbandono dell’ipotesi
dell’equilibrio locale con l’introduzione di variabili TD di non equilibrio. In particolare
ora, oltre alle variabili estensive si assumono come variabili indipendenti nella espressione
della equazione fondamentale anche i flussi
S = S (U, Xi, Ji)
Ovviamente il linguaggio matematico è quello della fisica del continuo il che ne
comporta un notevole appesantimento.
Non mi soffermerò pertanto sugli sviluppi della ricerca. Mi basti ricordare che, con
flussi dipendenti dal tempo, è necessario modificare le relazioni fenomenologiche tra flussi
e forze generalizzate nel senso di
a
dJi
bJ i Lik Fk
dt
Per ulteriori chiarimenti sul tipo di studi cito da un articolo di rassegna sulla TD
estesa del 1988 che esplicita anche la collocazione della TD estesa come ponte tra
l’approccio statistico e l’approccio macroscopico.
“Possiamo ricercare un approccio intermedio, o mesoscopico in cui il sistema è
descritto da ulteriori variabili oltre a quelle macroscopiche classiche. Per essere utile il
numero totale di variabili non deve essere troppo alto. La prima domanda da porsi
riguarda la necessità e il significato di tali descrizioni mesoscopiche. Le variabili
macroscopiche classiche non sono arbitrarie ma sono direttamente connesse con quantità
conservate. Altre variabili, non conservate, decadono molto rapidamente. Pertanto, in
tempi molto brevi, si rimane solo con le variabili conservate. Se però si è interessati a
fenomeni rapidi (tipo perturbazioni ad alta frequenza) il tempo di decadimento di alcune
variabili può essere confrontabile con la durata della perturbazione. Può anche accadere
che, in circostanze particolari, si abbia un allungamento del tempo di decadimento (punti
critici).
In questi casi le nuove variabili “lente” devono essere introdotte nell’insieme delle
variabili macroscopiche ….
Se siamo interessati a fenomeni di non-equilibrio, transienti o stazionari, i flussi
dissipativi giocano un ruolo importante. Essi normalmente non vengono considerati
variabili indipendenti, poiché hanno tempi di rilassamento molto brevi, ma vengono
trattati come grandezze dipendenti determinate dai gradienti delle grandezze
termodinamiche.
Quando tuttavia l’interesse è sulle perturbazioni ad alta frequenza o quando il
tempo di decadimento diventa lungo (fluidi polimerici, superconduttori, superfluidi,
sistemi vicino al punto critico) dobbiamo considerare i flussi come variabili indipendenti.”
11
6. E allora: quali idee della TD trasmettere nella didattica e nella divulgazione?
Le due mappe delle figure 3 e 4 esemplificano cosa ritengo che un insegnante di
Scuola Secondaria dovrebbe conoscere per impostare un discorso da trasmettere agli
studenti. La prima mappa è molto semplice e focalizza alcuni concetti fondamentali
(equilibrio, sistema termodinamico, variabili interne al sistema, azioni esterne) ma non
trascura i processi.
La seconda mappa utilizza il linguaggio matematico e pone in evidenza come la
trattazione usuale, trascurando i processi e limitando la trattazione al gas più o meno
perfetto non riesca a comunicare che una parte dell’universo termodinamico.
Alcuni commenti: ho spesso notato come il segno di disuguaglianza nel secondo
principio crei più problemi di quanti ne risolva.
L’espressione della variazione di entropia come somma di un termine di flusso
legato al calore (e quindi presente solo nei processi guidati da una differenza di
temperatura) e un termine di produzione legato agli attriti interni al sistema è di più facile
lettura anche perché legata all’intuizione (se una grandezza all’interno di un sistema varia,
ciò può essere dovuto a un flusso entrante o uscente e alla produzione (o perdita interna).
Forse lo stabilire un legame forte fra entropia e calore (Hermann) è la via maestra
per una comprensione del concetto di entropia e potrebbe evitare alcune imprecisioni
linguistiche molto diffuse. Ad esempio si sente spesso dire e si legge “il calore prodotto
per attrito”. L’attrito produce entropia e tale produzione si manifesta con un aumento di
temperatura.
Pur non sottovalutando l’utilità di un modello cinetico-statistico per interpretare i
concetti TD mi sembra utile rilevare che tale interpretazione è più importante per dare
validità al modello stesso che non per capire temperatura e entropia.
Ciò che si deve tentare di comunicare è che la termodinamica è un gioco tra energia
e entropia (Wanderlingh), un gioco complesso in cui le variabili non sono correlate due a
due ma si intrecciano tra loro. Ma … quanti giochi di questo mondo si svolgono in modo
analogo?
12
La TD ha
come
problema
centrale
quello di
descrivere e
spiegare
l’equilibrio
e i processi
verso
l’equilibrio
di un
sistema
TD
oggetto
macroscopico
ovvero di un
oggetto
dotato di
un interno
le cui
caratteristiche
interne
ovvero di un
possono
variare per
azioni
esterne
effetto di
Fig. 3
13
Per risolvere il problema è necessario
descrivere i
processi
che sono
Definire le variabili che caratterizzano
l’interno
Y intensive
(pT……)
y0
ycost
coniugate a paia
(T-S, N, pV…)
descritti da
'
''
Y a X b X
Forze
generalizzate
Fi
in particolare
JS
definire le
azioni
esterne
X estensive
(VMUS…)
I dQ
T dt
all’equilibrio
sono costanti
flussiJ i
dXi
dt
tutte
conservate
tranne S
che può
essere
prodotta
correlate da
equazioni
di stato
all’equilibrio
valgono
le
relazioni:
dU=TdS+YidXi
0=SdT+XidYi
ovvero Xi
Esistono materiali
che permettono di
isolare
azioni/processi
Valgono le
relazioni
U Q L
S
nei processi vicino
all’equilibrio
Sp= F1 Ji
Fornire/sottrarre
energia
(Q/L)
massa
……..
Q
Sp
T
Sp si valuta dalla
somma algebrica dei
JS in un percorso
quasistatico
Fig. 4
14