Corso di formazione:
Prevenzione della tubercolosi nelle aziende
sanitarie
Storia naturale e modalità di
trasmissione
M.Bugiani
P.Caramello
A.Macor
•Prevalence of infectious cases
•Duration of illness
•Intensity, frequency and duration of contact
Largely
endogenous
Largely exogenous
Innate resistance
Performance of cellmediated immunity
•Particles/volume x exposure time
•Production of infectious droplets
•Clearance of air
•Extent of exposure
Re-infection
Form and site of TB
Age
Patient’s susceptibility
Delay in diagnosis
Strain virulence
RF
RF
RF
RF
Exposure
Subclinical
Infection
Modello epidemiologico
TB
Infectious
Tuberculosis
Death
Non-infectious
Tuberculosis
TR
isolamen
to
TP
Tr
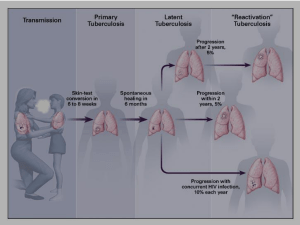
Patogenesi
Dall’esposizione alla malattia
Esposizione a
caso contagioso
Fondamentale è il
rapporto tra attività
battericida dei mφ e
virulenza dei bacilli
Fondamentale è
l’immunità
cellulo-mediata
Non infezione:
i macrofagi alveolari
(mφ) uccidono MTB
Infezione: MTB prolifera nello
spazio extracellulare e vengono
reclutate cellule infiammatorie
(nel 95% dei casi le
cellule T controllano
l’infezione, che
rimane subclinica)
* Rischio molto
maggiore negli
immunodepressi Infezione latente: MTB
controllato dal sistema
immunitario per tutto il
resto della vita
Riattivazione
(5% di rischio
durante il resto
della vita) *
(il 5% va incontro a
malattia attiva entro
1-2 *
anni)
TB attiva e sintomatica:
I soggetti possono trasmettere
la malattia ad altri
Storia naturale della TB
ESPOSIZIONE
Fattori di rischio di
esposizione
Incidenza di malattia contagiosa
nella comunità
Durata della contagiosità
(Prevalenza)
Numero di contatti suscettibili per
unità di tempo di contagiosità
Tempo di esposizione
Spazio (volume d’aria)
Modalità del contagio per via aerea
Il contagio avviene per condivisione
dell’aria col malato contagioso
Che emette agenti patogeni nelle
goccioline con
il respiro
la tosse (100 volte)
Dipende da
infettività del caso
tipologia del contatto
caratteristiche dell’ambiente
Fattori dell’ospite
Fattori influenzanti la
probabilità del contagio
Modalità del contatto
Spazio
Tempo
Caratteristiche individuali
Fattori dell’ospite
Carica biologica
Manovre generanti aerosol
Ambiente
Ricambi d’aria
Illuminazione naturale
Tipologia dell’aerosol
Cumulative Percentage of Droplets Expelled During
Aerosol Producing Maneuvres, by Droplet Size
Cumulative percentage
100
80
Coughing
60
40
Singing
20
Talking
0
1
3
5 7 10
100
1000
Droplet diameter (micrometers)
Loudon RG, et al. Am Rev Respir Dis 1968;98:297-300
Effetto della carica biologica
Fraction of cases / infected
Sensitivity of Direct Sputum Smear Examination
in Identifying Pulmonary Tuberculosis and Transmitters
1.0
0.8
Fraction due to
smear-neg cases
Smear-neg
Culture-pos
0.6
0.4
Fraction due to
smear-pos cases
Smear-pos
Culture-pos
0.2
0.0
Cases of
pulmonary
tuberculosis
Infected
contacts
< 15 yr
Calculated from data from:
Grzybowski S, et al. Bull Int Union Tuberc Lung Dis 1975;50:90-106
Ambiente
Volume
Ricambi d’aria
Luce solare
Effetto della luce solare
Killing of BCG by Sunlight and in Open Sky Without
Direct Exposure to Direct Rays of the Sun
7
10
Number of colonies
(log scale)
6
10
5
10
4
10
3
10
Skyshine
2
10
Sunlight
1
10
05 15 30
60
240
Exposure time (minutes)
Edwards LB, et al. Bull World Hlth Organ 1952;5:333-6
Effetto della durata del contatto
Prevalence of Tuberculous Infection Among Inflight
Personal in Contact with a Tuberculous Staff Member
Per cent tuberculin positive
100
80
60
40
20
0
0
10
20
30
40
50
60
Total flight time with index case (hours)
Driver CR, et al. JAMA 1994;272:1031-5
Effetto del trattamento sulla carica bacillare
1.2
1
*10^7
0.8
Sens
RES 2°
RES 1°
0.6
0.4
0.2
0
0
5
10
15
20
Giorni di trattamento
15
Incidence, Point Prevalence, and Period Prevalence
Time 1
Time 2
In year 3:
Incidence:
Point prevalence, March 15:
Period prevalence Time 3:
Time 3
Time 4
12 cases
24 cases
288 person-months
Incidence, Point Prevalence, and Period Prevalence
Time 1
Time 2
In Time 3:
Incidence:
Point prevalence, March 15:
Period prevalence Time 3:
Time 3
Time 4
12 cases
6 cases
72 person-months
Probabilità di infezione da Agenti
Biologici a Trasmissione Aerea
P =1-e
- Iqpt/Q
P = Probabilità di trasmissione
I = numero di soggetti infettivi
q = quantità di agenti patogeni emessi dal
paziente
t = tempo di esposizione al contagio
p=
ventilazione polmonare
Q = numero di ricambi d’aria
18
Probabilità di infezione da Agenti
Biologici a Trasmissione Aerea
P(di trasmissione) =>
n.infetti
carica bacillare
Tempo
Volume d’aria
19
Esposizione efficace
Particles
Volume
Particles:
Volume:
Exposure time:
x
Exposure time
Production of infectious droplet
nuclei+
Volume of air and ventilation
Time of inhaling air with droplet
nuclei
Nuclei inalabili (1µ
µm-5µ
µm) contenenti MT
Rischi di esposizione
L’incidenza dipende dal numero di
casi che accedono la struttura
(FATTORE MODIFICABILE NELLA
CCOMUNITA’)
LA PREVALENZA DEL N DI CASI E
DAL TEMPO CHE RESTANO NON
ISOLATI E TRATTATI
Fattore modificabile nella struttura
Cause del ritardo diagnostico
di TB (da Rieder 1993)
Rx
No Rx
Inizio
sintomi
Accesso al
medico
0
10
Inizio
terapia
diagnosi
20
30
40
50
Giorni dall'inizio dei sintomi
Paziente
Diagnosi
Terapia
60
70
Cause del ritardo diagnostico
e di trattamento
Ritardo nel trattamento per numero
di casi di TB ricoverati
Low
Intermediate
High
AMERICAN JOURNAL OF RESPIRATORY AND CRITICAL CARE MEDICINE VOL 165 2002
Controllo dell’esposizione
RIDUZIONE DEL NUMERO E DELLA
DURATA DEI CONTATTI EFFICACI
Diagnosi, trattamento e isolamento
dei casi contagiosi
Ricambi d’aria
DPI
Misura dell’esposizione
Generalmente non misurabile
Sorveglianza
Studi ambientali ad hoc
Misure dei ritardi diagnostici
INFEZIONE
Patogenesi
La prima infezione
L’infezione tubercolare è il risultato dell’inalazione di
MTB se la carica batterica è elevata o le difese
immunitarie sono inadeguate
Ingresso di MTB
negli alveoli
Fagocitosi
macrofagica
Diffusione per via linfatica
(ed eventualm. ematica)
Risposta linfocitaria
(IFN-γ e altre CK)
Moltiplicazione di
MTB nei macrofagi
Infezione di
altri macrofagi
Risposta attivante i mφ
Risposta danneggiante i tessuti
(ipersensibilità ritardata)
INFEZIONE TUBERCOLARE
LATENTE (ITBL)
Condizione nella quale il Mycobacterium
Tuberculosis (MT) si è insediato
nell’organismo senza sintomi clinici,
anomalie radiografiche e con reperti
batteriologici negativi
Problemi di nomenclatura
I definizione 1909 : TB latente
Mycobacterium tuberculosis
ALVEOLO
In sede alveolare i bacilli
vengono fagocitati dai
macrofagi
Possono essere distrutti
immediatamente oppure
riescono a moltiplicarsi, in
funzione di un bilancio di
fattori che è essenzialmente
scomponibile in:
Potere battericida costitutivo o indotto dei macrofagi
alveolari
Grado di virulenza dello stipite di Mycobacterium
tuberculosis
L’infezione può quindi essere arrestata già in questo stadio, sia per la
precedente sensibilizzazione dell’individuo , sia e soprattutto per le
capacità battericide costitutive dei macrofagi alveolari
I macrofagi non attivati,
con bacilli attivi in sede
intracellulare, migrano
nel linfonodo di
drenaggio
1
2
I macrofagi
secernono dei
fattori solubili con
proprietà
chemiotattiche nei
confronti dei
monociti circolanti,
che vengono quindi
reclutati in sede
linfonodale
In condizioni di permissività i bacilli
continuano a moltiplicarsi a spese dei
monocito-macrofagi attratti nel linfonodo
3
4
Raggiunta una quantità critica, da un
punto di vista antigenico, intervengono i
linfociti T attratti dalle cellule che
presentano l’antigene/i e la risposta
acquista specificità
MHC I & II
M
T
Ag. M.tuberculosis
Effetto della tipologia del caso e del
contatto
Tuberculous Infection Among Close Contacts (Children <15 yr)
by Bacteriologic Status of Index Case
70
s+/c+
60
Per cent infected
s-/c+
50
40
s-/cs+/c+
30
s+/c+
20
s-/c10
s-/c+
s-/c+
s-/c-
0
Bedfordshire
1948 - 1952
Rotterdam
1967 - 1969
Saskatchewan
1966 - 1971
Shaw JB, et al. Am Rev Respir Dis 1954;69:724-32
van Geuns HA, et al. Bull Int Union Tuberc 1975;50:107-21
Grzybowski S, et al. Bull Int Union Tuberc 1975;50:90-106
Diagnosi di ITBL
Nella malattia il MT è isolato solo
nel 50% dei casi
Nella Infezione Latente nessun
isolamento possibile
Test diagnostici ?: test tubercolinico
(TST)
Specificità verso (MOTT, BCG)
Sensibilità verso TB malattia
Non Gold Standard nella TBL
Basi biologiche dei test diagnostici di ITBL.
In vitro
Il test tubercolinico
Test epicutanei (HT)
Tst multipuntura
Iniezione intradermica (MANTOUX)
di un derivato proteico (+ o – purificato) di
MT
Vecchia tubercolina
PPD : purified protein derivative
Antigeni comuni a MT complex
M. Humanus, Africanus, Bovis, BCG
…… e ad alcuni MNT
Preferire metodi con misure in mm
Limiti del TST (Mantoux Test)
Somministrazione e LETTURA
Personale addestrato
Ritorno del testato
Non ritorni >30%. Chaisson et al 1996, Serwint et al 1997, Malotte et al
1999, Tanke et al 1994
Soggettività e variabilità
Interpretazione stratificta per livello di rischio (5,10, 15 mm).
NTM e BCG.Huebner et al 1993, Lalvani et al 2001, Delgado et al 2002
Cross reactività con BCG (
>10% falsi + per BCG; 10% NTM +, di cui 30% con TST +. Margileth 1994,
Huebner et al 1993, Von Reyn et al 2001
Variazione PPD tra produttori e batch
Villarino et al 2000, Chaparas et al 1985
Riproducibilità scarsa
Kendig et al 1998
Boosting–
Test ripetuti danno falsi positivi (Conversioni)(BCG)
Poco sensibile in TB attiva
20 to 40% of active TB patients are TST negative.Pathan et al 2000, Fietta et al 1985,
ATS/CDC Diagnostic guidelines
Anergia & HIV
> 50% di coinfettati TB/HIV sono TST -
Moderne misure diagnostiche
per TB: IFN- γ in vitro
Purified lymphocyte techniques
PBMC culture
Flow cytometry
Elispot
Whole blood culture
QuantiFERON
Diluted whole blood
Specie specificità di ESAT-6 e CFP10
TB Complex
ESAT
M tuberculosis
M africanum
M bovis
BCG substrain
gothenburg
moreau
tice
tokyo
danish
glaxo
montreal
pasteur
Environmental
strains
Antigens
CFP
+
+
+
+
+
+
-
-
M abcessus
M avium
M branderi
M celatum
M chelonae
M fortuitum
M gordonii
M intracellulare
M kansasii
M malmoense
M marinum
M oenavense
M scrofulaceum
M smegmatis
M szulgai
M terrae
M vaccae
M xenopi
Antigens
ESAT
CFP
+
+
+
-
+
+
+
-
Raccomandazione per la diagnosi di
ITBL
TST (Mantoux) : raccomandato
Serie storica consolidata
PPD 5UI o RT23 2 UI
NO TEST MULTIPUNTURA O HT
Test IFN-γ: consigliato
Previste risorse economiche durature
Laboratorio affidabile disponibile
Larga esperienza con TST
Molti vaccinati
SCARSI VANTAGGI IN FU (booster, BCG, …….)
Applicare test su sangue per conferma +
Ritestare tutti i positivi in prima applicazione
Laboratori di riferimento (per Q-TB)
40
Controllo
Terapia dell’infezione tubercolare
latente
Follow-up degli infettati non
trattabili
Efficacia dell’Tx ITBL H
(metanalisi)
(protezione massima, minima, media)
100%
100%
75%
50%
25%
0%
0%
t
To
ità
un
om
C
i
tt
i
os
br
Fi
ta
on
C
ni
io
rs
ve
on
C
Cohn L Treatment of latent Tuberculosis infection
In Reichman TUBERCULOSIS Chp 18 2000 M.Dekker
Indicazione alla Tx ITBL
Gruppo
TST+
mm (>=)
IPT Se > 35 aa
Viraggi
+10
Sì
5
Sì
Immigrati, Home-less, Carcerati
10
NO
TD, Alcolisti
10
NO
10
NO
5
10
Sì
Sì
5
Sì
Contatti Stretti
Op.sanità/comunità (>=
HIV+
Diabete, silicosi
Fibrosi
Medio Rischio*)
* Su indicazione del MC
Soggetti non ad alto rischio (>= 15 mm, età < 35 aa)
Non più raccomandata
Regimi raccomandati
(CDC/ATS
2003)
Regime
Effetti collaterali HIV+ HIV-
Raccomandazioni
9H
9H2
+
+-
A(II)
B(II)
A(II)
B(II) DOTP
6H**
6H2
4R
2RZ
2RZ 2
+++
+++
++
C(I)
C(I)
B(III)
D(III)
D(III)
B(I) No alto rischio
B(II) DOTP
B(II) Se resistenza H
D(II)
D(III)
** Raccomandato per HIV – da LG nazionali/AIPO
A=PREFERITO
B=ACCETTABILE
( I ) =TRIALS RANDOMIZZATI
C= se A e B NON PERCORRIBILI
( II) =T non RAND.
D= non raccomandato
(III) = OPINIONE DI ESPERTI
Preventive Therapy Use at a ProTEST Site
South Africa, 2000 - 2002
Aderenza
Number of persons
200
Past
TB
150
To 6 mo INH
TB
sympt
100
50
Eligible
Analyzed
Adherent
nonadherent
1 dose
only
Eligible
Started
Non-adherent
0
HIV +
Rowe KA, et al. Int J Tuberc Lung Dis 2005;9:263-9
Monitoraggio: Prima di
iniziare
Escludere TB attiva
Anamnesi, esame clinico, Rx …
Raccogliere informazioni su precedenti
TB attiva trattata
Trattamenti per TB o TBIL
Valutare controindicazioni al
trattamento
Ottenere informazioni su altre patologie
o terapia in corso
Consigliare test HIV se comportamenti
o situazioni a rischio
Sorveglianza
Screening su popolazioni ad alto
rischio di infezione
Contatti di casi di TB contagiosa
Operatori di strutture sanitarie o
assimibilabili
Comunità residenziali
Carceri
Case-finding in soggetti a rischio
Raccomandazioni
Ricerca attiva dell’ITBL solo in
Gruppi e soggetti ad alto rischio
(prevalenza) di
Malattia dopo l’infezione
Infezione
…… candidabili alla Terapia
Interpretare i test alla luce delle
conoscenze epidemiologiche
Cut-points = 5, 10, 15 mm, nazionali
Ove disponibile confermare i TST+ con
TiFG
MALATTIA
Da infezione tubercolare a
malattia
L’immunità acquisita tiene sotto
controllo i focolai di infezione nel
90% circa dei casi.
Solo il 10% dei soggetti con test
tubercolinico positivo si ammala
nell’arco della vita
Sviluppo di malattia
Su 100 soggetti esposti a FONTE DI CONTAGIO (MALATO BACILLIFERO)
40 - 90%
INFETTATO (MANTOUX POSITIVA)
PROTEZIONE DELL’INDIVIDUO
PROTEZIONE DELLA SOCIETA’
3-10%
MALATTIA
Più della metà entro i primi 2 anni dal viraggio
Gli altri nel resto della loro vita
TB polmonare: forma primaria e postprimaria
TB polmonare primaria
Opacità polmonare nei lobi
medi e inferiori
ingrandimento ilare
omolaterale e strie linfangitiche
Sintomi clinici spesso assenti o
aspecifici come febbre o
malessere generale
• Adenopatia ilare isolata con atelectasie con tosse
secca: frequente nei bambini
• Possibilità di escavazione acuta con formazione
di caverne negli adolescenti e giovani adulti
• Possibilità di malattia disseminata negli anziani e
immunodepressi
•
Rare manifestazioni
concomitanti:
•Eritema nodoso
•Cheratocongiuntivite
flittenulare
• TB polmonare post primaria
• Focolaio infiammatorio
localizzato nei lobi superiori
può andare incontro a
remissione o escavazione
(caverne).
• Sintomi clinici presenti con
maggior
intensità
• Comune
nei pazienti HIV+,
che hannoeun rischio
del 10%frequenza,
ogni anno di sviluppare
malattia, e in
ma lanon
pazienti anziani o con altre condizioni morbose
raramente
sottovalutati
associate ad immunosoppressione
• Lobite
• Broncopolmonite a focolai disseminati
• Pleurite e versamento pleurico
• Può essere associata a tubercolosi miliare (diffusa o
circoscritta, acuta o cronica) per disseminazione
ematogena di un focolaio riattivato
TB extrapolmonare: localizzazioni più frequenti
Rischio di tubercolosi dopo
l’infezione
Dipende
Dall’età
Dall’intervallo di tempo dall’infezione
Dalla superficie positiva del test
tubercolinico
Dai fattori di rischio immunologici :
HIV
Terapia immunosoppressiva (anti-TNF)
Cancro e terapia oncologica
Fumo
Rischio di tubercolosi dopo l’infezione
Horsburgh CR, NEJM 2004;350:2060-7
Fattori di rischio della riattivazione
Rischio di TB negli infettati
HIV
10 % nella vita
2-5% nei primi 2 anni
HIV + o immunodepressi
1% ogni anno
30% nei primi 2 anni
TB polmonare: i sintomi
Spesso asintomatica nelle fasi iniziali
Sintomi sistemici
• Febbre (spesso di basso grado, serotina e intermittente, ma
può essere
elevata)
• Sudorazione notturna
• Perdita di peso e anoressia
• Malessere generale e astenia
Sintomi da localizzazione polmonare
• Tosse da almeno 3 settimane (inizialmente non
produttiva,poi con
essudato purulento)
• Emottisi (rara, se bronchiectasie o rottura di aneurismi)
• Dolore toracico (se ci sono lesioni subpleuriche)
• Dispnea (in caso di malattia estesa: rara e di bassa specificità)
TB polmonare: gli esami
Esame obiettivo
• Segni aspecifici e di limitata utilità (spesso negativo, a volte
rantoli, sibili o ronchi).
Esami di laboratorio
•?
Esami radiografici
• RX del torace: positivo per quadri compatibili con TB
Esami microbiologici
• Esame diretto dell’escreato: positivo per bacilli alcol-acido
resistenti
• Esame colturale dell’escreato: positivo per ceppi di M.
tuberculosis +
antibiogramma
Esami immunologici
• Test di Mantoux: positivo se indurimento cutaneo >cut off
specifico
• Test dell’interferone gamma: positivo
Controllo
Trattamenti standardizzati
2RHZE+4RH
Accurata definizione dei percorsi
terapeutici
Misure per migliorare l’aderenza
Sorveglianza
Obbligatorie
Segnalazione dei casi contagiosi
sospetti
Segnalazione di tutti i casi di TB
Regionali
Sorveglianza degli esiti del
trattamento (della TB polmonare)
Segnalazione dai laboratori ed
anatomie patologiche
“….di tutte le malattie la tisi era la più virulenta la
più difficile da trattare, e causava la maggior parte
di decessi…….”
Ippocrate
Robert Koch
“…. Tuberculosis is Ebola with wings…….”
Richard Burmanger, WHO, 1993
Prevention tools (future)
Index case
Vaccination:
New vaccines (2)
Early Diagnosis:
Disease: new tools
LTBI: γINF (1)
Adequate Treatment:
New drugs
TLTBI:
New (safe
and shorter)
regimens (3)
contact
Infection
Environmental Control:
Policy to apply available
tools
Grazie per l’attenzione




![modulo di consenso informato []](http://s1.studylibit.com/store/data/002425407_1-6cd2d73436cdc58f9ad99d2df8bf9f08-300x300.png)