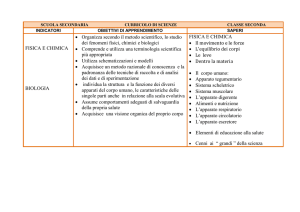
Justus Liebig's combustion apparatus
Justus von Liebig (1803–1873)
Liebig fu un chimico che si interessò a molti campi di applicazione della chimica come in
agricoltura . Qui voglio ricordare il ruolo di educatore che ebbe . Creò un modello di
laboratorio a Giessen , poi a Monaco in Germania che divenne una grande scuola dove
poterono esercitarsi studenti e chimici , poi divenuti famosi . Ideò strumenti e tecniche nuovi
che contribuirono a dare allo sviluppo della chimica un grande impulso. Progettò uno
strumento per l'analisi per combustione delle sostanze organiche che divenne
indispensabile per lo sviluppo della chimica organica . Sotto è una foto dello strumento .
Modello dell’ apparato di Liebig . Museo della Scienza di Monaco di Baviera .
Che il metodo fosse , nell'attività sperimentale , una novità importante , perchè sostituiva
metodi lenti e complessi , lo testimonia l’autorevole Wöhler che scriveva a Berzelius nel
1828: “ho eseguito di recente un piccolo esperimento , adatto al tempo limitato che avevo a
disposizione , che ho velocemente completato e il quale , grazie a Dio, non richiedeva che
una singola analisi per combustione .”
Come funzionava l'apparecchio di Liebig
Justus Liebig progetta nel 1831 l' apparato per eseguire analisi di routine . Il suo schema
mostra che il riscaldamento era ottenuto disponendo del carbone nella vaschetta di metallo
attorno al tubo di combustione chiuso di vetro a , a sinistra . Il tubo a contiene la sostanza da
bruciare e l’ossido di rame CuO che è l’agente ossidante . L’ossido di rame , con il
riscaldamento, si decompone in rame metallico e ossigeno . Un prodotto della combustione ,
l’acqua , viene assorbita nel tubo b, riempito di cloruro di calcio CaCl2 , questo sale è un buon
disidratante . Mentre l’altro prodotto , la CO2 , è assorbita da una soluzione concentrata di KOH
contenuta in d , una serie di cinque bulbi in vetro .
Quando la combustione è completa e il tubo a comincia poi a raffreddarsi , la soluzione inizia a
risalire nel bulbo a . Il raffreddamento e la rarefazione dei gas presenti provoca una diminuzione
della pressione all’interno dell’apparato e una conseguente spinta della pressione esterna che fa
risalire appunto la soluzione nel bulbo a . A questo punto viene rotta la punta del tubo a ,
indicata con B ( dove era alloggiato il campione ) , facendo cosi’ entrare aria . Si aspira poi con la
bocca dalla estremità destra dello strumento . L’aria , attraversando l’apparato , fa si che
l’acqua e la CO2 residui siano assorbiti nei rispettivi mezzi assorbenti . Da notare che
l’aspirazione era fatta con la bocca . Questo comportava dei rischi e occasionalmente i chimici
pagavano il prezzo. Oggi , nei nostri laboratori , con le norme di sicurezza adottate , questo
modo di operare non sarebbe ne lecito , ne possibile . Il tubo c in coda allo strumento a destra
contiene KOH , ed era incluso nell’apparato quando la sostanza da analizzare conteneva anche
l’elemento azoto oltre al carbonio e idrogeno . Poiché si poteva creare con la combustione una
forte corrente di gas azoto, ( N2) una parte della miscela contenuta nei 5- bulbi poteva uscire . Il
tubo serviva da trappola . Alla fine dell’esperimento venivano pesati i due pezzi a e b
dell’apparato e determinato l’aumento di peso . Questo apparecchio , cosi’ semplificato , era
economico , poteva essere fatto funzionare da un solo studente e richiedeva soltanto 0,5 g di
campione . L’opportunità di imparare a usare questo apparecchio, frequentando il laboratorio fu
senza dubbio la ragione principale che fece del Laboratorio di Liebig a Gessen un grande centro
della chimica in Europa , alla fine del XIX secolo . Ma la possibilità di ridurre il campione usato
era legata non solo alla bassa incertezza sperimentale raggiunta , ma anche alla nuova bilancia
analitica che Liebig contribuì a fare costruire . La bilancia poteva pesare 100g con una
accuratezza di 0,3 mg . Se veniva bruciato un campione di 0,5 g veniva prodotta circa 1g di CO2
, che poteva essere pesata con una accuratezza dello 0,1 % . Le lunghe braccia della bilancia
oscillavano così lentamente che Liebig aveva il tempo di fumarsi un sigaro durante il tempo che
occorreva per eseguire una pesata .
L'apparecchio a cinque bolle di Liebig rimase in uso per oltre tre quarti di secolo , cominciò a
essere sostituito agli inizi del ventesimo secolo quando iniziarono a diffondersi i metodi di
microanalisi . Questo apparato fu una innovazione importante tanto che è diventato un logo
molto diffuso , per esempio è inserito nello stemma della Associazione Chimica Americana .
Stemma della Associazione Chimica Americana
Note per la didattica
Gli studenti dovrebbero confrontare l'apparecchio di Liebig con quello di Lavoisier , rilevando
le differenze e le analogie . Intanto per la combustione non si usa più l'ossigeno dell'aria ma
l'ossidante diventa l'ossido di rame. Quale è il vantaggio ? Permette di riscaldare il tubo di
reazione , che è chiuso , a lungo , in modo che la combustione sia più completa . L'ossido di
rame è un ossidante che esercita anche una azione catalitica . La quantità di sostanza da
sottoporre alla combustione può essere molto ridotta . L'apparato a cinque bolle, introdotto per
la cattura della CO2 , è un sistema che lavora a cascata e nello stesso tempo la superficie di
assorbimento è complessivamente molto aumentata , permettendo un assorbimento completo
della CO2 prodotta . La esecuzione della analisi diviene veloce , rispetto ai tempi precedenti che
abbiamo visto preoccupavano tanto Wohler.