BVD-MD – diarrea virale bovina – malattia della mucose
E’ una malattia abbastanza subdola, con cui si può convivere in allevamento senza accorgersene ,a a lungo
andare procura perdidite in fatto di mancate fecondazioni, aborti, decrementi ponderali e cali della
produzione lattea.
È una malattia infettiva ad eziologia virale.
Colpisce i ruminanti domestici ed anche i selvatici, ma mentre nei domestici si ha la chiarezza della
responsabilità dell’agente eziologico, nei selvatici si è isolato l’Ag del pesti virus ma con l’ELISA solo nel
capriolo e nel cervo.
Si manifesta con vari quadri clinici:
Affezioni della sfera genitale (=vacche da latte)
Forme respiratorio ed enteriche (=vitelloni da ingrasso)
Forme emorragiche
Malattia delle mucose
La malattia ha oggi raggiunto una diffusione mondiale, essendo presente in tutti i paesi dove è praticato
l’allevamento dei vocini. In italia sono state documentate alte prevalenze d’infezione sia in allevamenti di
vacche da latte, sia nell’allevamento di bovini da carne spesso associate a focolai di malattia respiratoria ed
enterica.
Eziologia:
famiglia: flaviviridae
genere: pesti virus
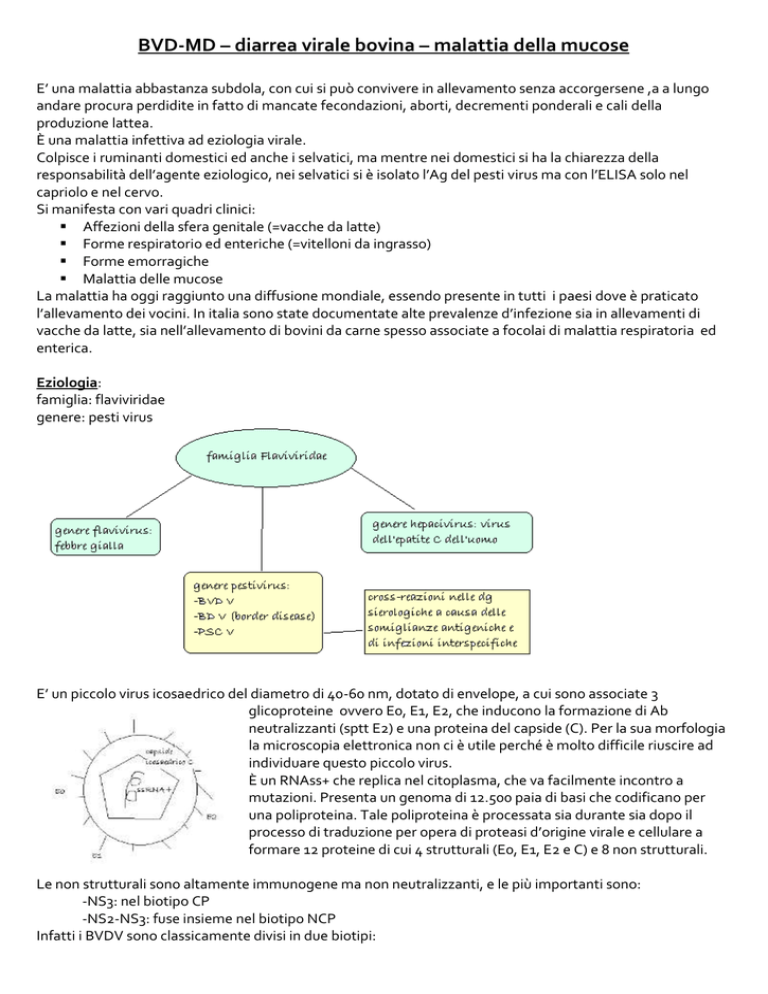
E’ un piccolo virus icosaedrico del diametro di 40-60 nm, dotato di envelope, a cui sono associate 3
glicoproteine ovvero E0, E1, E2, che inducono la formazione di Ab
neutralizzanti (sptt E2) e una proteina del capside (C). Per la sua morfologia
la microscopia elettronica non ci è utile perché è molto difficile riuscire ad
individuare questo piccolo virus.
È un RNAss+ che replica nel citoplasma, che va facilmente incontro a
mutazioni. Presenta un genoma di 12.500 paia di basi che codificano per
una poliproteina. Tale poliproteina è processata sia durante sia dopo il
processo di traduzione per opera di proteasi d’origine virale e cellulare a
formare 12 proteine di cui 4 strutturali (E0, E1, E2 e C) e 8 non strutturali.
Le non strutturali sono altamente immunogene ma non neutralizzanti, e le più importanti sono:
-NS3: nel biotipo CP
-NS2-NS3: fuse insieme nel biotipo NCP
Infatti i BVDV sono classicamente divisi in due biotipi:
Dalla fine degli anni ’80 sono stati osservati gravi casi di diarrea virale bovina in soggetti adulti
immunocompetenti che manifestavamo forme emorragiche. In alcuni di questi focolai a carattere
emorragico sono stati isolati ceppi non citopatogeni di BVDV genotipicamente diversi da quelli classici del
virus della diarrea virale bovina, questi nuovi ceppi sono attualmente raggruppati sotto la denominazione di
BVDVII (queste forme emorragiche primitivamente segnalate in canada e negli USA sono state
successivamente descritte anche in alcuni paesi europei quali Belgio, Francia e Italia).
Pertanto il BVDV presenta 2 genotipi:
presentano differenze a
livello di genotipo ed
antigenicamente. Sono
responsabili di diverse
patologie. NON SONO
SIEROTIPI
Effetti biologici:
1. diarrea virale vovina o contaminazioni di cellule e siero fetale bovino: determinata dal NCP genotipo 1
2. malattia delle mucose: determinata dal CP genotipo 1
3. forma emorragica: determinata dal NCP genotipo 2. Dà mortalità nei soggetti adulti
Resistenza:
-stabile tra pH 6 e 9 (max stabilità 7.4)
-sensibile ai raggi UV
-sensibile ai solventi di lipidi (etere e cloroformio), alla tripsina e ai normali disinfettanti
-sensibile al caloore: instabile a T> 40°C; inattivato in 20 minuti a 56°C
-resiste bene alle basse temperature: si conserva bene a -70°C, meglio se liofilizzato.
In definitiva è sufficientemente resistente per trasmettersi anche per via indiretta. In più si è ingegnato per
trasmettersi e resistere mediante gli individui immunotolleranti.
Coltivazione:
cresce su colture cellulari di bovino, provenienti sptt da cell embrionali o di vitello (polmone –
pneumociti-, reni , testicolo)
cresce anche su colture cellulari di testicolo di ovino e rene di suino
ottima crescita su linee continue MDBK (rene bovino)
in vivo replica bene nel coniglio
→i ceppi CP danno effetto CP dopo circa 3-7gg (vacuolizzazione del citoplasma, picnosi e cario ressi del
nucleo).
Il bovino sa cui si fanno le colture cellulari potrebbe essere infetto con ceppo NCP, che non dà sintomatologia
ma interferisce con il risultato della coltura. Le colture vanno per questo prima testate.
Recettività: isolato da varie specie di Artiodactyla domestici e selvatici (bovini, ovicaprini, bufali, cervo,
capriolo). La sieropositività evidenziata in molte specie di ruminanti selvatici ma il virus è stato isolato solo
nel cervo e nel capriolo. È stata anche evidenziata la presenza di Ab nell’uomo, ma non è una zoonosi. Anche
il suino si siero converte.
Trasmissione:
-orizzontale:
secreti ed escreti (sptt scolo nasale e saliva) di animali persistentemente infetti PI che albergano il
virus non citopatogeno. Sono soggetti Ab- e Ag+ che continuano ad eliminare il virus per tutta la loro
vita e sono il punto focale dell’epidemiologia della malattia. Hanno contratto il virus per via
intrauterina tra l’80° e il 120° giorno di gravidanza. Solo a volte hanno uno sviluppo corporeo ridotto
ed una costituzione debole; ma la maggior parte delle volte sono indistinguibili dai vitelli sani.
Secreti ed escreti di soggetti in forma acuta che in tal modo eliminano il virus per 8-15gg
Fecondazione artificiale o naturale con seme infetto (ormai questa evenienza non si manifesta più)
Fomites: strumenti veterinari contaminati con sangue o seme infetto
ET: infatti si usano terreni nutritivi con alte percentuali di SFB – siero fetale bovino – che può essere
contaminato da BVDV NCP
Vaccini vivi attenuati contaminati, cioè prodotti su colture cellulari di orgine bovina contaminate dal
pesti virus
Insetti ematofagi: solo sperimentalmente
Verticale: solo il ceppo NCP è in grado di attraversare la placenta ed infettare il feto (in certi casi inducendo
uno stato di immunotolleranza). L’infezione di una bovina gravida con un ceppo CP porta sempre a morte del
feto.
Patogenesi:
Ceppo NCP: nel bovino adulto immunocompetente può dare:
-forma subclinica: con poca sintomatologia
-forma clinica:
_lieve
_grave
Per quanto riguarda l’infezione in una bovina gravida, l’esito è differente a seconda del momento
dell’infezione stessa:
Ceppo CP:
Se è presente tale ceppo si manifesta la malattia delle mucose. Tale forma è tipica dei vitelli PI tra i 6 mesi e i
2 anni che infettati dal ceppo NCP possono dare origine nel loro orgnaismo alla trasformazione da NCP a CP.
Questa trasformazione avviene per:
Inserzione di sequenze di RNA di origine cellulare
Duplicazione e riarrangiamento di una sequenza del genoma virale della regione NS2
Mutazioni puntiformi nella regione NS2
Delezione di tratti del genoma
In generale l’inserzione e la duplicazione sono le più comuni ma sono tante e diverse le modificazioni del
genoma virale e sono tutte finalizzate all’espressione della proteina NS3.
Importante è capire la plasticità di tale virus che tramite complesse trasformazioni riesce sempre a
raggiungere il suo scopo, cioè ad acquisire NS3
Ceppo NCP del genotipo 2. possibilità:
1. piastrine distrutte, consumate o sequestrate a livello periferico per un’azione diretta del virus
2. azione lesiva del virus nel midollo osseo
→trombocitopenia.
Sintomatologia:
Forma emorragica:da NCP gen 2:
forma abbastanza grave, con una letalità del 20%
provocata dal ceppo NCP così com’è sena nessuna trasformazione nel genoma virale
colpisce i soggetti adulti immunocompetenti
trombocitopenia: diatesi emorragica con epistassi, petecchie ed emorragie sulle mucose, diarrea
emorragica
lesioni sulle mucose simili a quelle della malattia delle mucose
febbre
Diarrea virale: da NCP gen 1:
incubazione 7-10gg
morbilità 70-80% ma letalità scarsa o assente ed esito in guarigione
spesso si ha la forma asintomatica
forma subclinica:febbre,conseguente a viremia, leucopenia, inappetenza , calo della produzione lattea
forma acuta: diarrea e erosioni alle mucose gastroenteriche, depressione
come già detto l’evoluzione tende ad una guarigione spontanea ma l’attività immunodepressiva del
BVDV predispone ad infezioni da patogeni opportunisti (es infezioni respiratorie sostenute da
pasteurella haemolytica, IBR virus, virus respiratorio sinciziale e parainfluenzavirus 3)
Malattia delle mucose: CP genotipo 1: ricorda che si manifesta solo nei vitelli persistentemente infetti tra i 6
mesi e i 2 anni in cui il ceppo NCP si è trasformato in CP:
bassa morbilità ma elevata letalità
febbre, leucopenia, depressione, debolezza, tachipnea, tachicardia
anoressia, dimagrimento, disidratazione, acidosi e diminuzione della ruminazione
calo della produzione lattea
pelo arruffato e brutto
edema della cornea, lacrimazione e scolo oculare purulento
diarrea acquosa e profusa con sangue fresco o digerito e stampi fibrosi, forte tenesmo (sintomi uguali
alla PSC) – c’è un detto somalo che dice che “l’animale si caga l’anima”
erosioni delle mucose, spt gastroenteriche ( a livello di abomaso e placche del peyer) e nel cavo orale
(colletti dentari, gengive, lingua, palato, commessure buccali). Queste sono lesioni erosive e
ulcerative a margini irregolari ma netti che avvengono in precedenti focolai necrotici
lesioni podali e genitali
ptialismo e scialorrea
morte in pochi giorni o settimane.
Diagnosi di laboratorio
Vista l’elevata variabilità della sintomatologia la diagnosi necessita di una conferma di laboratorio. Le
indagini devono essere svolte anche solo per deficit riproduttivi poiché ci interessa individuare i PI.
Diretta:
1. isolamento virale (con immunofluorescenza o immunoperossidasi): dall’animale vivo possono usare
come materiali da destinare alla ricerca virologica il sangue, il siero, il seme, lo scolo nasale, le feci.
Dall’animale morto si usano invece milza, fegato, polmone, rene, tonsille, intestino, feti. Il prelievo va
effettuato in condizioni di asepsi e il campione va trasportato al laboratorio refrigerato. L’isolamento
si fa su colture cellulari a basso numero di passaggi di rene, testicolo, turbinati. Nel caso di ceppi NCP
2.
3.
4.
5.
si effettua una colorazione con immunofluorescenza o immunoperossidasi. Per i ceppi CP invece è
possibile evidenziare l’effetto citopatico oltre che effettuare la colorazione o la siero neutralizzazione.
I vantaggi dell’isolamento virale risiedono spt sulla sua elevata sensibilità. Per non alterare il nostro
test è necessario che le colture cellulari su cui si effetua l’isolamento non siano contaminate da BVDV.
ELISA: la maggior parte dei kits elisa attualmente in commercio utilizzano i MoAb verso NS3/NS2NS3. Come materiale di partenza si può usare il sangue intero o meglio solo i leucociti (in quanto il
virus ha localizzazione prevalentemente intracellulare nella frazione leucocitaria). Con questo test si
possono rilevare sia i soggetti PI sia i soggetti con infezioni acute.
Flow-citometry: le cellule vanno fatte reagire con Ab fluorescenti e vengono poi analizzate con
citometro a flusso: cioè le cellule passano in fila attraverso un raggio laser e se hanno reagito con Ab
emettono fluorescenza captata da appostiti rilevatori.
immunoistochimica: tecnica che viene impiegata più per scopi di ricerca. Si può effettuare su un
prelievo autoptico o biopsia su un padiglione auticolare.
RT-PCR (reverse transcriptase-pcr): è una metodica molto sensibile che si basa sulla estrazione di RNA
virale da siero, sangue, tessuto, dalla scelta del primer (possibilmente in zone non variabili, ma in zone
no trascrizionali) la sua trascrizione in DNA (retro trascrizione) che viene quindi amplificato e
visualizzato su un gel.