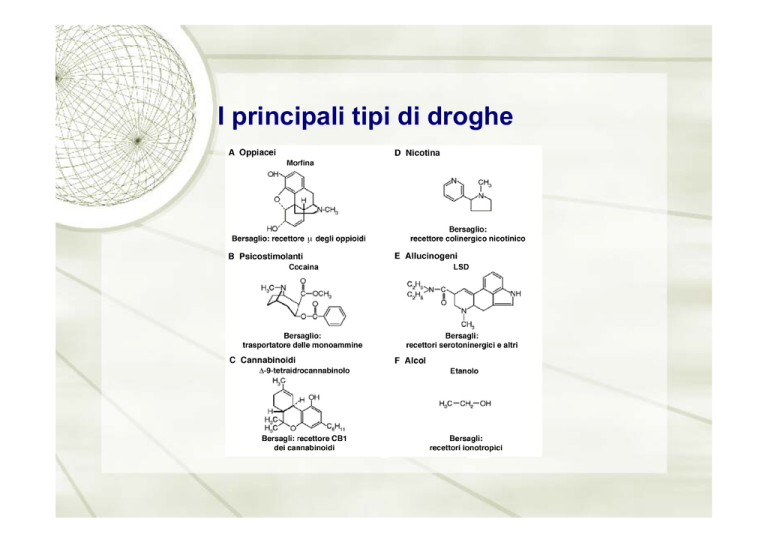
I principali tipi di droghe
Droghe e basi neuronali della gratificazione
•
Tutte le sostanze che danno dipendenza aumentano il
tono dopaminergico del sistema mesolimbico, in
particolare dell’accumbens (shell) e della VTA,
mediante meccanismi diretti o indiretti.
•
Ciò è dovuto alla complessa regolazione del rilascio di
dopamina da parte dei neuroni di tali strutture.
1 - Analgesici stupefacenti
•
IL DOLORE: È causato dall’attivazione di nervi periferici
sensoriali ad opera di stimoli meccanici, termici, chimici e da
ferite che agiscono sui nocicettori. Questi nervi utilizzano come
neurotrasmettitore la sostanza P, un neuropeptide che attiva i
neuroni spinali i quali trasmettono lo stimolo doloroso al tronco
dell’encefalo, al talamo e da qui ai centri corticali che lo
elaborano e lo portano alla coscienza.
•
Neuroni del tronco dell’encefalo inibiscono i neuroni sensoriali
che rilasciano la sostanza P rilasciando peptidi oppioidi, altri
neuropeptidi che provocando analgesia.
•
Gli analgesici stupefacenti sono agonisti dei peptidi oppiodi,
poiché agiscono, attivandoli, gli stessi recettori neuronali diffusi
nel midollo spinale e nelle strutture encefaliche. Tali sostanze
hanno perciò azione centrale e provocano analgesia.
Effetti cellulari degli analgesici stupefacenti
•
•
•
•
•
•
Sono stati largamente studiati sui neuroni del Locus Coeruleus
del ratto.
Gli oppiacei agiscono sui recettori metabotropi dei peptidi
oppioidi, che si dividono in tre tipi: (mu), (kappa) e (sigma).
L’attivazione in acuto di tali recettori inibisce, attraverso la
proteina Gi, l’adenilato ciclasi producendo una diminuzione della
concentrazione di cAMP e la riduzione dell’attività della Protein
Kinasi A.
Il risultato è una diminuzione dell’attività neuronale per l’apertura
di canali di rettifica per gli ioni K+ che iperpolarizzano la
membrana.
L’esposizione cronica agli oppiacei produce invece una
regolazione verso l’alto (upregulation) del sistema del cAMP che
aumenta l’attività neuronale di base e richiede maggiori quantità
di droga perché si osservi un effetto farmacologico (tolleranza).
Tali cambiamenti coinvolgono l’espressione genica attraverso
l’attività di un fattore di trascrizione che risponde al cAMP
(CREB), e sono perciò a lungo termine.
Gli oppiacei
Comprendono l’oppio e i suoi derivati: Oppio grezzo, morfina,
codeina, eroina. Ad essi si deve il nome di oppioidi endogeni
dato ai peptidi che legano gli stessi recettori.
La parte in rosso della morfina
dell’encefalina, un peptide oppioide.
la
rende
agonista
I comuni oppiacei
La morfina è il più potente analgesico conosciuto. L’eroina è un
derivato semisintetico della morfina e attraversa più velocemente
la barriera ematoencefalica, ma è poi riconvertita in morfina.
La morfina stimola i recettori talamici e corticali degli oppiacei e
ha effetto euforizzante; altera permanentemente il sistema dei
peptidi oppioidi.
Provoca depressione respiratoria e spesso con essa la morte del
tossicodipendente (overdose).
Antagonisti degli oppiacei sono il naloxone e il naltrexone.
L’agonista terapeutico degli oppiacei è il metadone (orale).
Effetti di rinforzo degli analgesici
stupefacenti
Esperimenti condotti sui ratti hanno mostrato che:
•
iniezioni dirette di oppiacei nella VTA producono
rinforzo;
•
iniezioni dirette di oppiacei nell’accumbens aumentano
notevolmente il livello di DA.
Meccanismo: gli oppiacei agiscono riducendo l’attività dei
neuroni GABAergici, che inibiscono i neuroni
dopaminergici del sistema mesolimbico; tale azione
aumenta il rilascio di DA e produce rinforzo. Ciò
dimostra l’associazione fra l’aumento di DA e il concetto
psicobiologico di rinforzo.
Effetti psicofisici degli analgesici
stupefacenti
•
L’eroina dà un flash di intenso piacere, proporzionale alla
quantità assunta e alla velocità di saturazione dei recettori.
•
Dopo gli effetti iniziali, solitamente si accusa sonnolenza per
diverse ore per la compromissione delle funzioni mentali
(azione inibitoria sul Locus Coeruleus).
•
Con lo sviluppo della dipendenza si presentano crisi di
astinenza, caratterizzate da dolori diffusi, insonnia, diarrea,
vomito, che si riducono solo dopo una settimana.
2 - Psicostimolanti
•
Cocaina e anfetamine. Agiscono direttamente sui neuroni
dopaminergici aumentando con meccanismi diversi il tono
della DA.
Struttura
molecolare
e
azione
cellulare
del-la cocaina.
•
La cocaina inibisce la ricaptazione presinaptica della DA
bloccandone il trasportatore di membrana (DAT).
Effetti di rinforzo degli psicostimolanti
•
Le anfetamine inibiscono la ricaptazione della DA e ne
provocano un aumentato rilascio.
•
Il risultato è un aumento della stimolazione dei neuroni del
sistema mesolimbico, che costituisce l’effetto di rinforzo
diretto. Sono potenti stimolanti psicomotori determinando
euforia, eccitazione, insonnia e inappetenza. Il loro uso
cronico porta ad aggressività, violenza, psicosi e grave
anoressia.
•
Inducono
positivo.
dipendenza
psicologica
da
condizionamento
Effetti psicofisici degli psicostimolanti
•
Spesso, dopo l’euforia iniziale, può manifestarsi disforia fino ad
attacchi di panico, comportamento violento e disturbi
dell’umore.
•
Gli effetti somatici hanno natura neurovegetativa e dipendono
dall’at-tivazione del tono noradrenergico che segue quella del
tono della DA (ipertensione arteriosa, tachicardia, nausea,
tremore).
•
L’azione cronica della cocaina può indurre stati depressivi e
disturbi psichiatrici, psicosi, allucinazioni.
•
Le crisi di astinenza sono caratterizzate da
rallentamento psicomotorio che interferiscono
funzionamento sociale.
disforia,
con il
Modificazioni cellulari da uso cronico di
psicostimolanti
•
L’encefalo di soggetti con storia di abuso di cocaina mostra un aumento
della densità dei recettori della DA nel nucleo accumbens. Il craving per
la cocaina perciò è associato alla sovraregolazione di tali recettori e alla
necessità di un aumentato tono dopaminergico capace di tenerli attivi.
Densità dei recettori DRD3
nel nucleo striato ventrale di
un soggetto normale (sn) e
uno deceduto per overdose
di
coca-ina
(dx).
Cd,
caudato;
NA
nucleo
accumbens; Pt putamen. Da
Staley and Mash, 1996).
3 - Eccitanti - I
•
La nicotina stimola i recettori nicotinici dell’acetilcolina
producendo,
principalmente,
aumento
dell’attività
psicomotoria.
•
I recettori nicotinici nel SNP sono concentrati nelle placche
motrici (le giunzioni neuromuscolari). Nel SNC sono soprattutto
nel talamo e nella corteccia: i recettori nicotinici sono presenti
sui neuroni dopa-minergici e serotoninergici del sistema
mesolimbico dove mediano la liberazione di dopamina e con
essa la sensazione di gratificazione.
•
La dipendenza è sia fisica che psicologica.
Struttura
molecolare
nicotina.
della
Altri effetti della nicotina
•
Oltre che sul sistema mesolimbico, la nicotina agisce anche su
alcuni neuroni del Locus Coeruleus, attivandoli. Ciò provoca
aumento delle performances intellettive e un miglioramento delle
funzioni cognitive. A differenza di altre droghe, perciò, la nicotina
non genera confusione né turbe psichiche o distacco sociale.
•
La nicotina agisce anche sull’ipotalamo, aumentando la sintesi di
LH e prolattina, e quella di ACTH, con conseguenze rapide sulla
sintesi di cortisolo, l’ormone dello stress, e benefici sulla
percezione di situazioni stressanti.
•
La crisi d’astinenza è dovuta a meccanismi compensatori,
compresa un ’ aumentata ricaptazione di DA mesolimbica e
desensibilizzazione/ sensibilizzazione recettoriale, con disforia,
depressione, fame, agitazione, irritabilità (già osservate per la
cocaina).
3 - Eccitanti - II
•
La caffeina è un antagonista dell’adenosina, una purina che
produce normalmente sedazione del comportamento, inibendo la
liberazione di molte classi di neurotrasmettitori (NA, DA, ACh, Glu).
•
Bloccando i recettori purinergici, la caffeina determina una
stimolazione comportamentale dovuta soprattutto all’aumento dei
livelli di adrenalina e noradrenalina.
4 - Allucinogeni o psichedelici
•
Sono sostanze con struttura simile a quella dei principali neurotrasmettitori. Comprendono:
•
ANTICOLINERGICI: (ad es. la scopolamina)
intossicazione, amnesia e delirio bloccando
dell’acetilcolina.
•
CATECOLAMINICI:
sono
agonisti
dei
recettori
delle
catecolamine. La mescalina, ottenuta dal peyote, è molto simile
alla noradrenalina. Ha ef-fetti di tipo lotta/fuga/spavento.
•
SEROTONINICI: Ad ed., LSD e psilocibina. Sono agonisti della
serotonina. L’LSD attiva in particolare i recettori 5-HT2A dei
neuroni del proencefalo.
•
I derivati sintetici delle anfetamine, come l’extasy (MDMA)
causano deplezioni acute di serotonina e distruzione
irreversibile di neuroni serotoninergici nel proencefalo: l’alta
tossicità dell’MDMA ne impedisce anche l’uso farmacologico
sull’uomo.
producono
i recettori
Marijuana - I
Nella marijuana e nell’hashish esistono oltre 400
differenti composti, 61 dei quali sono cannabinoidi.
Una foglia di Cannabis
indica da cui si produce la
marijuana.
Marijuana - II
L’unico cannabinoide ad accertata
attività
psichica
è
il
delta-9tetraidrocannabinolo (THC). Le comuni
preparazioni
superano
raramente
concentrazioni del 7% di THC.
Strutturalmente la molecola è
simile agli steroidi, ma agisce su
una
classe
di
recettori
metabotropi denominati CB1 e
CB2.
Marijuana - III
Il THC lega recettori endogeni diffusi nell’intero encefalo, che
alterano il funzionamento delle cellule bersaglio, producendo effetti
di tipo motorio, cognitivo, psichedelico e analgesico. I recettori,
CB1 e CB2, sono recettori di tipo metabotropo accoppiati alle
proteine Gi, che inibiscono l’adenilato-ciclasi. Oltre che
nell’encefalo, sono diffusi anche in diversi organi.
I
ligandi
endogeni
identificati
di
questi
recettori sono l’anandamide (ANA) e il 2-arachidonoilglicerolo
(2-AG),
neurotra-smettitori lipidici
non
canonici
che
sembrano
agire
come
messaggeri retrogradi.
Marijuana - VI
Il THC induce il rilascio di DA nel nucleo accumbens. È probabile che
la droga agisca mediante interazione con il sistema oppioide
endogeno, capace di modulare il rilascio di dopamina. La dipendenza
da THC è principalmente di tipo psicologico.
Si prospetta da tempo la possibilità di un uso terapeutico del THC e
dei suoi derivati per:
dolore, glaucoma, inappetenza, sclerosi multipla
Tuttavia, l’uso cronico di THC provoca un declino cognitivo,
apparentemente dovuto a neurotossicità (induzione di morte per
apoptosi). Un simile mecca-nismo potrebbe agire nelle gonadi nella
quali gli endocannabinoidi sembrano coinvolti in processi di
controllo della proliferazione/morte cellulare insieme a ormoni, i.e.
l’FHS. In particolare, mentre l’FSH stimola la vitalità e la proliferazione di cellule follicolari e del Sertoli, mentre l’ANA induce la
morte cellulare per apoptosi. L’uso cronico di marijuana potrebbe
essere un fat-tore di rischio per la sterilità.
5 – Benzodiazepine
(ansiolitici)
Le benzodiazepine (BDZ) - ad es.
Diazepam – sono farmaci
utilizzati
nel
trattamento
dell’ansia, ad azio-ne ipnotica.
Il bersaglio molecolare di tali
farmaci è il recettore ionotropo
del GABA, detto GABAA.
Il
loro
effetto
consiste
nell’intensifica-zione dell’azione
del GABA, con au-mentata
sedazione neuronale.
Sezione
GABAA
del
recettore
Alcune
benzodiazepi
ne
Formula
BDZ
generale
delle
Caratteristiche delle benzodiazepine
Proprietà:
sedative
ipnotiche
ansiolitiche
anticonvulsivant
i
anestetiche
miorilassanti
Differenze
farmacodinamiche
e
farmacocineti-che determinano sostanziali
differenze cliniche, ma solo in termini di:
Potenza
Inizio e durata degli effetti clinici
Tipo e frequenza degli effetti avversi
A dosaggi adeguati tutte le BDZ sono
equivalen-ti nell’attività ansiolitica e in
quella sedativo-ipnotica.
Complicanze delle benzodiazepine - I
ABUSO
Consiste nell’uso eccessivo, persistente o sporadico, e
incongruente con una pratica medica accettabile.
Alcuni pazienti aumentano spontaneamente il dosaggio e
assumono un comportamento di richiesta insistente del
farmaco.
Il rischio di dipendenza da BDZ differisce fra i vari composti ed
è tanto più alto quanto più veloce è l’inizio dell’azione
farmacologica (rinforzo positivo).
ASSUEFAZIONE
Bisogno di aumentare la dose per mantenere lo stesso effetto
sedativo (già entro la prima-seconda settimana di uso), ipnotico
(più lento).
Complicanze delle benzodiazepine - II
DIPENDENZA FISICA
Dopo alcuni mesi di uso, si sviluppa la dipendenza, con i
seguenti sintomi d’astinenza:
irrequietezza, irritabilità
ansia
insonnia
depersonalizzazione
cefalea
fotofobia
iperacusia
ipersensibilità visiva
Si risolvono spontaneamente in poche settimane.
La sospensione della terapia dev’essere graduale.
6 - Alcool etilico
•
•
•
•
L ’ alcool etilico rappresenta, probabilmente, la più antica e
diffusa sostanza psicoattiva di abuso.
La dipendenza patologica da alcool, pur avendo basi
neurobiologiche ed aspetti di predisposizione geneticamente
determinati, si correla, nel tempo, a disturbi della sfera psicoaffettiva, mentale e sociale.
L’etanolo è agonista indiretto dei recettori GABAA. L’etanolo è
anche antagonista indiretto dei recettori NMDA del glutamato in
diverse aree cerebrali compreso l’ippocampo, che è la sede
delle funzioni mnestiche, alterando la memoria.
Ciò modifica l’attività di numerose popolazioni neuronali: nel
sistema mesolimbico, stimola l ’ attività elettrica dei neuroni
dopaminergici ed il rilascio di DA, con rinforzo positivo.
‘Alcool etilico
•
•
•
L’alcolista non può fare a meno dell’alcool poiché in sua assenza
egli sente fortemente la sindrome d’astinenza, uno stato
caratterizzato da sintomi psicofisici quali ansia, depressione,
tremori, delirio e convulsioni. Per l’alcolista, perciò, l’alcool
produce un potente rinforzo negativo.
Nel craving alcolico è principalmente coinvolta la regolazione
glutamatergica (NMDA) della VTA che si sposta verso l’alto
diminuendo in assenza di etanolo il rilascio di DA.
L’abuso di alcool è spesso associato a quello di altre droghe, con
conseguenze molto più gravi dell’abuso separato delle singole
sostanze. Questo è tuttavia, un problema comune a diverse
droghe.