L’energia e il trasporto
Copyright © 2006 Zanichelli editore
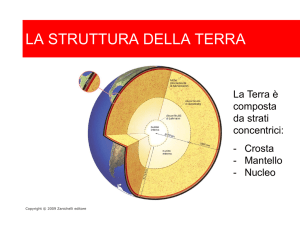
La cellula e l’energia
L’energia è la capacità di
produrre lavoro
• Tutti gli organismi hanno
bisogno di energia per
vivere.
• L’energia è definita
come la capacità di
effettuare un lavoro
(cioè di spostare un
corpo modificandone il
moto o lo stato di
quiete).
Copyright © 2006 Zanichelli editore
Energia cinetica e potenziale
• L’energia cinetica è l’energia posseduta dai corpi in
movimento.
• L’energia potenziale è l’energia immagazzinata
(dovuta alla posizione del corpo) e può essere
trasformata in energia cinetica.
Copyright © 2006 Zanichelli editore
Primo principio della termodinanica
Il primo principio della termodinamica stabilisce che:
• l’energia può essere trasformata da una forma all’altra;
• l’energia non può essere né creata né distrutta.
Copyright © 2006 Zanichelli editore
Secondo principio della termodinanica
Il secondo principio della termodinamica afferma che durante le
trasformazioni dell’energia aumenta il disordine (o entropia) e
parte dell’energia è persa sotto forma di calore.
Copyright © 2006 Zanichelli editore
Disordine
Il passaggio da una forma ordinata a una disordinata è spontaneo (la vostra
stanza)
Qualsiasi trasformazione subisca l’energia, rende l’Universo più “disordinato.
Forme di energia nei viventi sono forme di energia potenziale depositate nelle
molecole, formate da legami chimici che uniscono i loro atomi.
I viventi sono isole a basso contenuto di disordine (sistemi complessi altamente
organizzati) immersi in un universo che continua ad aumentare il proprio
disordine.
“Bateson”
Copyright © 2006 Zanichelli editore
Energia in uscita o in entrata?
Copyright © 2006 Zanichelli editore
Reazioni endoergoniche
Le reazioni chimiche consentono di immagazzinare
o di liberare energia
Le reazioni endoergoniche assorbono energia e
danno origine a prodotti ricchi in energia potenziale
(con un livello di energia chimica superiore a quella
delle sostanze di partenza).
Energia potenziale
delle molecole
Prodotti
Copyright © 2006 Zanichelli editore
Energia assorbita
Reagenti
Quantità
di energia
assorbita
Reazioni esoergoniche
Le reazioni esoergoniche liberano energia e danno
origine a prodotti che contengono meno energia
potenziale dei loro reagenti.
Energia potenziale
delle molecole
Reagenti
Quantità
di energia
liberata
Energia liberata
Prodotti
Copyright © 2006 Zanichelli editore
Accoppiamento energetico
• Le cellule compiono migliaia di reazioni chimiche
(esoergoniche ed endoergoniche).
• L’insieme di queste reazioni costituisce il
metabolismo cellulare.
• L’accoppiamento energetico utilizza le reazioni
esoergoniche per far avvenire le reazioni
endoergoniche.
Copyright © 2006 Zanichelli editore
Il ruolo dell’ATP
Nella cellula l’ATP funge da
navetta per il trasporto
dell’energia chimica
• L’ATP fornisce l’energia
necessaria per tutte le
forme di lavoro cellulare.
• In una molecola di ATP
l’energia risiede nei
legami covalenti che
uniscono i gruppi fosfato.
Copyright © 2006 Zanichelli editore
Il ruolo dell’ATP
• L’ATP libera energia utile per le reazioni
endoergoniche attraverso la fosforilazione.
• La fosforilazione è il trasferimento di un gruppo
fosfato a una molecola per renderla più reattiva.
ATP
Lavoro chimico Lavoro meccanico Lavoro di trasporto
Membrana della proteina
Proteina
motrice
P+
Soluto
P
Reagenti
P
P
P
Prodotto
Molecola formata
Proteina mobile
ADP+ P
Copyright © 2006 Zanichelli editore
P
Soluto trasportato
Fosforilazione
La fosforilazione è un processo mediante il quale un
gruppo fosfato (PO43–) viene aggiunto a una molecola.
Si tratta di una reazione molto importante perché in
genere quando una molecola viene fosforilata, il suo
contenuto energetico aumenta ed essa è in grado di
partecipare a una data reazione.
Copyright © 2006 Zanichelli editore
Fosforilazione
Il lavoro cellulare può essere sostenuto nel tempo
perchè l’ATP è una molecola rinnovabile, che viene
rigenerata dalle cellule.
ATP
Energia prodotta
dalle reazioni
esoergoniche
Energia utile
per le reazioni
endoergoniche
ADP +
Copyright © 2006 Zanichelli editore
P
Fosforilazione
Copyright © 2006 Zanichelli editore
Enzimi
Gli enzimi accelerano le reazioni chimiche della
cellula abbassando la richiesta energetica
Perchè una reazione chimica inizi, i reagenti devono
assorbire una quantità di energia chiamata energia di
attivazione (EA).
Enzima
Barriera EA
Reagenti
Contenitore 1
Copyright © 2006 Zanichelli editore
Prodotti
Contenitore 2
Enzimi
• Un enzima è una molecola proteica che si comporta
come catalizzatore biologico.
• Un enzima può abbassare l’energia di attivazione
necessaria per avviare una reazione chimica.
EA senza
enzima
EA con
enzima
Energia
Reagenti
Differenza
netta
di energia
Prodotti
Direzione della reazione
Copyright © 2006 Zanichelli editore
Come lavorano gli enzimi
Ogni reazione cellulare è catalizzata da un enzima
specifico
• Gli enzimi hanno strutture tridimensionali
caratteristiche che determinano le reazioni
chimiche che essi sono in grado di catalizzare in
una cellula.
• La sostanza su cui agisce l’enzima, ossia il
reagente, si chiama substrato.
Copyright © 2006 Zanichelli editore
Esempio di reazione catalizzata da un enzima:
1 Enzima disponibile
con il sito attivo
vuoto
Sito attivo
Glucosio
Substrato
(saccarosio)
Il substrato
2 si lega all’enzima
che subisce
un adattamento indotto
Enzima
(saccarasi)
Fruttosio
H2O
4 I prodotti
vengono liberati
3 Il substrato
si scinde
nei prodotti
Copyright © 2006 Zanichelli editore
Specificità degli enzimi
La maggior parte degli enzimi presenta una notevolissima
specificità per la reazione catalizzata e per i substrati
coinvolti. La specificità è legata a diversi fattori che
caratterizzano l'associazione tra il substrato ed il sito
attivo, come la conformazione della struttura delle
molecole, le cariche elettriche, la natura idrofilica o
idrofobica
Copyright © 2006 Zanichelli editore
Ambiente cellulare e attività enzimatica
L’ambiente cellulare influenza l’attività degli enzimi
• La temperatura, la concentrazione dei sali e il pH
influenzano l’attività enzimatica.
• Per funzionare, alcuni enzimi richiedono molecole non
proteiche chiamate cofattori.
• I cofattori possono essere sostanze inorganiche,
come gli ioni metallo, o molecole organiche (in questo
caso si chiamano coenzimi).
Copyright © 2006 Zanichelli editore
Inibitori
Gli inibitori bloccano l’azione degli enzimi
• Una sostanza chimica che interferisce con l’attività di un
enzima è detta inibitore.
• L’azione di un inibitore è irreversibile se si formano legami
covalenti tra inibitore ed enzima. È reversibile quando si
formano solo legami deboli (come il legame idrogeno).
Per scoraggiare i predatori di
semi, le lenticchie contengono
inibitori della tripsina che
interferiscono con la
digestione.
Copyright © 2006 Zanichelli editore
Inibitori
• Gli inibitori competitivi occupano il sito attivo di un
substrato.
• Gli inibitori non competitivi cambiano la funzione
dell’enzima modificando la sua forma.
Substrato
Sito attivo
Enzima
Legame normale del substrato
Inibitore
competitivo
Inibitore
non competitivo
Inibitore enzimatico
Copyright © 2006 Zanichelli editore
Inibitori
Copyright © 2006 Zanichelli editore
Inibitori
Copyright © 2006 Zanichelli editore
Inibitori
Gli inibitori sono spesso utilizzati come farmaci, ma
possono agire anche come veri e propri veleni. In
realtà, la differenza tra farmaco e veleno è
esclusivamente una questione di dose del
composto: la maggior parte dei farmaci, infatti, se
somministrati ad alte dosi può risultare tossica.
Un esempio di inibitore utilizzato come farmaco è
l'aspirina, che inibisce l'attività delle ciclossigenasi,
che producono le prostaglandine, mediatori
dell'infiammazione, riducendo dunque la
sensazione di dolore.
Il cianuro è invece un inibitore irreversibile che si
combina con il rame ed il ferro presenti nel sito
attivo dell'enzima citocromo c ossidasi, bloccando
la respirazione cellulare
Copyright © 2006 Zanichelli editore