LA TUBERCOLOSI
epidemiologia
• microbiologia
• patogenesi
• manifestazioni cliniche
• diagnosi
• strategie per il controllo
• prevenzione
• terapia
•
1882 KOCH: SCOPERTA DEL MICOBATTERIO TUBERCOLARE
Inizio dell’Era della Batteriologia
Mycobacterium tuberculosis complex
•
•
•
•
•
•
Mycobacterium tuberculosis o M. hominis
Mycobacterium bovis
Mycobacterium bovis BCG
Mycobacterium africanum
Mycobacterium microti
Mycobacterium canetti
Mycobacterium tuberculosis
Patogeno esclusivamente umano
• Bastoncello immobile di 1-4 x 0.3-0.6 mcm
•Debolmente Gram pos.
•Aerobio obbligato
•Optimum di temperatura a 37°C
•Non sporigeno, privo di capsula e ciglia
•Crescita lenta e su terreni arricchiti (es. terreni solidi di
Löwenstein-Jensen e di Petragnani); più rapida (circa 15 gg) con
l’utilizzo di terreni liquidi (es. Bactec, Migit), più adeguati per
l’effettuazione dei test di sensibilità a farmaci
Alcol-acido-resistenza, evidenziabile con
colorazione di Ziehl-Neelsen
La parete cellulare ricca in
lipidi conferisce particolari
caratteristiche: lento tempo
di moltiplicazione, alcolacido-resistenza, reazione
del sistema immunitario
come da “corpo estraneo”,
inefficacia della maggior
parte dei comuni antibiotici
LA TUBERCOLOSI
epidemiologia
• microbiologia
• patogenesi
• manifestazioni cliniche
• diagnosi
• strategie per il controllo
• prevenzione
• terapia
•
Dall’esposizione alla malattia
Esposizione
a caso
contagioso
Fondamentale
il
rapporto tra attivita’
battericida dei mØ,
virulenza e carica dei
bacilli
Infezione:
MTB prolifera nello spazio
extracellulare e vengono
reclutate cellule infiammatorie
Fondamentale
l’immunita’
cellulo-mediata
Non infezione:
i macrofagi alveolari
(mØ) uccidono MTB
* (il 5% va incontro a
malattia attiva entro
1-2 anni)
* Rischio molto
maggiore
negli
immunodepressi
(nel 95% dei casi le
cellule T controllano
l’infezione, che
rimane subclinica)
Infezione latente:
MTB controllato dal
sistema immunitario per
tutto il resto della vita
Riattivazione
(5% di rischio
durante il resto
della vita) *
TB attiva e sintomatica:
I soggetti possono trasmettere
la malattia ad altri
La prima infezione
L’infezione tubercolare è il risultato
dell’inalazione di MTB se la carica
batterica
è
elevata
o
le
difese
immunitarie sono inadeguate
Ingresso di MTB
negli alveoli
Fagocitosi
macrofagica
Diffusione per via linfatica
(ed eventualm. ematica)
Risposta linfocitaria
(IFN-gamma e altre
CK)
Moltiplicazione di
MTB nei macrofagi
Infezione di
altri macrofagi
Risposta attivante i macrofagi
Risposta danneggiante i tessuti
(ipersensibilità ritardata)
Russell Nature Reviews Microbiology 5, 39–47 (January 2007)
Essendo un microrganismo intracellulare,
la risposta a MTB è basata sulla
Immunità cellulo-mediata
Il ruolo dei linfociti T
•
I linfociti T CD4+ riconoscono
gli
antigeni
presentati
e
amplificano
la
risposta
immune
verso
MTB
soprattutto
attraverso
la
produzione di IFN-gamma
reclutando
altre
cellule
flogistiche
•
Diversi fattori possono ridurre
l’efficienza dei linfociti T
CD4+:
– coinfezione di HIV
– età
– farmaci
ad
azione
immunosoppressiva
Rook G.A.W. et al. Eur Respir J 2001
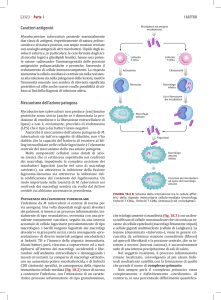
Patogenesi dell’attivazione dei linfociti T, della formazione del granuloma e
della attivazione dei linfociti B nella tubercolosi polmonare
Le due sottopopolazioni di
linfociti T-helper producono
effetti diametralmente opposti
Th1: produzione di IFNgamma,
IL-2,
TNF-beta;
attivazione
sinergica
dei
macrofagi
Th2: produzione di IL-10 e
altre linfochine che sopprimono
l’attivazione dei macrofagi
Interrelazioni
tra
macrofagi,
linfociti
e
citochine
Macrofagi IL-12 e IL-18
linfociti naive Th1 e Th2
TNFα TH1: apoptosi e
formazione di granulomi; Th2 o con
< Th1/Th2: necrosi e formazione di
caverne
RUOLO DEL TNF NELLA RISPOSTA IMMUNE
Il TNF possiede un’importanza chiave nella risposta immunitaria
cellulo-mediata verso il M. tuberculosis:
Attiva i macrofagi infettati –
(azione sinergica con IFN-γ)
Induce l’apoptosi dei macrofagi
cronicamente infetti
Stimola la produzione di nuovi
macrofagi da parte del midollo
Recluta nuovi macrofagi nel
sito d’infezione
Il
TNF
è
necessario
mantenere
l’integrità
di
granuloma esistente
per
un
L’infezione
Lo
sviluppo
dell’immunità
specifica (di norma 2-4 sett.
p.i.) e l’accumulo di MØ attivati
porta alla formazione di un
granuloma (tubercolo) nel sito
della lesione primaria
Si riscontrano linfociti, MØ,
cellule epiteloidi, cellule giganti
di Langhans
La necrosi caseosa centrale
impedisce la moltiplicazione di
MTB, che vi rimane confinato
A. Primary site of TB infection (Ghon focus) in the lung periphery,
exhibiting caseous necrosis
B. Caseous necrosis in regional hilar lymph nodes
Infezione tubercolare latente (ITL)
Infezione
subclinica
con
bacilli
tubercolari
senza
segni
clinici,
batteriologici o radiologici di malattia
manifesta. Tipicamente si tratta di
individui con Mantoux (TST) e/o test
basati sul rilascio di Interferon-gamma
(IGRA) positivi ed un Rx torace normale,
che possono essere contatti di un
precedente caso di tubercolosi.
Malattia tubercolare
Stato di malattia manifesta dal
punto
di
vista
clinico,
batteriologico e/o radiologico.
– Polmonare
•Malattia primaria
•Malattia postprimaria
– Extrapolmonare
Infezione versus Malattia (1)
L’infezione, ossia l’avvenuto contatto dell’organismo ospite
con M. tuberculosis, non significa necessariamente malattia
tubercolare. La maggior parte degli individui, infatti, viene
infettata in modo del tutto asintomatico.
Esposizione
Infezione versus Malattia (2)
Tra i soggetti immunocompetenti che vengono a contatto con il BK il 5% svilupperà
la malattia nei primi 2 anni e < 10% nel corso della vita
L’infezione da HIV è il principale fattore di rischio per lo sviluppo della TB
Rischio del 7-10% per anno (dal 3 al 13% per anno, > 30% nell’arco della vita)
Esistono alcune condizioni che aumentano il rischio di progressione della malattia
Infezione da HIV
Soggetto con Rx Torace con immagini di tb previa (es.
Tossicodipendenza
inflitrati
fibronodulari apicali, spesso con perdita di
volume) mai trattato: rischio di 2,5 volte maggior di
Infezione recente
sviluppare malattia attiva rispetto ai soggetti senza lesioni
alla Rx del torace
Soggetto con Rx Torace con immagini di tb primaria
Reperti radiografici suggestivi di pregressa TB
guarita (noduli solitari calcifici, linfonodi ilari calcificati,
ispessimento pleurico): stesso rischio dei soggetti con tb
Diabete mellito
latente senza lesioni alla Rx torace.
Silicosi
Terapia corticosteroidea prolungata (4 sett prednisone 15 mg/die)
Altre terapie immunosoppressive
Inibitori del TNFalfa
Infliximab
Trapianto di midollo, trapianto di organo solido
Adalimumab
Etanercept
Neoplasie della testa e del collo
Golimumab
Malattie ematologiche o reticoloendoteliali
Insufficienza renale cronica / emodialisi
Bypass intestinale o gastrectomia
Sindromi di malassorbimento cronico
Denutrizione o basso peso corporeo (< 10% del peso ideale)
TB & HIV/AIDS
>300 CD4
<200 CD4
Distribuzione
polmonare
Lobo superiore
Lobo medio e
inferiore
Cavitazione
Spesso presente
Tipicamente assente
Adenopatie
Rare
Comuni
TST
~70% positivo
Tipicamente
negativo
Positività
espettorato
~ 80%
~ 40%
Diffusione
extrapolmonare
10-15% dei casi
Almeno il 50% dei
casi
Tubercolosi attiva: ~ 8 milioni di nuovi casi/aa
Solo la punta dell’iceberg
TBC latente = l’ ”epidemia nascosta” 2 miliardi di persone infette
I nuovi casi di tubercolosi derivano dal “serbatoio” rappresentato dalle
persone con infezione latente
Se vogliamo ridurre i casi di tubercolosi attiva, dobbiamo eliminare il
“serbatoio” di infezione
Infezione latente
Fase attiva
bassa replicazione di M.tuberculosis
non ci sono lesioni d’organo
prevede l’uso di 1 solo farmaco per 6-9
mesi
costituisce il serbatoio della fase di
infezione attiva
1/3 della popolazione mondiale ne è affetta
replicazione attiva di M.tuberculosis
che si manifesta con lesioni d’organo
caratteristiche
necessita di una terapia anti-TBC
efficace per almeno 6 mesi con
almeno 4 farmaci
Controllo della diffusione della TB
Cura dei pazienti con malattia attiva
Diagnosi e trattamento nei pazienti con infezione tubercolare
latente (LTBI)
Punto debole di un programma di controllo è il
ritardo diagnostico
TB: trasmissione dell’infezione
CONTAGIO INTERUMANO
VIA AEROGENA: via più comune
SORGENTE D’INFEZIONE
» Espettorato di soggetti affetti da forme aperte
» Quando un soggetto espettora o starnutisce elimina nell’ambiente una
miriade di goccioline (DROPLETS) che evaporando danno origine a
particelle residue (DROPLETS NUCLEI) che rimangono nell’aria per un
lungo periodo in modo particolare nei luoghi confinati o senza ventilazione
» Un colpo di tosse di un paziente BK positivo dà origine a 3000 droplet
nuclei carichi di germi
VIA GASTROINTESTINALE: BACILLO BOVINO
VIA CUTANEA: RARA
TB: trasmissione dell’infezione
Le particelle infettanti
Goccioline di
flügge
Sospensione
nell’aria
Evaporazione
e riduzione a dimensioni di 1-5 m con
bacilli vivi e vitali
Possibilità di essere inalati fino a livello alveolare
Modello ipotetico di ricaduta delle particelle
La TUBERCOLOSI si trasmette per via aerea tramite i DROPLET NUCLEI
F
O
N
T
E
1° metro: trasmissione da
droplet
Trasmissione aerea
DROPLET NUCLEI
• diametro tra 1 e 5 μm
• hanno scarsa tendenza a
depositarsi
DROPLET
• diametro > 5 μm
• tendono a depositarsi a 1 m
dalla fonte
• si fermano alle alte vie aeree
• raggiungono con facilità le basse
vie aeree
• passano attraverso maschere
chirurgiche, tessuti
• espongono gli agenti infettivi ai
raggi UV
• possono essere bloccate da
mani, maschere
• possono proteggere gli agenti
infettivi
Streptococchi (es. pneumococco)
Tbc, morbillo, varicella
Probabilità di infezione da Agenti
Biologici a Trasmissione Aerogena
P = 1 – e–Iqpt/Q
P = Probabilità di trasmissione
I = Numero di soggetti infettivi
q = Quantità di bacilli emessi dal paziente
t = tempo di esposizione al contagio
p = ventilazione polmonare
Q = numero di ricambi d’aria
È pericoloso il contagio ?
Ogni paziente contagioso infetta 7-10
contatti
Il 40-50 % dei contatti stretti si infetta
Nei contagiati il 5-10 % si ammala di TB
3-5 % malati nei primi 2 anni
2-5 % cumulativo per il resto della vita
Nei malati:
Probabilità di guarigione = 80 %
Probabilità di morte = 1 %
Rischio di acquisizione dell’infezione
R
Età
E
0
1
0
2
0
3
0
4
0
5
0
6
0
7
0
8
0
Spiegazione: il rischio aumenta con l’età fino circa a 60 anni in funzione
dell’aumento progressivo dell’esposizione (E) che diminuisce a un certo punto
(trattini più ravvicinati)
Il contagio dipende da:
Paziente
Ambiente
Contatto
Gravità della
patologia
Volume e ricambio
d’aria
Durata
dell’esposizione
Carica bacillare *
Ricircolazione d’aria
Stato immunitario
Terapia
Filtrazione
Raggi UV
* Carica bacillare
Macrofagi
(fagocitosi) 105
Granuloma e
caseosi 105
Caverna aperta
(>>O2 > CO2) 108-109
Tassi di mutazione naturali INH 10-8-10-9, RMP 10-8-10-10, EMB 10-610-7, SM 10-5-10-8, PZ 10-3
Acocella G., 1993
Multiresistenza naturale: X gli esponenti dei tassi di mutazione alle singole
sostanze
Controllo delle infezioni in ambiente sanitario
• Fattori contribuenti alla diffusione dell’infezione TB in ambiente nosocomiale :
ritardo diagnostico nel caso fonte
ritardo di applicazione o inadeguatezza dei mezzi di protezione ambientale
contro la diffusione aerea di M. tuberculosis
mancanza di adeguata protezione respiratoria individuale
I pazienti dovrebbero essere considerati infettivi se:
» Tossiscono
» Vengono sottoposti a procedure che inducono la
tosse o provocano la formazione di aerosol
» Hanno espettorato positivo per bacilli acidoresistenti e non sono in terapia
» Hanno iniziato da poco la terapia
» Hanno una scarsa risposta clinica alla terapia
I pazienti possono essere considerati non più
infettivi se rispondono a tutti i seguenti criteri:
» Sono in trattamento adeguato
» Hanno avuto una risposta clinica significativa alla
terapia
» Hanno 3 risultati consecutivi negativi
di ricerca del BK nell’espettorato
Dovrebbe essere adottata :
- da soggetti che soggiornano in ambienti occupati
da pz con TB sospetta/confermata dove controllo
amministrativo e ambientale non possono
garantire la prevenzione dell’inalazione di droplet
nuclei infettanti
Filtranti facciali ad alta efficienza filtrante (95 →
100%), in grado di arrestare particelle <1µm