I principi della Termodinamica
La termodinamica
Interagire con l’ambiente significa
scambiare energia
In quanti modi ciò è possibile:
LAVORO e CALORE
Ogni sistema può essere osservato
dal punto di vista dei trasferimenti di
energia con l’ambiente esterno
La termodinamica studia le leggi con
cui i corpi scambiano energia (lavoro
e calore)
La termodinamica si fonda su
due principi fondamentali
Il primo principio è una
generalizzazione del principio di
conservazione dell’energia
Il secondo principio stabilisce delle
limitazioni circa le possibilità di
trasformare il calore in lavoro
(DA QUI LA MORTE)
I sistemi di cui si occupa la
termodinamica vengono descritti
utilizzando tre grandezze
macroscopiche
(pressione,volume,temperatura)
Il mulinello di Joule
• Sappiamo che possiamo riscaldare un corpo
(ad es. una massa di acqua) avvicinandolo ad
una sorgente di calore, ma anche mediante
lavoro meccanico.
• Noi tutti sappiamo che sfregando le mani
queste si riscaldano, percuotendo un oggetto
con un martello questo si scalda.
Il mulinello di Joule
• Il fisico Joule verso la metà del 1800
fece un celebre esperimento.
• Con il marchingegno in figura riscaldò
l’acqua .
• L’energia potenziale dei pesi attratti
dalla forza di gravità si trasforma in
energia cinetica e questa si trasferisce
alle pale che riscaldano l’acqua nel
calorimetro.
• Ripetendo più volte l’esperimento Joule
riuscì a determinare l’equivalente
meccanico della caloria.
• Un lavoro di 4,186 J corrisponde ad 1
caloria.
Sistemi termodinamici
• La Termodinamica è quella parte della Fisica che studia la
trasformazione del lavoro meccanico in calore e
(viceversa) del calore in lavoro meccanico.
• I suoi principi sono alla base delle macchine termiche cioè
di quelle macchine che sfruttano il calore per produrre
movimento, come ad es. il motore a vapore, il motore a
scoppio, il motore Diesel.
• Si definisce sistema Termodinamico un qualsiasi sistema
che può scambiare con l’ambiente calore e lavoro.
• Il nostro corpo ad es. è un sistema termodinamico che
irraggia calore nell’ambiente e può compiere lavoro
meccanico ad es. sollevando pesi.
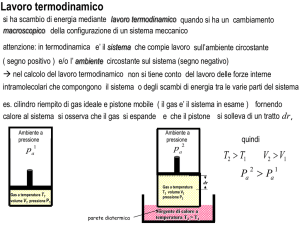
Sistemi termodinamici
Per studiare i Principi della Termodinamica noi utilizzeremo
un sistema termodinamico ideale, costituito da un cilindro
con un pistone scorrevole, all’interno del quale è contenuto
un gas perfetto. Faremo tre ipotesi:
1) il pistone è a perfetta tenuta
2) non c’è attrito tra il pistone ed il cilindro
3) mentre le pareti del cilindro sono perfettamente isolate
termicamente, la base è un ottimo conduttore di calore
Trasformazioni termodinamiche
• Trasformazione adiabatica: è una trasformazione che avviene senza
scambio di calore.
• Ciò significa che tutto il cilindro, sia le pareti che la base, è
perfettamente isolato termicamente.
• Trasformazione isoterma: è una trasformazione che avviene a
temperatura costante, obbedisce cioè alla legge di Boyle.
• Nel piano di Clapeyron (piano cartesiano avente in ascisse il Volume
e in ordinate la pressione) si ottiene un ramo di iperbole.
Non si può comprimere il
gas fino a portare il suo
volume a zero. Per quanto
piccole le molecole del
gas occuperanno un
volume.
Geometricamente
l’iperbole è asintotica
all’asse orizzontale.
Trasformazioni termodinamiche
• Trasformazione isobara: è una trasformazione che avviene a
pressione costante.
• Ciò significa che sul pistone non vengono aggiunti o tolti pesi.
• Nel piano di Clapeyron si ottiene un segmento orizzontale.
Trasformazioni termodinamiche
• Trasformazione isocora: è una trasformazione che avviene a volume
costante.
• Ciò significa che il pistone è “inchiodato”, non può muoversi.
• Nel piano di Clapeyron si ottiene un segmento verticale.
Trasformazioni cicliche
• Le trasformazioni cicliche sono trasformazioni che riportano il gas
nelle stesse condizioni di temperatura, pressione, volume.
• Si parte da un punto A e dopo una serie di trasformazioni si ritorna
in A.
Piano di Clapeyron