
SCHIZOMICETI
BATTERI
• Microrganismi unicellulari, più piccoli
complessi, capaci di autoreplicazione
( ca 1µ)
e meno
– Thiomargarita nabimiensis 10-300 µm
• Procarioti
• DNA ed RNA
• Parete batterica
eccetto micoplasmi e batteri che vivono in
habitat ad alta conc salina
•
•
•
•
Replicazione per scissione binaria
Molto abbondanti in natura cicli biologici
Per lo più autonomi
Simbiosi con altre forme di vita
– parassiti facoltativi, parassiti obbligati
• patogeni (virulenza e patogenicità)
1
Metodi di studio in microbiologia
Tradizionali
visualizzazione microscopia
• Gram, Ziehl-Neelsen forma, dimensioni, disposizione,
caratteristiche tintoriali
• IF forma, dimensioni, disposizione, sede intracellulare, identificazione
coltivazione
• terreni artificiali in vitro
– agarizzati colonie coltura pura
– brodi sospensione cellulare
• in vivo (animali, da esperimento, colture cellulari)
analisi antigene
Innovativi
metodiche biomolecolari
• analisi proteine, lipidi, acidi nucleici
2
Batteri
colorazione di Gram
Gram pos blu-violetto
Gram neg rossi
3
Batteri
• Eccetto se parassiti obbligati, si
possono coltivare su terreni artificiali,
solidi o liquidi
• esigenze nutrizionali
• temperatura ottimale
• tensione O2
• aerobiosi, microaerofilia, anaerobiosi
4
Anaerobi Batteri incapaci di svolgere in presenza
di ossigeno i processi catabolici necessari alla
produzione di energia, ATP, da utilizzare nelle
reazioni anaboliche, biosintetiche
Meccanismi molteplici
• Catalasi
•
scindono perossidi formati in presenza di ossigeno
• Superossido-dismutasi
•
protezione dall’azione nociva del radicale superossido
libero
Stretti -O2 0.5%- e meno stretti -O2 2-8%-
Gram pos Clostridium
Gram neg Bacteroides, Porphyromonas, Prevotella,
Treponema, …
5
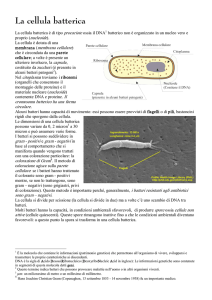
Schema di cellula procariota
6
Batteri
Il citoplasma batterico spicca per
l’alta concentrazione salina
• Salvo eccezioni, i batteri si trovano in
ambiente ipo-osmotico
richiamo di acqua lisi osmotica
I batteri devono resistere alla lisi osmotica
7
Batteri Membrana citoplasmatica
• Simile per struttura e funzioni alla
membrana delle cellule eucariotiche
• barriera di permeabilità
• trasporto di soluti
• Assenza di steroli
• Maggior contenuto proteico
• proteine non glicosilate
• Sede di funzioni appannaggio, nella cellula
eucariotica, di organuli intracitoplasmatici
• sistema trasporto elettroni
8
Strutture ACCESSORIE
Capsula [strato mucoso]
protezione
Appendici filiformi
• Pili, Fimbrie
adesività
• Ciglia, flagelli, filamenti assiali [o endoflagelli]
movimento
Granuli
9
Capsule e strati mucosi
• Esterni alla parete
• ben strutturati: capsula
• non ben strutturati: strato mucoso, glycocalix
• Polimerici, per lo più polisaccaridici
• talvolta poliaminoacidici (non proteine)
• Tendenza a essere persi nei passaggi in
coltura
• Importanti se fattori di virulenza
• Antigeni anticorpi protettivi
10
Pili (fimbrie)
Proiezioni filiformi dalla superficie
•Pili sessuali
•coniugazione ricombinazione genetica
•Adesine
•importanti se fattori di virulenza
•antigeni anticorpi protettivi
11
Parete batterica
Involucro rigido al di sopra della
membrana citoplasmatica
• Anti lisi osmotica
• Forma
• Bastoncini, cocchi, a virgola, a spirale
• Caratteristiche tintoriali
• Gram, alcool-acido resistenza
• Virulenza e patogenicità
• Sede di antigeni
12
Peptidoglicano o Mureina
componente strutturale della parete
• singola macromolecola
• lunghissimo polimero lineare,
stabilizzato da fitti legami trasversi
• avvolge la cellula, formando un
astuccio rigido e resistente
determina la forma
impedisce il rigonfiamento
13
Peptidoglicano o Mureina
Il monomero
•Due aminozuccheri
(NAM e NAG) legati
da legame glucosidico
•Polipeptide (4 o5 aa)
legato al NAM
14
Peptidoglicano o Mureina
15
Peptidoglicano Sintesi
16
Peptidoglicano Sintesi
17
Peptidoglicano
Sintesi
18
Parete batterica
La parete batterica nella sua componente
del peptidoglicano costituisce il bersaglio di
molti antibiotici
• Tali antibiotici agiscono impedendo la
sintesi del peptidoglicano
• Antibiotici diversi agiscono su momenti
diversi del processo sintetico
•assemblaggio finale transpeptidizzazione
•passaggio trans-membrana
•sintesi del monomero
19
Parete Gram neg e Gram pos
20
VIRULENZA probabilità che
• si instauri il rapporto infettivo
PATOGENICITA’ probabilità che
• si instauri la malattia
21
Virulenza
caratteristica propria e qualificante degli
agenti di infezione in quanto tali
Capacità di superare le difese dell’ospite
Probabilità che si instauri il rapporto infettivo
•Variabile estrinseca o relativa
–dipende dall’ospite che si considera
•Variabile quantitativa
–misurabile Dose Infettante 50
•Generalmente multifattoriale
–fattori di virulenza cellulari o solubili
–antigeni risposta protettiva
•Correlata alla patogenicità
22
Fattori di virulenza
• Adesine (pili o fimbrie, capsule)
• Fattori antifagocitari
– uccisione del fagocita (leucocidine)
– evasione (capsula)
– resistenza al killing intrafagocitario
Immunità
innata
• Invasine
• Proteine chelanti il Fe (IBP),
siderofori
• Fattori istotossici (proteasi)
• ……
• sIgA proteasi
• Mimetismo e variabilità antigene
acquisita
23
Patogenicità
Capacità di provocare il danno
Probabilità che si instauri la malattia
• Variabile estrinseca o relativa
– dipende dall’ospite che si considera
• Variabile quantitativa
– misurabile Dose 50
• Generalmente multifattoriale
– fattori di patogenicità cellulari o solubili
– antigeni risposta protettiva
• Non strettamente correlata alla virulenza
24
Patogenesi
Replicazione intensa
• risposta flogistica
Tossicità
• mediatori della flogosi
• alterazioni funzionali
Terapia
Prevenzione
– sintesi proteica
– rilascio neurotrasmettitori
– equilibrio idrico
25
Patogenicità microbica prevalentemente,
ma non esclusivamente, infettiva
Patogenicità svincolata dalla virulenza
• alcuni agenti producono delle tossine così
potenti che il danno e la patologia possono
essere forti e gravi anche se il germe è poco
virulento, o addirittura in mancanza di rapporto
infettivo o di reazione infiammatoria
• tetano; botulismo classico; colera
patologia anche se il germe è poco virulento, o
addirittura in mancanza di rapporto infettivo
26
Fattori di patogenicità
classicamente rappresentati dalle
esotossine
•
•
•
•
•
tossine
rilasciate da Gram pos e Gram neg
proteiche
buoni immunogeni
Vaccini
specie-specifiche
tossine binarie, citolisine, superantigeni
Sieri
alcune molto potenti
endotossina componente membrana esterna Gram neg
• LPS
• non buon immunogeno
• non specie-specifico
• tossicità indiretta rilascio di mediatori cellulari
• non molto potente
27
Esotossine
• c-AMP alterazione contenuto intracellulare
– tossina colerica diarrea
– tossina pertussica
• Sintesi proteica inibizione
– tossina difterica
• Citoscheletro alterazioni funzioni
– tossina C.difficile
• Rilascio di neurotrasmettitori interferenza
– tossina tetanica paralisi spastica
– tossina botulinica paralisi flaccida
• Superficie cellulare
– Citolisine
• Linfociti T attivazione policlonale
– superantigeni stafilococcici
28
LPS
endotossina
29
Patogenicità microbica prevalentemente,
ma non esclusivamente, infettiva
Patogenicità svincolata dalla virulenza
• alcuni agenti producono delle tossine così
potenti che il danno e la patologia possono
essere forti e gravi anche se il germe è poco
virulento, o addirittura in mancanza di rapporto
infettivo o di reazione infiammatoria
• tetano; botulismo classico; colera
patologia anche se il germe è poco virulento, o
addirittura in mancanza di rapporto infettivo
30
Disinfectant Selection Table
Compound
Chlorine
IodineIodophor
Chlorhexidine Alcohol Oxidizing
Phenol
0.01-5%
0.01-5%
0.05-0.5%
0.2-3%
0.1-2%
1-2%
Examples
Clorox
Tincture /Provodine
Novalsan
VikronS
Lysol
Roccal-D
Wavicide
Bactericidal
Good
Good
Very Good
Good
Good
Good
Good
Very Good
Bacterial Spores
Fair
Fair
Poor
Fair
Fair-Good
Poor
Poor
Good
Very Good
Good
Very Good
Good
Good
Fair
Fair
Very Good
Enveloped Viruses
Yes
Yes
Yes
Yes
Yes
Yes
Yes
Yes
Non-Enveloped Viruses
Yes
Yes
No
No
Yes
No
No
Yes
Fungicidal
Good
Good
Fair to Good
Fair
Fair
Good
Fair
Good
Effective in Organic Matter
Poor
Fair
Fair
Fair
Poor
Good
Fair
Good
Inactivated by soap
No
No&Yes
No
No
No
No
Yes
No
Effective in Hard water
Yes
No
Yes
Yes
Yes
Yes
No
Yes
Contact Time (minutes)
5 - 30
10 - 30
5 - 10
10 - 30
10-600
Residual activity
Poor
Poor
Good
Viricidal
70-95% 0.2-3%
10 - 30 10 - 30 10 - 30
Fair
Poor
Poor
Quaternary NH4 Aldehyde
Fair
31
Fair
La spora batterica
•Citoplasma povero di H2O
•Dipicolinato di Calcio
•Rivestimenti costituiti da proteine ricche in legami disulfidrici
32
La spora batterica
• Forma di resistenza
– temperature estreme
– agenti chimico-fisici
di disinfezione
– mancanza di acqua
• Metabolicamente
inattiva
• Differenziazione
della cellula
batterica
• Caratteristica di alcuni
generi
– Bacillus, Clostridium
• Non legata alla
replicazione batterica
– cellula vegetativa spora
cellula vegetativa
• La spora infetta
non in quanto tale
deve ritornare a cellula
vegetativa
33
Cinetica di sviluppo di una
popolazione batterica
Conta batterica
Concentrazione
Cellule totali
batterica
• camera contaglobuli
rispetto al tempo • stime correlate col numero di
cellule
1.
Trapianto in terreni
liquido
2. A tempi diversi
aliquota fissa
3. Conta
– concentrazione proteica
– turbidimetria
• proprietà ottiche delle sospensioni
e loro dipendenza dal numero di
particelle
Cellule vive
• subcoltivazione in agar conta
colonie
una colonia una cellula34
Fasi della crescita batterica
• Latenza
– numero costante
– attività di sintesienzimi
per utilizzazione terreno
• enzimi costitutivi/adattativi
• Crescita logaritmica
– aumento esponenziale
– attività sintetica al max
• Stasi
– numero costante o in
diminuizione
– esaurimento fattore
limitante lo sviluppo
• conte totali vs conte vitali
Differenze fisiologiche in rapporto alla fase di sviluppo
sensibilità agli antibiotici, ai fagi; ….
35
infezione acuta vs infezione cronica
Specie batterica: insieme di ceppi con alcune
caratteristiche a comune che li differenziano da altri
ceppi
Tipo Specie Genere Famiglia Ordine Classe Philum Regno
Denominazione linneiana Genere e specie
•
•
•
•
•
•
Escherichia coli
Treponema pallidum, Treponema denticola
Clostridium tetani, Clostridium botulinum
Streptococcus pyogenes, Streptococcus mutans
Porphyromonas gingivalis, Porphyromonas endodontalis
Helicobacter pylori
Differenze al di sotto della specie tipi
•
•
•
E.coli O157H7
Str. pyogenes M12
Str. mutans c
36
I farmaci antibatterici
Prodotti naturali di miceti o batteri,
antibiotici (competizione vitale) o
composti sintetici, chemioterapici
• che uccidono [battericidi] o
inibiscono [batteriostatici] la
crescita dei batteri
• MBC Concentrazione Minima Battericida
• MIC Concentrazione Minima Inibente
37
I farmaci antibatterici bersaglio e meccanismi azione
Acidi nucleici
• sintesi precursori acidi folici sulfamidici, trimethroprim
• sintesi DNA novobiocina, chinolonici, metronidazolo
• sintesi RNA rifampicina
Parete
• sintesi peptiglicano
– sintesi dei precursori cicloserina
– passaggio trans-membrana bacitracina ristocetina
– assemblaggio –lattamici, vancomicina
• sintesi composti tipici dei micobatteri
– acidi micolici isoniazide
– arabinogalattano etanbutolo
Sintesi proteica
– subunità 30S aminoglicosidi, tetracicline
– subunità 50S macrolidi, cloramfenicolo
– fattori extraribosomiali acido fusidico
Membrana membrana esterna Gram neg
• disorganizzazione polimixine
38
I farmaci antibatterici farmaco-resistenza
Resistenza innata o intrinseca
•
•
caratteristica di un gruppo,
specie, genere
nota a priori
Meccanismi
• assenza del bersaglio
– lattamici, altri micoplasmi
• ostacolo alla entrata nella
cellula batterica
– aminoglicosidi O2-dipendente
anaerobi
– vancomicina gram-neg
• non attivazione nella cellula
batterica
– metronidazolo aerobi
Resistenza estrinseca o acquisita
•
cambiamento del genoma
•
pochi ceppi di un gruppo, specie,
genere selezione
non nota a priori sotto i nostri occhi
•
–
evoluzione
Meccanismi
• sul batterio
– modificazione del bersaglio
– impedimento al raggiungimento
del bersaglio
– aumento dell’efflusso
• sul farmaco
– modificazione enzimatica
– distruzione enzimatica
39
I farmaci antibatterici
Antibiogramma
• saggio in vitro per guidare la terapia antibatterica
• il ceppo isolato viene saggiato contro un pannello
di antibiotici
– verranno non impiegati quello/quei farmaci verso i quali
si ha resistenza
– per gli altri si sceglierà quello più adatto
•
•
•
•
sede di infezione e farmacocinetica
condizioni del soggetto
costo
tossicità
40
Antibiogramma - M. diffusione in piastra
Sensibile
Multiresistente
41
Adattabilità ad un nuovo ambiente
•
•
ambiente inanimato
ambiente animato
sedi diverse nell’ospite
Regolazione
• Sequenza DNA
– amplificazione del gene
– riarrangiamento del gene
espressione coordinata
dei fattori di virulenza e • Trascrizione
patogenicità
– attivatori
– repressori
• controllata da fattori
ambientali
• Post-trascrizione
–
temperatura, fonti
carbonio, osmolatrità,
conc Fe, nutrienti …
– modificazione covalente
– clivaggio proteolitico
– legame a proteine della
cellula ospite
42
Genoma batterico
informazione
replicazione sincrona con divisione cellulare
• Cromosoma unico e Unità genetiche accessorie
(plasmidi)
– assenza di istoni
– unità trascrizionali multicistroniche
– quasi tutta la sequenza per
• codificazione proteine
• regolazione trascrizione
• Aploidia
– espressione fenotipica immediata di un qualsiasi
cambiamento
– controllo
• attivazione/disattivazione promoters
43
Batteri Plasmidi
• DNA extracromosomico
• copie multiple
• informazione per
• fattori di virulenza & patogenicità
• antibiotico-resistenza….
• trasferibili
• coniugazione batterica
44
Adattabilità
variazioni fenotipiche
• tutta la popolazione si adatta
fisiologicamente al nuovo ambiente nell’ambito
del potenziale genomico
– cambia il fenotipo non il genotipo espressione
del gene/i
variazioni genotipiche
• la cellula mutata viene selezionata perché
meglio si adatta all’ambiente
– mutazione
– ricombinazione
• trasformazione, coniugazione, transduzione
elementi genetici di trasposizione
45







![5\) batteri [modalità compatibilità]](http://s1.studylibit.com/store/data/000928299_1-28a224c15810efb654d8d9e4b207aa31-300x300.png)



