Compiti di termodinamica 5
n = 0,2 moli di gas monoatomico ( cv =3/2 R; cp =5/2 R) . Trova le temperature nei quattro stati
A, B, C, D. Quante sono le temperature in gioco? Se fosse un ciclo di Carnot, quale rendimento
avrebbe? Da quali trasformazioni è costituito il ciclo? L’area racchiusa dal ciclo, che cosa
rappresenta?
Calcola il calore assorbito da A a B.
Da B a C : Q = L = nRT ln( Vc/Vb).
Da C a D : calcola il calore Q ceduto.
Da D ad A : Q = L = nRT ln( Va/Vd).
Calcola il rendimento di questo ciclo di Stirling.
(non c’è T , quindi U = 0 )
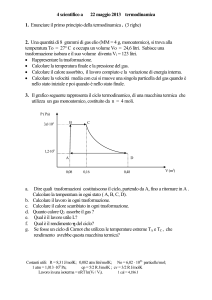
Ciclo di Stirling
P (atm)
B
7
6
A
C
2,33
2
D
3
9
V (litri)
Risultati: TA = 1098 K ; TB = 1280 K ; TC = 1280 K; TD = 1098 K
QAB = 454 J; QBC = 2337 J;
QCD = - 454 J; QDA = - 2005 J
L = Qass - | Qced | = 2791 – 2459 = 332 J; = 332 / 2791 = 0,12 = 12 %
di Carnot = ( TB – TA) / TB = 0,14 = 14%
Il rendimento di un ciclo di Carnot:
1. Dipende dalla quantità di sostanza che lo descrive
2. È uguale all’unità poiché tutte le trasformazioni che lo compongono sono ideali,
reversibili
3. È uguale per tutte le macchine di Carnot
4. È calcolabile allorché si conoscono le temperature delle due sorgenti.
Una macchina termica preleva una quantità di calore Q2 da una sorgente e cede
una quantità di calore Q1 ad un refrigerante. Se il rapporto Q2/Q1 =10/7, il
rendimento della macchina risulta:
1. 30 %
2. 70 %
3.
4.
1,42 %
non calcolabile
Scrivi sotto ciascun grafico il nome della trasformazione rappresentata.
P
P
P
P
V
T
V
V
2. Una quantità di 8 grammi di gas elio (MM = 4 g, monoatomico), si trova alla
temperatura To = 27° C e occupa un volume Vo = 24,6 litri. Subisce una
trasformazione isobara e il suo volume diventa V1 = 123 litri.
Rappresentare la trasformazione.
Calcolare la temperatura finale e la pressione del gas.
Calcolare il calore assorbito, il lavoro compiuto e la variazione di energia
interna.
3. Il grafico seguente rappresenta il ciclo termodinamico, di una macchina termica
che utilizza un gas monoatomico, costituito da n = 4 moli.
P ( Pa)
B
3,6∙105
1,2∙105
C
A
0,08
D
0,16
0,48
V (m3)
a. Dire quali trasformazioni costituiscono il ciclo, partendo da A, fino a ritornare
in A .
Calcolare la temperatura in ogni stato ( A, B, C, D).
b. Calcolare il lavoro in ogni trasformazione.
c. Calcolare il calore scambiato in ogni trasformazione.
d. Quanto calore Q2 assorbe il gas ?
e. Qual è il lavoro utile L?
f. Qual è il rendimento del ciclo?
g. Se fosse un ciclo di Carnot che utilizza le temperature estreme TA e TC , che
rendimento avrebbe questa macchina termica?
Costanti utili: R = 8,31 J/molK; 0,082 atm litri/molK;
No = 6,02 · 1023 particelle/mol;
5
1 atm = 1,013 ∙10 Pa;
cp = 5/2 R J/molK ; cv = 3/2 R J/molK
Lavoro in una isoterma = nRT ln(Vf / Vi).
1 cal = 4,186 J