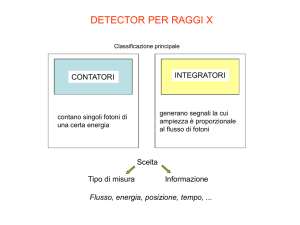
Lezione 11
Ionizzazione dei gas
Una particella carica (veloce) che attraversa un mezzo lascia una traccia di
ionizzazione lungo la sua traiettoria (Bethe-Block):
dE
2mc2 b 2g 2Tmax
d g
2 Z 1 1
2
Kz
ln
b
2
2
dx
A b 2
I
2
Se il mezzo è molto sottile ( in gr/cm2 ) i raggi d molto energetici possono
lasciare il mezzo per alcune applicazioni si usa la perdita di energia
ristretta.
2 2 2
dE
Z
1
1
2
mc
b g Tcut
d g
2
2
Kz
ln
b
2
2
dx
A b 2
I
2
dove Tcut non è piu’ la massima energia trasferibile, ma è quella energia per
cui il range dell’elettrone è > dello spessore del materiale.
Ricordiamo Tmax = 2mc2b2g2
Rivelatori di Particelle
1
Lezione 11
Ionizzazione dei gas
La particella incidente incontra gli atomi del gas e li ionizza. Gli scontri con gli atomi del gas
sono casuali e caratterizzati da un cammino libero medio l, dato dalla sezione d’urto di
ionizzazione sI e dalla densità N di elettroni.
l=1/(NsI)
Il numero di scontri in L ha una media L/l e la distribuzione in frequenza è una Poissoniana
(pochi scontri):
P(L/l,k) = ((L/l)k)/k! e-L/l
(*)
la distribuzione di probabilità f(l)dl dei cammini liberi medi è un esponenziale. Infatti la
probabilità di non trovare atomi nel tratto l per la probabilità di uno scontro in dl è :
1 ll
l
dl
f (l )dl P( ,0) P(
,1) e dl
l
l
l
La (*) fornisce anche la probabilità di avere 0 scontri in un percorso L
P( L ,0) e
l
L
l
Rivelatori di Particelle
2
Lezione 11
Ionizzazione dei gas
Nella tabella abbiamo una collezione di
misure eseguite con particelle veloci (è
indicato il g).
Se ho un contatore, sensibile nel tratto L,
capace di contare anche un solo elettrone,
posso misurare l, contando tutte le volte
che conto 0.
Naturalmente, per quanto perfetto sia tale
contatore, bisogna applicare una
correzione per gli elettroni sotto soglia.
gas
1cm/l # collisioni) g
H2
5.32±0.06
4.0
He
5.02±0.06
4.0
Ne
12.4±0.13
4.0
Ar
27.8±0.3
4.0
Xe
44
4.0
N2
19.3
4.9
O2
22.2±2.3
4.3
Aria
18.5±1.3
3.5
Rivelatori di Particelle
3
Lezione 11
Ionizzazione dei gas
Meccanismi di ionizzazione
Primaria uno o più elettroni sono strappati dall’atomo dalla particella
incidente. (e.g. pA pA+e-, pA++e-e-….)
Secondaria istantanea: gli elettroni sono strappati da atomi non colpiti
dalla particella incidente. Questa ionizzazione è essenzialmente dovuta ai
raggi d prodotti dalla ionizzazione primaria. ( il potenziale di ionizzazione medio
è ~10 – 20 eV mentre la massima energia trasferibile all’atomo è 2mc2b2g2 è facile
avere elettroni con energia cinetica dell’ordine dei KeV)
Secondaria ritardata : gli elettroni sono emessi da stati intermedi eccitati
A*. Se il gas A contiene un altro gas B con potenziale di ionizzazione
minore di quello di A posso avere pA pA* e A*B AB+e-.(effetto
Penning)
Rivelatori di Particelle
4
Lezione 11
Ionizzazione dei gas
I raggi d non troppo energetici (E<<Emax) sono emessi quasi ortogonali
alla direzione di volo della particella incidente (cos2q=E/Emax), ma… lo
scattering multiplo randomizza la direzione del moto dei raggi d, che
diventa completamente casuale dopo pochi mm.
Il range RT di un raggio d di energia E può essere calcolato integrando la
Bethe-Block sulla lunghezza di percorso RT e richiedendo che l’integrale
sia pari ad E. Ma…. scattering multiplo RT ???
si definisce un range empirico (ottenuto con misure di assorbimento)
Rp=0.71 E1.72
(E in MeV ed Rp in g cm-2)
che da una buona rappresentazione del range. (valida fino a ~ 100 KeV)
In argon un elettrone di 1 KeV si ferma in ~30 m, mentre uno di 10 KeV fa ~1.5
mm.
Rivelatori di Particelle
5
Lezione 11
Ionizzazione dei gas
Pittoricamente una particella carica che attraversa un gas produce una traccia
di ionizzazione:
Primary ionization
Total ionization ~ 3..4 n primaria
Il numero totale di coppie ioni-elettroni prodotti in Dx sarà:
DE
ntotale
wi
dove DE non è altro che la perdita di energia (Bethe-Block) nel tratto Dx e wi è
la perdita di energia media per coppia ione-elettrone.
Rivelatori di Particelle
6
Lezione 11
Ionizzazione dei gas
Rivelatori di Particelle
7
Lezione 11
Ionizzazione dei gas
KeV/cm
np
i.p/cm
nT
i.p/cm
1.47
2.44
29.4
94
24
1.32
4.60
22
192
12.1
22
1.23
6.76
44
307
13.7
13.7
33
1.62
3.01
34
91
16
15.2
13.1
28
2.21
1.48
16
53
58
10.6
10.8
23
1.86
4.50
46
195
Eex
Ei
I0
Wi
dE/dx
dE/dx
eV
eV
eV
eV
MeV/g cm-2
39.9
11.6
15.7
15.8
26
36
83.8
10.0
13.9
14.0
Xe
54
131.3
8.4
12.1
CO2
22
44
5.2
CH4
10
C4H10
34
Gas
Z
A
Ar
18
Kr
Dove:
Eex = energia minima di eccitazione;
Ei = energia minima di ionizzazione;
I0 =I/Z = potenziale efficace medio di ionizzazione per elettrone atomico;
Wi = perdita di energia media per produrre una coppia ione-elettrone;
dE/dx = perdita di energia per particelle al minimo (MIP);
np = numero di coppie primarie;
nT = numero totale di coppie.
Nel caso di composti e miscugli Z, A ed I sono valori medi.
Rivelatori di Particelle
8
Lezione 11
Ionizzazione dei gas
Commenti
Assumiamo un apparato spesso 1 cm e riempito di Argon
1 cm
n totale ~ 100 e-ion pair
nprimaria ~ 25 coppie
elettroni ioni primari fluttuano alla Poisson (poco), ma … sono solo ~25
contare il numero di cluster non e’ banale
n totale ~100 e code di Landau difficile misurare dE/dx con una sola misura
e strati sottili di gas e da questo dedurre (noto l’impulso) la massa della
particella
In ogni caso il rumore degli amplificatori è ~ 1000 e- (ENC)
bisogna aumentare il numero di coppie ioni-elettroni.
Rivelatori di Particelle
9
Lezione 11
Ionizzazione dei gas
Ricombinazione ed ioni negativi.
Siccome abbiamo poche coppie ione-elettrone è bene che non se ne perdano.
Ma….
1)
X+ + e- X + hn
ricombinazione ed emissione di 1g
2)
X- + Y+ XY + hn
ioni molecolari
In generale, la velocità di ricombinazione dipende dalla concentrazione degli
ioni positivi e negativi
dn=-bn-n+dt
dove b è una costante che dipende dal tipo di gas ed n+ e n- sono le
concentrazioni degli ioni negativi e positivi rispettivamente. Se n+=n-=n
n=n0/(1+bn0t)
integrato sul tempo t, essendo n0 la concentrazione al tempo t=0.
Rivelatori di Particelle
10
Lezione 11
Ionizzazione dei gas
Atomi elettronegativi.
Atomi elettronegativi possono catturare un e- formando degli ioni negativi.
Questi atomi hanno il livello più esterno quasi pieno per cui l’aggiunta di un erisulta in un rilascio di energia.
L’energia rilasciata è nota come affinità elettronica. La presenza di atomi
elettronegativi diminuisce l’efficienza di collezione ione-elettrone mangiandosi
gli elettroni prima che questi possano raggiungere gli elettrodi di rivelazione.
Gas elettonegativi : O2, H2O, CO2, SF6 ( filtri per H2O e O2).
Hanno invece affinità elettronica negativa He, Ne, Ar, Xe, Kr (gas nobili).
Rivelatori di Particelle
11
Lezione 11
Ionizzazione dei gas
Diffusione in assenza di campo elettrico.
Le cariche prodotte per ionizzazione perdono rapidamente la loro energia a causa di
collisioni multiple con le molecole del gas e raggiungono rapidamente l’energia termica:
e = (3/2)KT ~ 40 meV
la distribuzione delle energie termiche è:
F(e) = c(e)1/2 e-e/kt
(Maxwell)
A causa di collisioni multiple gli e ed ioni diffondono come segue:
x2
dN
1
e 4 Dt dx
N
4pDt
(Gauss)
dove dN/N è la frazione di carica in dx a distanza x dal punto di nascita e dopo un tempo t.
D è il coefficiente di diffusione. (D~vT<L> dove <L> è il cammino libero medio e vT la
velocità termica)
Rivelatori di Particelle
12
Lezione 11
Ionizzazione dei gas
s x (t ) 2Dt
Varianza nel volume
s V (t ) 6Dt
dN/N
Varianza lineare
sx
t=0.1 s
più stretta a
tempo <
t=0.3 s
x
t
Rivelatori di Particelle
13
Lezione 11
Ionizzazione dei gas
Ioni ed elettroni hanno masse molto diverse
velocità termica elettroni
vt ~ 10x106
cm/s
velocità termica ioni
vt ~ 104
cm/s
(La velocità termica si ricava immediatamente dalla e=3/2KT=½mv2)
In seguito ci interesseremo solo degli elettroni.
Rivelatori di Particelle
14
Lezione 11
Ionizzazione dei gas
Diffusione e deriva in presenza di campo elettrico.
3KT
si sommerà
m
una velocità dovuta al campo E. Infatti fra una collisione e l’altra gli elettroni
sono accelerati dal campo elettrico. Se <L> è il cammino libero medio e t il
tempo medio fra collisioni avremo ( dalla a=eE/m):
Se applico un campo elettrico alla velocità termica
vD ~ at ~
vt
eE L
m vt
Ma il cammino libero medio dipende dalla s di collisione
eE
vD ~
m
A
L
1
~ No
s
A
eEA
No s
vt
No s 3KT m
Rivelatori di Particelle
15
Lezione 11
Ionizzazione dei gas
La sezione d’urto di collisione dipende fortemente dall’energia termica e passa attraverso
minimi e massimi ( s Ramsauer ). Questi minimi e massimi sono dovuti ad effetti
d’interferenza quando la lunghezza d’onda dell’elettrone è ~ alle dimensioni della
molecola.
Ma la s è connessa al tempo t fra collisioni che dipende da E per certi valori del
campo posso avere una <vD> costante (importante per le camere a deriva).
Rivelatori di Particelle
16
Lezione 11
Ionizzazione dei gas
Mobilità.
La velocità di deriva è proporzionale ad E ed inversamente proporzionale alla
sezione d’urto di collisione ed alla velocità termica ci attendiamo quindi
che la velocità di deriva per campo elettrico unitario diviso per la densità sia
costante, cioè mobilità costante.
La mobilità m e’ definita come la <vD> per campo elettrico E/ ridotto.
vD
P
m
costante vD mE 0
P
E
P e’ la pressione e Po = 1 atmosfera
Rivelatori di Particelle
17
Lezione 11
Ionizzazione dei gas
In figura sono indicate alcune velocità di deriva per diversi campi elettrici e
diversi miscugli di gas.
Con 75% argon e 25% isobutano e campi di 800-1000 V/ cm si ha <vD>~ 50 mm/ms
Rivelatori di Particelle
18
Lezione 11
Ionizzazione dei gas
Abbiamo analizzato solo la diffusione, velocità di deriva e mobilità degli
elettroni.
Il comportamento degli ioni è simile, ma data la loro massa elevata, se
paragonata a quella degli elettroni, si muovono così lentamente che
poco ci interessa per qualunque applicazione pratica.
Rivelatori di Particelle
19
Lezione 11
Ionizzazione dei gas
Diffusione in presenza di campo elettrico E.
s x ~ 2Dt ~ 2vt L x
Abbiamo:
ma: vt ~
3KT
m
vD ~ at ~
vD
eE L
m vt
2 KT
2 KT
x
x
eV0
eE
sx
L’energia termica KT è in competizione con l’energia del campo elettrico eV0.
sx ~ 100 m con un campo elettrico di 1 KV/cm2 e una distanza di deriva di 1 cm.
limitazione intrinseca delle camere a deriva.
Rivelatori di Particelle
20
Lezione 11
Ionizzazione dei gas
Diffusione in presenza di E
Alto E piccola diffusione.
Conviene usare gas freddi (CO2) che hanno elettroni termici anche con alto E
(2KV/cm). diffusione D(E) isotropa e piccola. Ma.. bassa moltiplicazione
(male) e lungo tempo di deriva (bene).
Gas caldi (Argon) hanno elettroni non termici anche a bassi E diffusione
anisotropa.
Rivelatori di Particelle
21
Lezione 11
Ionizzazione dei gas
Moto in un campo elettrico e magnetico.
La velocità di deriva di un e in un gas è molto influenzata dalla
presenza di un campo magnetico B. Infatti:
mx eE ev B mAt
v
At m
indica la forza resistiva dovuta agli urti.
t
vD
m
ˆ wt Eˆ Bˆ w 2t 2 Eˆ Bˆ Bˆ
E
E
1 w 2t 2
Abbiamo assunto vD 0,m=et/m e w (frequenza di ciclotrone) = eB/m
( viene da mrw2=evB)
Rivelatori di Particelle
22
Lezione 11
Ionizzazione dei gas
In generale:
B0
vD
B0
vD
mE
ha 3 componenti
- // ad E
- // a B
- // a E B
Rivelatori di Particelle
23
Lezione 11
Ionizzazione dei gas
wt>>1 (alto B) gli elettroni
seguono B
wt<<1 (basso B) gli
elettroni seguono E
Rivelatori di Particelle
24
Lezione 11
Ionizzazione dei gas
In particolare:
caso :
EB
vd
y
aL:
vD || E
mE
1 w 2t 2
Lorentz angle
tan a L wt
vD
eB
w
m
aL
B
E
x
t tempo medio fra collisioni
tan a L vD
Esempio: E = 500 V/cm e <vD>=3.5 cm/ms se B=0
E = 500 V/cm e B = 1.5 T <vD>=2.4 cm/ms e aL=46o
Rivelatori di Particelle
B
E
25
Lezione 11
Ionizzazione dei gas
Special case:
Transverse diffusion s (mm) for a
drift of 15 cm in different
Ar/CH4 mixtures
E || B
(A. Clark et al.,
PEP-4 proposal, 1976)
The longitudinal diffusion (along
B-field) is unchanged.
In the transverse projection the
electrons are forced on circle
segments with the radius vT/w.
The transverse diffusion coefficient
appears reduced
D0
DT ( B)
1 w 2t 2
Very useful… see later !
Rivelatori di Particelle
26