Direzione Generale Sanità e Politiche Sociali
Commissione Regionale del Farmaco
(D.G.R. 1540/2006, 2129/2010 e 490/2011)
Documento PTR n. 223 relativo a:
RANIBIZUMAB:
diminuzione visiva causata dall’edema maculare
diabetico (DME);
diminuzione visiva causata dall’edema maculare
secondario ad occlusione venosa retinica (RVO di
branca o RVO centrale).
Giugno 2014
Assessorato Politiche per la salute – Commissione Regionale del Farmaco
RANIBIZUMAB
Indicazioni registrate
Ranibizumab è indicato negli adulti per:
- il trattamento della degenerazione maculare neovascolare (essudativa) correlata all’età (AMD);
- il trattamento della diminuzione visiva causata dall’edema maculare diabetico (DME);
- il trattamento della diminuzione visiva causata dall’edema maculare secondario ad occlusione venosa retinica (RVO
di branca o RVO centrale).
ATC S01BA04 - Sostanze per i disturbi vascolari dell’occhio-Sostanze antineovascolarizzazione
Regime di fornitura: OSP
Classe di rimborsabilità: H medicinale soggetto a prescrizione medica limitativa, utilizzabile esclusivamente in
ambiente ospedaliero o in struttura ad esso assimilabile). Scheda raccolta dati (Registro AIFA su piattaforma web)
Procedura registrazione: centralizzata
Prezzo
Somministrato mensilmente come una singola iniezione intravitreale da 0,5 mg (pari a 0,05 ml).
Prezzo ex factory IVA esclusa (al netto dello sconto obbligatorio alle strutture pubbliche -22% dal 16 dicembre 2013:
634,96 €
Trattamento di riferimento disponibile per le
patologie elencate
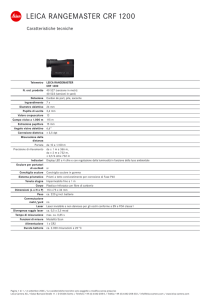
L'edema maculare diabetico (DME) è una
vasculopatia oculare che rappresenta una delle
principali complicanze del Diabete Mellito (DM),
è più frequente nel DM di tipo 2. Si stima che ne
sia affetta il 10% della popolazione diabetica ma
può colpire fino al 30% dei diabetici con una
durata di malattia di oltre 25 anni. L’alterata
permeabilità dei capillari retinici comporta un
ispessimento della macula dovuto all’accumulo di
fluidi con conseguente riduzione dell’acuità
visiva. La progressione naturale della malattia
può portare nel 50% dei casi alla perdita della
vista pari a 10 o più lettere in 2 anni.1
Per il DME, l’attuale standard di cura è
rappresentato dalla fotocoagulazione con laser
che in media stabilizza l’acuità visiva a 3 anni,
meno del 3% di occhi mostra un miglioramento, il
13% o più dei pazienti perde più di 15 lettere
dopo 3 anni dalla diagnosi.2
L'edema maculare rappresenta inoltre una delle
complicanze dell’occlusione venosa retinica
(RVO) ed il suo persistere nel tempo può
comportare la perdita irreversibile della vista.3
Nella metà circa dei pazienti con RVO l'edema si
risolve spontaneamente, con il recupero parziale
della vista nell'arco di 3-6 mesi. Allo stato attuale
non esistono terapie risolutive, capaci di
garantire un miglioramento rapido e consistente
della acuità visiva. I possibili fattori di rischio
devono essere individuati e corretti, mantenendo
uno stretto monitoraggio oculistico per eventuali
complicanze,
prima
fra
tutte
la
neovascolarizzazione.
Rispetto allo standard di cura della RVO, è
necessario distinguere tra occlusione retinica di
una branca della vena centrale della retina
(BRVO) ed occlusione della vena centrale della
retina (CRVO). Nella prima situazione, il laser
viene considerato lo standard di trattamento, in
grado di determinare una stabilizzazione e in
alcuni casi un lento miglioramento della vista nel
tempo; tuttavia una quota significativa di pazienti
non ne trae alcun beneficio.
La terapia con laser non ha mostrato invece alcun
beneficio nel trattamento del CRVO anche se può
essere usata sia nel BRVO che nel CRVO per
trattare i processi di neovascolarizzazione
secondaria4
Il desametasone impianto per uso intravitreale
rappresenta una opzione solo per il trattamento
dell’edema maculare secondario a RVO di branca
o centrale, mentre per il DME la Commissione
Tecnico Scientifica di AIFA ha espresso di recente
un parere favorevole al suo inserimento nella
2
Documento approvato nella seduta della CRF del 12 Giugno 2014
Assessorato Politiche per la salute – Commissione Regionale del Farmaco
lista L.648/96 in pazienti resistenti o intolleranti a
ranibizumab (verbale del 9-10 giugno 2014).
Infine, il triamcinolone presenta l’indicazione
registrata (Taioftal®), ma non è stato ancora
negoziato da AIFA e il bevacizumab intravitreale è
off-label per entrambe le indicazioni.
Meccanismo d’azione
Il DME ha un’origine multifattoriale legata
prevalentemente a:
- cambiamenti biochimici da iperglicemia con
conseguente aumento della permeabilità
vascolare a causa del rilascio da parte delle
cellule retiniche e dell’epitelio pigmentato di
messaggeri biochimici (VEGF, istamina ecc.);
- grave ipossia tissutale con conseguente
dilatazione arteriolare e movimento di fluidi
verso lo spazio extracellulare;
- cambiamenti biochimici del vitreo che ne
favoriscono l’adesione al polo posteriore con
conseguenti possibili trazioni sulla retina.
E’
stata
inoltre
dimostrata
un’elevata
concentrazione di VEGF nel vitreo dei diabetici.
L'occlusione della circolazione venosa della retina
è una patologia che causa la perdita visiva e di
conseguenza una riduzione della qualità della
vita. Solitamente l'occlusione si verifica nel punto
in cui una vena si incrocia con una arteria e
comporta l'interruzione del drenaggio del sangue
che giunge dalla rete capillare retinica. Di
conseguenza la pressione all'interno della rete
capillare aumenta provocando emorragie e
diffusione di liquido e materiale plasmatico nello
spessore della retina. La sede dell'occlusione
determina la distribuzione e l'estensione delle
emorragie. In alcuni casi l’entità dell’occlusione
venosa è tale da portare ad una chiusura più o
meno estesa del letto capillare con conseguente
ischemia della retina. Per questo motivo le
occlusioni venose della retina si distinguono in
due forme: ischemiche o edematose.
Il RVO è un evento acuto a seguito del quale si
verifica un calo della vista. Nelle forme
ischemiche le cellule ganglionari della macula
sono danneggiate in modo irreversibile e di
conseguenza saranno minori le possibilità di
miglioramento della funzione visiva. Nelle forme
edematose, che interessano il 60% dei pazienti
con BRVO e l’80% dei pazienti con CRVO,
l’andamento della funzione visiva è solitamente
più favorevole; in alcuni casi risulta compromessa
in modo meno rilevante e secondariamente si
può verificare un miglioramento spontaneo.
L’edema maculare che può conseguentemente
svilupparsi ha una durata circoscritta di brevemedio termine. I dati disponibili nella letteratura
sulla durata dell’edema maculare a seguito
dell’occlusione venosa retinica sono limitati, ma è
possibile attendersi che, nella maggioranza dei
casi, l’occhio affetto si stabilizzi entro 2 o 3 anni
dall’evento acuto.5,6
Il meccanismo patogenetico dell’edema maculare
nel RVO è complesso, e sembra comprendere una
componente
infiammatoria
mediata
da
prostaglandine, interleuchine e un danno
vascolare, mediato dal VEGF.
Il razionale per l’uso dei farmaci anti-VEGF nella
DME e nel RVO deriva dalle loro proprietà anti
VEGF. Ranibizumab (R) è un frammento di un
anticorpo monoclonale ricombinante umanizzato
diretto contro il fattore di crescita endoteliale
vascolare umano A (VEGF-A). Esso si lega con
un’elevata affinità alle isoforme del VEGF-A
prevenendo così il legame del VEGF-A ai suoi
recettori. Tale legame porta infatti ad una
proliferazione delle cellule endoteliali, ad una
neovascolarizzazione, e ad un aumento della
permeabilità vasale.7
Evidenze disponibili per il farmaco in oggetto e
loro trasferibilità
Edema maculare diabetico (DME)
Studi registrativi per EMA (a 12 mesi):
Sono due gli studi che EMA ha considerato al fine
dell’autorizzazione
dell’estensione
delle
indicazioni terapeutiche di R nel trattamento del
DME.
Il primo (Studio RESOLVE) è un RCT di fase II (151
pz) che ha confrontato R alle dosi di 0,3 mg o 0,6
mg (51 pz) e 0,5 mg o 10 mg (51 pz) con placebo
(iniezione sham, 49 pz).8 Lo studio inizialmente
ideato con un disegno flessibile per consentire di
definire meglio alcuni parametri per lo sviluppo
clinico del farmaco (dose, frequenza di
somministrazione ecc.) prevedeva un analisi ad
interim a 6 mesi (42 pz) i cui risultati hanno
permesso il proseguimento dello stesso studio in
cieco. A partire dal primo mese era concesso di
raddoppiare la dose del farmaco attivo in base ai
risultati
dell’OCT
(Optical
Coherence
Tomography); era inoltre possibile un
3
Documento approvato nella seduta della CRF del 12 Giugno 2014
Assessorato Politiche per la salute – Commissione Regionale del Farmaco
trattamento rescue con laser a partire dal terzo
mese in entrambi i bracci in caso di un
peggioramento di BCVA1 (>10 lettere) o se la
macula non raggiungeva uno spessore ≤225 μm.
R è stato somministrato 1 volta al mese per i
primi 3 mesi, poi al bisogno sulla base di VA2 e
OCT; il 70%-78% dei pazienti ha raddoppiato la
dose di R nel primo mese.
Il secondo (Studio RESTORE) è un RCT di fase III
su 345 pazienti che ha valutato R (0,5 mg) in
monoterapia (116 pz) o in associazione alla
fotocoagulazione laser (116 pz) vs iniezione sham
+ fotocoagulazione laser (111 pz).9 R veniva
somministrato ogni mese per i primi 3 mesi.
Successivamente, il trattamento con il farmaco
attivo o sham proseguiva mensilmente fino a
stabilizzazione della vista per 2 visite consecutive
oppure fino ad ottenere un guadagno ≥ 84 lettere
(≈20/20 scala Snellen). La terapia veniva ripresa
con iniezioni mensili quando si osservava una
riduzione BCVA dovuta a progressione del DME.
Le caratteristiche principali della popolazione
erano simili in entrambi gli studi e sono descritte
in dettaglio nella tabella delle evidenze in
allegato. E’ importante osservare che i pazienti
con diabete di tipo 1 erano poco rappresentati.
L’esito primario, di superiorità, era lo stesso per
entrambi gli studi:
- media delle variazioni medie nella BCVA vs
baseline valutata a partire dal primo mese
fino al 12° mese.
Tra gli esiti secondari (a 12 mesi) per i due studi
erano le percentuali di pazienti con:
vs basale in termini di guadagno o perdita
di 10 o 15 lettere.
1
; BCVA= best corrected visual activity [miglior visione
possibile raggiungibile con lenti correttive, misurata in
termini di linee di Snellen su un tabellone luminoso
(ottotipo)];
2
VA = visual activity
Risultati degli studi RESOLVE e RESTORE
Esito primario
A 12 mesi, R in monoterapia o in associazione a
laser ha mostrato di essere superiore al controllo
con differenze significative in termini di lettere
guadagnate, sia nello studio RESOLVE (+ 8,2
lettere con R 0,6 mg e + 4,8 lettere con R 10 mg),
che nello studio RESTORE (5,1 lettere con R in
monoterapia e 5,3 lettere con R associato a laser
terapia) (vedi in allegato tabella delle evidenze).
In quest’ultimo studio non si sono osservate
differenze significative fra l’uso di R in
monoterapia o in associazione a fotocoagulazione
con laser.
Tra gli esiti secondari:
- la percentuale di pazienti che hanno
ottenuto un recupero > 15 lettere variava dal
32,5% al 40,5% (studio RESOLVE); dal 37,4%
fino al 43,2% nel braccio dove R era stato
associato a laser terapia (studio RESTORE);
- la percentuale di pazienti che hanno
ottenuto un recupero > 10 lettere variava dal
52,5% al 73% (studio RESOLVE); dal 22,6% e
22,92% nel braccio dove R era stato
associato a laser terapia (studio RESTORE);
L’analisi ad interim dell’estensione a due anni
dello studio RESTORE ha confermato di efficacia
(obiettivo secondario) emersi dallo studio a 12
mesi.10
Studi di supporto (a 12 mesi)
Un’ulteriore RCT di fase III (DRCR.net) su 691 pz,
ha valutato R (0,5 mg) in associazione a laser vs
triamcinolone (1 mg o 4 mg) per via intravitreale
+ laser o laser da solo in termini di recupero
dell’acuità visiva a 12 mesi (esito primario).11
Risultati
Il braccio trattato con R + laser ha ottenuto un
guadagno di lettere (pari a 9) superiore a quello
trattato con triamcinolone + laser (4 lettere) o
con solo laser (3 lettere). L’aggiunta di
triamcinolone al laser non ha determinato
vantaggi aggiuntivi rispetto al solo laser (diff. non
significativa), ma una più rapida insorgenza di
beneficio.
Il 57% dei pz è stato seguito per 2 anni con esiti in
linea con quelli del primo anno (guadagno di circa
9 lettere).
4
Documento approvato nella seduta della CRF del 12 Giugno 2014
Assessorato Politiche per la salute – Commissione Regionale del Farmaco
Studi registrativi per FDA (a 24 mesi + loro
estensione)
Nei due RCT multicentrici, di disegno
sovrapponibile, RISE (377 pz) e RIDE (382 pz), R
(0,5mg o 0,3 mg) è stato confrontato con placebo
(iniezione sham) in pazienti con DME per
valutarne l’ efficacia in termini di percentuale di
pazienti con un guadagno > 15 lettere (esito
primario) a 1 anno. La fotocoagulazione con laser
era consentita dal terzo mese. Dopo i primi 24
mesi i pazienti in trattamento con placebo (sham)
passavano al trattamento attivo (R 0,5 mg) e
venivano seguiti per ulteriori 12 mesi.12
Risultati
A 24 mesi, la percentuale di pz che ha raggiunto
l’endpoint primario (guadagno > 15 lettere) è
stata significativamente maggiore nel braccio
trattato co R (34% con R 0,3 mg e 46% con R 0,5
mg) rispetto ai non trattati (12%-18%). Tali
risultati sono stati confermati nel periodo di
estensione di ulteriori 12 mesi dello studio (36
mesi totali).13 I pz trattati con R solo nel terzo
anno hanno ottenuto un recupero del visus
inferiore rispetto ai pz che hanno iniziato il
trattamento al basale.
Edema maculare secondario ad occlusione
venosa retinica (RVO di branca o RVO centrale)
Studi registrativi (6 mesi)
Gli studi registrativi che hanno valutato l’efficacia
e la sicurezza di R in pazienti con RVO sono due:
lo studio BRAVO (395 pz) in pazienti con RVO di
branca e lo studio CRUISE (345 pz) in pazienti con
RVO centrale.14,15 Si tratta di due RCT in doppio
cieco di disegno sovrapponibile che hanno
confrontato R (0,3 mg o 0,5 mg 1 volta al mese)
con placebo (iniezione sham) per 6 mesi; a partire
dal terzo mese solo nello studio BRAVO era
concesso un trattamento rescue con laser. Il
trattamento con farmaco attivo o controllo era
preceduto da 28 giorni di osservazione per
escludere i pazienti che ottenevano un
miglioramento spontaneo del visus (guadagno
≥10 lettere). La maggioranza dei pazienti
presentava un RVO non ischemica mentre erano
esclusi pazienti con evidenze di retinopatia
diabetica.
L’esito primario per entrambi gli studi era la
media delle variazioni medie nella BCVA (lettere)
a partire dal primo fino al sesto mese.
Tra i principali esiti secondari erano:
% pz con guadagno > 15 lettere ( rispetto al
basale), riduzione CFT3, % pz BCVA ≥20/40.
Risultati
Per quanto riguarda l’esito primario, a 6 mesi, R
ha mostrato di essere superiore al controllo con
differenze statisticamente significative in termini
di lettere guadagnate, sia nello studio BRAVO
(+9,4 lettere con R 0,3 mg e + 10,6 lettere con R
0,5 mg), che nello studio CRUISE (11,5 lettere con
R 0,3 mg e 13,8 lettere con R 0,5 mg) (vedi in
allegato tabella delle evidenze). Nello Studio
BRAVO sono ricorsi al laser il 54,5% dei pz nel
gruppo sham, il 18,7% e il 19,8% rispettivamente
di quelli trattati con 0,3 mg e 0,5 mg di R.
Anche per gli esiti secondari R ha mostrato
differenze statisticamente significative rispetto al
gruppo sham. In particolare i pz trattati con R che
hanno ottenuto un BCVA ≥20/404 variavano dal
67,9% al 64,9% vs 41,7 (gruppo sham) per lo
studio BRAVO e dal 43,9% al 46,9% vs 20,8%
(gruppo sham) per lo studio CRUISE,
rispettivamente per le dosi di 0,3 mg e 0,5 mg.
Dal 6° e fino al 12° mese tutti i pazienti (braccio
con farmaco attivo e braccio sham) venivano
rivalutati mensilmente e ritrattati con R al
bisogno in base ai valori rilevati di acuità visiva
(BCVA) e spessore della macula (CMT)516,17
Per entrambi gli studi, l’analisi dei dati a 12 mesi
conferma che con somministrazioni di R al
bisogno i guadagni di lettere ottenuti nei primi 6
mesi vengono mantenuti (vedi Fig. 1 e Fig. 2).
Inoltre, i pazienti del gruppo sham mostrano un
miglioramento spontaneo della patologia a 6
mesi e un guadagno di lettere a 12 mesi inferiore
rispetto a coloro che hanno ricevuto il R dal
tempo 0 (Figura 1).
3
CFT = spessore foveale centrale (misurato tramite OCT)
Valore considerato soddisfacente per leggere e guidare
5
BCVA ≤ 20/40 o CMT ≥250 µm. Il gruppo sham ha iniziato il
trattamento con R 0,5mg.
5
4
Documento approvato nella seduta della CRF del 12 Giugno 2014
Assessorato Politiche per la salute – Commissione Regionale del Farmaco
Fig. 1-Studio BRAVO
Fig. 2-Studio CRUISE
dall’inizio del trattamento); il miglioramento
medio della BCVA era di 25,9 lettere vs 17,1
lettere in quelli con edema non risolto; in
entrambi i gruppi, l’80% dei pz raggiunge una
BCVA ≥ 20/40 o migliore alla visita finale.
Il restante 50%, che non ha avuto risoluzione
dell’edema, riceve 3 somministrazioni di R
nell’ultimo anno di follow-up.
Il 44% dei pazienti con CRVO (n=32) ha ottenuto
una risoluzione dell’edema; di questi il 71% ha
ricevuto l’ultima iniezione entro 2 anni.
Il 56% dei pz con CRVO non ha una risoluzione
dell’edema e riceve 6 somm. di R nell’ultimo anno
di follow-up. Rispetto ai pz con edema non
risolto, i pz con edema risolto hanno un maggiore
miglioramento della BCVA (25,2 vs 4,3 lettere) ed
una % maggiore ha una BCVA finale ≥ 20/40
(64,3% vs 27,8%).
6
Studi di supporto a lungo termine:
Lo studio HORIZON (608 pz) ha un disegno in
aperto non controllato e ha seguito per ulteriori
12 mesi la coorte di pazienti (circa l’85%) che ha
completato gli RCT BRAVO (304 pz) e CRUISE (304
pz).18 I pazienti sono stati valutati rispetto alla
comparsa di ADR oculari o non (esito primario di
sicurezza) e ad alcuni parametri di efficacia (esiti
secondari) tra cui anche la variazione media dal
baseline del BCVA.
Risultati
La frequenza di ADR gravi è risultata del 2-9% per
le ADR oculari e dell’1-6% per quelle
potenzialmente correlate al meccanismo d’azione
(anti-VEGF).
Infine lo studio RETAIN con disegno in aperto,
singolo braccio ha seguito per 5 anni 66 pz che
avevano terminato l’HORIZON [BRAVO (n=34) e
CRUISE (n=32)]19
Risultati
Il 50% dei pazienti con BRVO (n=34) ha ottenuto
una risoluzione dell’edema7 (i 2/3 entro 2 anni
6
La scala utilizzata prevede 3 livelli decrescenti di evidenze (A, B, C).
Definita come assenza del fluido intraretinico per almeno 6 mesi
senza tratt. con R.
7
Va considerato, comunque, che la numerosità
campionaria dei gruppi trattati era esigua (poco
più di una sessantina di pazienti).
Linee Guida e Revisioni sistematiche (DME)
Le recenti linee guida nazionali inglesi del Royal
College of Opthalmologists (2012)20 considerano
gli anti-VEGF il nuovo gold standard in presenza
di edema maculare centrale e visione ridotta
(forza della raccomandazione A).
Le linee guida della società spagnola di
oftalmologia del 200921 mettono al primo posto il
laser,
ritenendo
l’uso
dei
farmaci
antiangiogenetici non conclusivo.
Secondo l’NHS inglese (2010)22, sia ranibizumab
che bevacizumab dispongono di evidenze a
supporto del loro impiego nel DME, sebbene di
qualità diversa (bassa per bevacizumab, più
elevata per ranibizumab in quanto dispone di
studi finalizzati alla sua registrazione.
Una revisione sistematica Cochrane23 ha valutato
l’efficacia e la sicurezza dei farmaci anti-VEGF
(bevacizumab, ranibizumab, aflibercept) nel
preservare o migliorare l’acuità visiva (>3 lettere)
a 1 anno in pazienti con DME. Sono stati inclusi
tutti gli RCT che hanno confrontato un farmaco
ani-VEGF con qualsiasi trattamento, trattamento
sham o nessun trattamento
6
Documento approvato nella seduta della CRF del 12 Giugno 2014
Assessorato Politiche per la salute – Commissione Regionale del Farmaco
I pochi studi disponibili impediscono di fare
confronti indiretti e individuare eventuali
differenze di efficacia tra gli anti-VEGF. I risultati
vanno comunque tutti nella stessa direzione.
Costo della terapia
In termini di beneficio assoluto ogni 100 pazienti
trattati con la fotocoagulazioni o in alternativa un
anti-VEGF 8 vs 26 pazienti rispettivamente
possono guadagnare 3 o più lettere in un anno.
Al prezzo in vigore al dicembre 2013 il costo di un
ciclo minimo di trattamento è il seguente:
- Ranibizumab (1 somministrazione al
mese per 3 mesi per entrambe le
indicazioni) è di 1904,88 €.9
- desametasone impianto intravitreale10 a
lungo rilascio (trattamento di RVO) si può
ragionevolmente ipotizzare di € 869,94 +
IVA.
I dati di sicurezza relativi ai farmaci anti-VEGF
appaiono rassicuranti, ma la breve durata degli
RCT rispetto al decorso clinico, i pochi pz.
arruolati e la loro selezione non consentono di
ottenere informazioni conclusive .
(elaborato con riferimento al prezzo ex
factory indicato nella Determinazione AIFA o, in mancanza, al prezzo
pubblicato su Farmadati. Tale costo può essere soggetto a riduzioni
a seguito dell’espletamento della gara di acquisto)
Linee Guida (RVO)
Le linee guida nazionali inglesi del Royal College
of Opthalmologists (2010)24 attribuiscono un
livello di evidenza A8 all’uso del R, della
formulazione sterile priva di conservanti di
triamcinolone
acetonide
e
dell’impianto
intravitreale di desametasone nel trattamento
dell’edema maculare da RVO. Il bevacizumab
viene collocato al livello di evidenza D nell’edema
secondario a CRVO per le modalità di dosaggio
giudicate poco chiare e la mancanza di dati a
lungo termine, e in C nell’edema maculare
secondario a BRVO per la necessità di dati di
efficacia e sicurezza a lungo termine. Infine, viene
attribuito livello di evidenza C al pegaptanib per
la non disponibilità di esiti a lungo termine.
Le linee guida della società spagnola25 di
oftalmologia
(2010)
raccomandano,
nel
trattamento sia di CRVO che di BRVO, l’uso di
ranibizumab,
desametasone
impianto
intravitreale (per entrambi livello di evidenza 1,
forza di racc. A), corticosteroidi intravitreali
(livello di evidenza 4, forza di racc. D) e
bevacizumab (livello di evidenza 3, forza di racc. C
per l’assenza di dati di efficacia e sicurezza a
lungo termine). Non viene preso in
considerazione il pegaptanib.
9
8
La scala utilizzata prevede 4 livelli decrescenti di evidenze (A, B, C,
D).
Calcolato sul prezzo ex factory IVA esclusa (al netto
dello sconto obbligatorio alle strutture pubbliche -22%
dal 16 dicembre 2013 ).
10
Al netto degli sconti e delle riduzioni di legge.
7
Documento approvato nella seduta della CRF del 12 Giugno 2014
Assessorato Politiche per la salute – Commissione Regionale del Farmaco
CONCLUSIONI
In pazienti con DME, ranibizumab (da solo o associato alla fotocoagulazione laser) somministrato una
volta al mese per 3 mesi e successivamente al bisogno, al follow-up di 12 mesi, ha mostrato di essere
superiore al controllo (sham o sham +fotocoagulazione laser) con differenze statisticamente significative
in termini di lettere guadagnate (esito primario comune agli studi RESOLVE e RESTORE).
In pazienti con RVO, ranibizumab somministrato una volta al mese per 6 mesi si è dimostrato più
efficace del placebo in termini di lettere guadagnate [> 15 lettere; studio BRAVO (pz con RVO di branca)
e CRUISE (pz con RVO centrale)]. Tale risultato è confermato dall’analisi a 12 mesi.
Rispetto ai risultati degli studi esaminati si possono esprimere le seguenti considerazioni.
Studi in DME:
la fotocoagulazione con laser in media stabilizza l’acuità visiva a 3 anni, ma una parte di pz. non
risponde o non ottiene un beneficio soddisfacente;
la breve durata degli studi (12-24 mesi) non permette di trarre conclusioni sui reali benefici
determinati da ranibizumab rispetto allo standard di cura con laser;
gli studi non hanno permesso di definire le caratteristiche dei pz. che potrebbero trarre maggior
beneficio dal trattamento anche se complessivamente un maggior numero di pazienti trattati con
ranibizumab ottiene un guadagno ≥ 15 lettere (e ciò influenza la capacità di guidare e leggere)
rispetto al placebo.
Studi in RVO:
gli studi non hanno permesso di individuare elementi (es. OCT, fluoroangiografia), predittivi
dell’esito del trattamento con ranibizumab;
il momento più idoneo per l’inizio della terapia con ranibizumab non è stato chiaramente definito
dagli studi a causa del fatto che l’intervallo di tempo in cui si può osservare un miglioramento
spontaneo della sintomatologia è mediamente più lungo rispetto a quello considerato negli studi
(28 gg);
non sono noti gli effetti sull’acuità visiva nel lungo termine della maggior permanenza dell’edema.
La CRF, pur con i limiti emersi dall’analisi degli studi disponibili e sopra esposti, esprime un parere
favorevole all’inserimento di ranibizumab in PTR per le due nuove indicazioni terapeutiche (DME e RVO)
e si propone di rivalutarne la posizione quando saranno disponibili le medesime indicazioni per altri antiVEGF, al fine di definire più chiaramente il posto in terapia.
Per quanto riguarda l’indicazione di ranibizumab nell’edema maculare secondario a RVO, non essendo
disponibili studi di confronto diretto con desametasone impianto intravitreale, la scelta dovrà essere
effettuata dal clinico, sulla base delle caratteristiche individuali dei pazienti considerando, a parità di
indicazione, il costo del trattamento.
Per quanto riguarda il DME solo ranibizumab presenta l’indicazione registrata, il ricorso a desametasone
intravitreale potrà essere considerato in caso di pz. resistenti o intolleranti a ranibizumab ricorrendo alla
L. 648/96 (in attesa di pubblicazione in G.U.).
I dati relativi ai pazienti eleggibili dovranno essere inseriti sull’applicativo web AIFA, così come i dati di
follow up e di rivalutazione.
8
Documento approvato nella seduta della CRF del 12 Giugno 2014
Assessorato Politiche per la salute – Commissione Regionale del Farmaco
BIBLIOGRAFIA (aggiornata a gennaio 2014)
1. Lucentis
Assessment
report.
No.:
EMEA/H/C/000715/II/0020
October
http://www.ema.europa.eu/docs/en_GB/document_library/EPAR_-_Assessment_Report__Variation/human/000715/WC500101009.pdf [accesso: gennaio 2014].
2010.
2. ETDRS Reports No 1, 1985; No 2, 1987 and No 9, 1991.
3. Occlusion veineouse rétinienne. Rev Prescr 2011; 31:289-90.
4. Lucentis
Assessment
report.
No.:
EMEA/H/C/000715/II/0022
http://www.ema.europa.eu/docs/en_GB/document_library/EPAR_-_Assessment_Report__Variation/human/000715/WC500107807.pdf [accesso: gennaio 2014].
March
2011.
5. Rogers SL et al. Natural history of branch retinal vein occlusion: an evidence-based systematic review.
Ophthalmology 2010; 117:1094-1101.e5.
6. McIntosh RL et al. Natural history of central retinal vein occlusion: an evidence-based systematic review.
Ophthalmology. 2010 Jun;117(6):1113-1123.e15.
7. Lucentis® Riassunto delle Caratteristiche del Prodotto. Fonte: FarmaDati [accesso: gennaio 2014].
8. Massin P, Bandello F, Garweg JG, Hansen LL, Harding SP, Larsen M, Mitchell P, Sharp D, Schnurrbusch W,
Gekkieva M, Weichselberger A, Wolf S. Safety and Efficacy of R in Diabetic Macular Edema (RESOLVE Study).
Diabetes Care 2010; 33:2399–2405.
9. Mitchell P, Bandello F, Schmidt-Erfurth U, Lang GE, Massin P, Schlingemann RO, Sutter F, Simader C, Burian G,
Gerstner O, Weichselberger A. The RESTORE Study R Monotherapy or Combined with Laser versus Laser
Monotherapy for Diabetic Macular Edema. Ophthalmology 2011;118(4):615-625.
10. Lang GE, Berta A, Eldem BM, Simader C, Sharp D, Holz FG, Sutter F, Gerstner O, Mitchell P. Two-Year Safety and
Efficacy of R 0.5 mg in Diabetic Macular Edema Interim Analysis of the RESTORE Extension Study.
Ophthalmology 2013;120:2004-2012.
11. The Diabetic Retinopathy Clinical Research Network, Elman MJ, Aiello LP, Beck RW, Bressler NM, Bressler SB,.
Edwards AR, Ferris FL, Friedman SM, Glassman AR, Miller KM, Scott IU, Stockdale CR, Sun JK. Randomized Trial
Evaluating R Plus Prompt or Deferred Laser or Triamcinolone Plus Prompt Laser for Diabetic Macular
EdemaOphthalmology. 2010 June ; 117(6): 1064–1077.
12. Nguyen QD, Brown DM, Marcus DM, Boyer DS, Patel S, Feiner L, Gibson A, Sy J, Rundle AC, Hopkins JJ, Rubio RG,
Ehrlich JS. Research Group*R for Diabetic Macular Edema Results from 2 Phase III Randomized Trials: RISE and
RIDE. Ophthalmology 2012;119:789–801
13. Brown DM, Nguyen QD, Marcus DM, Boyer DS, Patel S, Feiner L, Schlottmann PG, Rundle AC, Zhang J, Rubio RG,
Adamis AP, Ehrlich JS, Hopkins JJ. Long-term Outcomes of R Therapy for Diabetic Macular Edema: The 36-Month
Results from Two Phase III Trials RISE and RIDE. Ophthalmology 2013;120:2013-2022.
14. Campochiaro PA, Heier JS, Feiner L, Gray S, Saroj N, Rundle AC, Murahashi WY, Rubio RG. R for Macular Edema
following Branch Retinal Vein Occlusion Six-Month Primary End Point Results of a Phase III Study. Ophthalmology
2010;117:1102–1112.
15. Brown DM, Campochiaro PA, Singh RP, Li Z, Gray S, Saroj N, Rundle AC, Rubio RG, Murahashi WY. R for Macular
Edema following Central Retinal Vein Occlusion Six-Month Primary End Point Results of a Phase III Study.
Ophthalmology 2010;117:1124–1133.
16. Brown DM, Campochiaro PA, Bhisitkul RB, Ho AC, Gray S, Saroj N, Adamis AP, Rubio RG, Murahashi WY.
Sustained Benefits from R for Macular Edema Following Branch Retinal Vein Occlusion: 12-Month Outcomes of a
Phase III Study. Ophthalmology 2011;118:1594–1602.
17. Campochiaro PA, Brown DM, Awh CC, Lee SY, Gray S, Saroj N, Murahashi WY, Rubio RG. Sustained Benefits from
R for Macular Edema following Central Retinal Vein Occlusion: Twelve-Month Outcomes of a Phase III Study.
Ophthalmology 2011;118:2041–2049.
18. Heier JS, Campochiaro PA, Yau L, Li Z, Saroj N, Rubio RG, Lai P. R for Macular Edema Due to Retinal Vein
Occlusions Long-term Follow-up in the HORIZON Trial. Ophthalmology 2012;119:802–809.
9
Documento approvato nella seduta della CRF del 12 Giugno 2014
Assessorato Politiche per la salute – Commissione Regionale del Farmaco
19. Campochiaro PA, Raafay S, Pearlman J, Brown DM, Boyer DS, Heier JS, Marcus DM, MD, Feiner L, Patel A, for the
RETAIN Study Group. Long-term Outcomes in Patients with Retinal Vein Occlusion Treated with Ranibizumab.
Ophthalmology 2014;121:209-219.
20. Diabetic Retinopathy Guidelines. The Royal College
http://www.rcophth.ac.uk/page.asp?section=451&sectionTitle
of
Ophthalmologists.
December
2012.
21. Pareja-Ríos A, Serrano-García M et al. Guías De Práctica Clínica De La Serv: Manejo De Las Complicaciones
Oculares De La Diabetes. Retinopatía Diabética Y Edema Macular. Arch Soc Esp Oftalmol 2009; 84: 429-450
22. Gabriel Coscas et al. Anti-vascular endothelial growth factor therapies (bevacizumab and ranibizumab) for
diabetic macular oedema. North East Treatment Advisory Group. October 2010.
23. Virgili G, Parravano M, Menchini F, Brunetti M. Antiangiogenic therapy with anti-vascular endothelial growth
factor modalities for diabetic macular oedema Cochrane Database of Systematic Reviews 2012, Issue 12. Art.
No.: CD007419. DOI: 10.1002/14651858.CD007419.pub3.
24. Interim Guidelines for Management of Retinal Vein Occlusion. The Royal College of Ophthalmologists. December
2010. http://www.rcophth.ac.uk/page.asp?section=451&sectionTitle=
25. Gómez-Ulla F et al. Guías de práctica clínica de la SERV: manejo de las oclusiones venosas de la retina. Arch Soc
Esp Oftalmol 2010; 85:294–309.
10
Documento approvato nella seduta della CRF del 12 Giugno 2014
Assessorato Politiche per la salute – Commissione Regionale del Farmaco
Allegato 1. Evidenze disponibili
Edema maculare diabetico (DME)
Edema maculare secondario ad occlusione
venosa retinica (RVO di branca o RVO centrale)
Studi registrativi per EMA (12 mesi):
Studi registrativi (6 mesi):
1. RESOLVE (151 pz)
1. BRAVO (395 pz)
2. RESTORE (345 pz)
2. CRUISE (345 pz)
Studi di supporto(12 mesi):
Studi di supporto(12 mesi):
3. DRCR.net (691 pz) vs triamcinolone
3. HORIZON (608 pz)
Studi registrativi per FDA (a 24 mesi + loro
estensione ad altri 12 mesi):
Studi di estensione:
4. RISE (377 pz)
5. RIDE (382 pz)
4. BRAVO (estensione a 12 mesi)
5. CRUISE (estensione a 12 mesi)
6. RETAIN (66 pz estensione a 49 mesi)
Ricerca bibliografica aggiornata al 10 gennaio 2014
11
Documento approvato nella seduta della CRF del 12 Giugno 2014
Assessorato Politiche per la salute – Commissione Regionale del Farmaco
Tabelle delle evidenze
Principali studi nell’Edema Maculare Diabetico (DME)
RESOLVE, Fase II, n=151
RESTORE, Fase III, n=345
P
Inclusione: pz con DME ≤ 9 mesi , DM tipo II
(97%), HbA1c ≤ 12%, CRT ≥ 300 µm, BCVA score
tra 73 e 39 lettere, storia di ictus
Esclusione: pz con ischemia retinica significativa e
retinopatia diabetica proliferativa.
Inclusione: pz con DME (1,8 aa circa), DM tipo I o
tipo II (circa 87%); HbA1c ≤ 10%, ischemia retinica
centrale (n=68), BCVA score tra 78 e 39 lettere.
Esclusione: pz con storia di ictus.
I
R 0,3 o 0,6 mg (n=51)*
R 0,5 o 0,10 mg (n=51)
+
Rescue laser consentita dal mese 3
C
O
T
R 0,5 mg+ fotocoagul. laser (n=118)
R 0,5 mg + sham laser (n=116)
Iniezione Sham (n=49)
+
Rescue laser consentita dal mese 3
♦
♦
Iniezione sham + fotocoagul. laser (n=111)
Primario: media delle variazioni medie nella BCVA dal mese 1 al mese 12 (misurazione mensile).
Secondari: vs basale in termini di guadagno o perdita di 10 o 15 lettere, CRT, perfusione retinica
(esploratorio), acuità visiva > 73 lettere.
12 mesi
CRT = central retinal thickness; BCVA = best corrected visual
activity [miglior visione possibile raggiungibile con lenti
correttive, misurata in termini di linee di Snellen su un
tabellone luminoso (ottotipo)]; VA = visual activity;
DME=edema maculare diabetico.
• Raddoppio dose effettuato sulla base dei risultati
dell’OCT (Optical Coherence Tomography); R 1/mese per
3 mesi, poi al bisogno sulla base di VA e OCT.
♦
R 1/mese per i primi 3 mesi. Trascorsi i primi 3
mesi, il tratt. Con R o sham proseguiva
mensilmente fino a quando la vista rimaneva
stabile per 2 visite consecutive oppure otteneva
un guadagno ≥ 84 lettere (≈20/20 scala Snellen).
Il tratt. veniva ripreso con iniezioni mensili
quando veniva osservata riduzione BCVA dovuta
a progressione del DME.
12
Documento approvato nella seduta della CRF del 12 Giugno 2014
Assessorato Politiche per la salute – Commissione Regionale del Farmaco
Risultati: esito primario e secondari
RESOLVE (gruppo B 109 pz)
RESTORE (345 pz)
R 0,6 mg
n=37
R 0,10 mg
n=40
Iniezione
sham
n=32
R 0,5 mg +
laser
n=118
R 0,5 mg +
Iniezione
sham laser sham + laser
n=111
n=115
9,4
6,0
1,2
5,9
6,1
8,2
[4,7 - 11,6]
4,8
[0,4 - 9,2]
5,1
[2,8 - 7,0]
5,3
[3,5 -7,3]
Guadagno ≥ 15 lettere
40,5
32,5
9,4
43,2
37,4
15,5
Guadagno ≥ 10 lettere
73,0
52,5
18,8
22,9
22,6
8,2
12
53
44,9
23,6
Primario (in lettere)
Media delle medie nella
BCVA dal mese 1 al mese
12 vs baseline
∆ verso sham
[IC95%]
0,8
Secondari (%pz)
Acuità visiva > 73 lettere
49
BCVA = best corrected visual activity
13
Documento approvato nella seduta della CRF del 12 Giugno 2014
Assessorato Politiche per la salute – Commissione Regionale del Farmaco
DRCR.net, Fase III, n=691 (854 occhi)
P
Inclusione: pz con DME e DM tipo I e II, VA tra 78 e 24 (20/32-20/320), CRT≥250 µm.
Esclusione: trattamento per DME nei 4 mesi precedenti o necessità di fotocoag. panretinica nei
successivi 6 mesi, storia di glaucoma o ipertensione oculare, patologie CV.
I
R 0,5 mg + laser ♦
C
Triamcinolone 1 mg o 4 mg + laser (prompt)
Iniezione sham + laser (prompt)
O
Primario: guadagno medio nella VA
Secondario: CRT
12 mesi
T
CRT= spessore retinico centrale;
♦ deferred per 24 sett. o prompt
■
CMT= spessore maculare centrale
Se entrambi gli occhi erano eleggibili, entrava nello studio
quello con CMT maggiore.
*laser effettuato al basale e successivamente ogni 3 mesi se CMT ≥250 µm.
14
Documento approvato nella seduta della CRF del 12 Giugno 2014
Assessorato Politiche per la salute – Commissione Regionale del Farmaco
RISE Fase III
n=377
P
RIDE Fase III
n=382
Inclusione: pz con DME, BCVA 20/40 (scala Snellen), CRT ≥ 275 µm, no laser nei 3 mesi
precedenti. Il 25% dei pz arruolati ha una retinopatia diabetica.
Esclusione: pz con ipertensione non controllata, HbA1c > 12%, recente accidente
celebrovascolare, IMA.
I
R 0,5 mg
R 0,3 mg
C
Iniezione sham
O
Primario: guadagno ≥ 15 lettere
T
0-24 mesi
Estensione a 36 mesi: il gruppo sham riceve R 0,5 mg
Fotocoag. laser consentita dal terzo mese.
Analisi di efficacia sulla popolazione ITT (LOCF)
Risultati degli studi RISE e RIDE:
A 24 mesi, una maggior percentuale di pz trattati con R raggiunge l’endpoint primario (34%
con 0,3 mg e 46% con 0,5 mg) rispetto ai non trattati (12%-18%)
I risultati si confermano a 36 mesi
I pz trattati solo nell’ultimo anno con R ottengono guadagno inferiore rispetto ai pz che
hanno iniziato il trattamento al basale (confronto indiretto)
Profilo di sicurezza in linea con quello noto da studi precedenti (eccezione: > numero di
decessi ed eventi CV, fatali e non, con R)
Mancato confronto verso terapia standard (laser)
15
Documento approvato nella seduta della CRF del 12 Giugno 2014
Assessorato Politiche per la salute – Commissione Regionale del Farmaco
Confronto anti-VEGF sul miglioramento dell’acuità visiva (≥3 lettere) a un anno
Figure 2. Forest plot of comparison: 2 Anti VEGF versus Laser, outcome: 2.2 Gain 3+ lines of visual acuity at
1 year. Antiangiogenic therapy
16
Documento approvato nella seduta della CRF del 12 Giugno 2014
Assessorato Politiche per la salute – Commissione Regionale del Farmaco
Principali studi nell’Occlusione Venosa Retinica di Branca (BRVO) o Centrale
(CRVO).
BRAVO, Fase III, n=395 (BRVO)
CRUISE, Fase III, n=390 (CRVO)
P
Inclusione: pz con DME secondario a BRVO (studio BRAVO) o CRVO (Studio CRUISE), BCVA
compresa tra 20/40 e 20/400 (BRVO) o 20/40 e 20/320 (CRVO), CMT ≥250 µm, maggioranza di pz
con RVO non ischemica.??
Esclusione: pz con storia di eventi CV o IMA nei 3 mesi precedenti, difetto pupillare afferente (>
rischio ischemico), evidenze di retinopatia diabetica.
I
R 0,3 o 0,5 mg (1/mese per 6 mesi)
N.B. dal terzo mese, nello studio BRAVO era permesso il laser come rescue
C
Iniezione sham
O
Primario: media delle variazioni medie nella BCVA (lettere) dal mese 1 al mese 6.
Secondari (principali): % pz con guadagno > 15 lettere ( rispetto al basale), riduzione CFT,
Altri: % pz BCVA ≥20/40
T
Trattamento: 1-6 mesi (doppio cieco) *
Follow-up: 6-11 mesi (osservazione: ritrattamento con R al bisogno in base a rivalutazione
mensile**)
CFT = spessore foveale centrale (misurato tramite OCT)
* Preceduti da 28 giorni di screening per escludere pz con miglioramento spontaneo (guadagno ≥10 lettere)
** BCVA ≤ 20/40 o CMT ≥250 µm. Il gruppo sham ha iniziato il tratt. con R 0,5mg.
Risultati: esito primario e secondari
BRAVO (6 mesi)
sham
CRUISE (6 mesi)
sham
R
R
n=132
0,3 mg
n=134
0,5 mg
n=131
n=130
0,3 mg
n=132
0,5 mg
n=130
7,3
16,6
18,3
0,8
12,7
14,9
Primario (in lettere)
media nella BCVA vs
baseline
17
Documento approvato nella seduta della CRF del 12 Giugno 2014
Assessorato Politiche per la salute – Commissione Regionale del Farmaco
∆ verso sham
[IC95%]
9,4
10,6
[6,6 – 12,2] [7,6- 13,6]
11,5
13,8
[7,7- 15,3] [10,3 – 17,4]
Secondari
Guadagno ≥ 15 lett. % pz
28,8
55,2
61,1
16,9
46,2
47,7
Riduzione CFT (µm)
158
337
345
157,7
337,3
345,2
BCVA ≥20/40 ** (%)
41,7
67,9
64,9
20,8
43,9
46,9
Studio BRAVO: sono ricorsi al laser il 54,5% dei pz nel gruppo sham, il 18,7% (0,3 mg) e il 19,8% (0,5
mg) di quelli trattati con R.
**Valore considerato soddisfacente per leggere e guidare.
Tutte le differenze sono statisticamente significative
18
Documento approvato nella seduta della CRF del 12 Giugno 2014