1
I diuretici sono farmaci capaci di aumentare il volume delle urine, ossia di indurre
diuresi. La maggior parte di essi è dotata di proprietà natriuretiche significative e
agisce a livello della membrana luminale dei tubuli renali bloccando i meccanismi
di trasporto ionico. Alcuni di essi sono inoltre dotati di effetti terapeutici extrarenali (ad es., proprietà vasodilatante diretta o indiretta).
2
Conoscere con esattezza il sito d’azione di ciascun diuretico consente di
ottimizzarne l’impiego attuando un blocco ragionato e, se necessario,
sequenziale del nefrone. Per esempio, nello scompenso cardiaco non responsivo
a furosemide appare spesso vantaggiosa l’associazione di tiazidici al fine di
bloccare sequenzialmente ansa di Henle e tubulo distale ed evitare che il sodio
non riassorbito nell’ansa venga riassorbito nel tubulo distale.
3
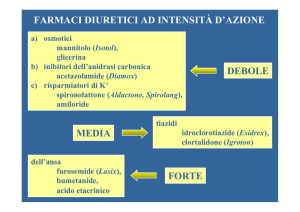
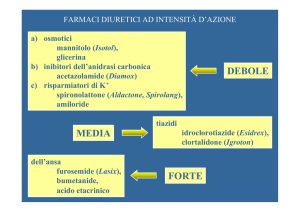
Diversi sono i siti d’azione dei diuretici: per esempio, acetazolamide e diuretici
osmotici agiscono a livello del tubulo contorto prossimale, furosemide e gli altri
diuretici dell’ansa a livello del tratto ascendente dell’ansa di Henle, i tiazidici a
livello del tubulo contorto distale, gli antialdosteronici a livello del tubulo
collettore. Come si vedrà, la gamma dei diuretici si è recentemente arricchita di
una nuova classe rappresentata dagli acquaretici, farmaci in grado di
antagonizzare l’azione dell’ADH a livello del nefrone distale.
4
La secrezione di ADH (adiuretina o vasopressina, od ormone antidiuretico) è
molto sensibile agli stimoli osmotici; tuttavia, anche riduzioni della volemia sono
in grado di stimolarne la secrezione. Iperosmolalità, ipovolemia e attività dei
recettori atriali stimolano la liberazione dell’ADH da parte dell’ipofisi.
5
Per agire, l’adiuretina deve legarsi a specifici recettori; sono stati identificati
fondamentalmente 3 tipi di recettori dell’ADH (V1a, V1b o V3 e V2), distribuiti
variabilmente a livello di piastrine, epatociti e miometrio (V1a), ipofisi anteriore
(V1b), membrana basolaterale del tubulo collettore, endotelio vascolare e cellule
muscolari lisce (V2).
6
Iperosmolalità, ipovolemia e attività dei recettori atriali stimolano la
liberazione dell’ADH da parte dell’ipofisi; una volta rilasciato, l’ADH si lega
ai recettori V1 (presenti peraltro anche nelle cellule mesangiali)
provocando vasocostrizione e ai recettori V2 provocando antidiuresi.
7
Struttura tridimensionale del recettore di AVP con posizionamento del
ligando naturale (AVP) e un antagonista.
Antagonisti non peptidici del recettore V2 della vasopressina si sono
rivelati promettenti nel trattamento delle iposodiemie ipervolemiche e
normovolemiche. Si tratta di farmaci con azione vasopressina-antagonista.
Questa nuova classe di molecole, denominate vaptani, si differenzia dai
diuretici classicamente utilizzati per l’interessante e specifica capacità di
determinare esclusiva escrezione di acqua (azione acquaretica).
8
Il legame dell’ADH ai recettori V2 sulla membrana basolaterale dei tubuli contorti
distali e dei dotti collettori midollari induce la sintesi, attraverso la via
dell’adenilato ciclasi/AMPc, di acquaporina-2 (AQP2) e ne favorisce l’inserimento
nella membrana apicale del tubulo, aumentando la permeabilità della cellula
all’acqua. Questo aumento della permeabilità della membrana consente la
retrodiffusione di acqua libera da soluti, con conseguente aumento
dell’osmolalità urinaria.
9
I vaptani sono antagonisti non peptidici dei recettori V2; legandosi a questi
recettori, tali farmaci bloccano l’azione dell’ADH sulla ritenzione di acqua, agendo
quindi con effetto “acquaretico” (escrezione di acqua libera da soluti). Esistono
attualmente diversi tipi di vaptani, con differente selettività per il legame
recettoriale: conivaptan (V1a, V2), lixivaptan (V2), tolvaptan (V2), satavaptan (V2).
Quando somministrato per via orale, tolvaptan induce aumento del volume
urinario e riduzione dell’osmolalità delle urine, senza alterazioni significative della
sodiuria.
10
Tolvaptan (OPC-41061), unico vaptano approvato per l’uso clinico nel nostro
Paese, è un derivato benzazepinico altamente selettivo nei confronti del recettore
V2. La sua affinità per il recettore V2 è 1,8 volte superiore rispetto a quella
dell’arginina vasopressina nativa. È 29 volte più selettivo per il recettore V2
rispetto al recettore V1a e la sua affinità per il recettore V1b è virtualmente nulla.
Tale selettività si traduce in un’azione mirata a livello del nefrone distale.
L'assenza di studi di farmacodinamica dose-risposta sopra i 60 mg fornisce un
razionale all’uso di un dosaggio massimo di 60 mg/una sola volta al giorno di
tolvaptan.
11
Sono stati condotti due studi multicentrici di fase III (Study of Ascending Levels
of Tolvaptan in Hyponatremia, SALT-1 e SALT-2) nell’ambito dei quali pazienti
(età >18 anni) con iponatremia non acuta lieve (sodiemia 130-134 mEq/L) o
severa (sodiemia <130 mEq/L) euvolemica o ipervolemica (sindrome da
inappropriata secrezione di ormone antidiuretico [SIADH], cirrosi, scompenso
cardiaco) sono stati randomizzati in doppio cieco a ricevere tolvaptan (SALT-1,
n=102; SALT-2, n=123) o placebo (SALT-1, n=103; SALT-2, n=120) per 30
giorni.
Endpoint primario dello studio era la correzione dell’iponatremia al 4° e al 30°
giorno di trattamento. Il numero di pazienti con natremia nella norma al 4° e al
30° giorno è risultato significativamente superiore nel gruppo tolvaptan rispetto
al gruppo placebo.
12
SALT-1 e SALT-2, al pari di altri studi, hanno evidenziato come il trattamento con
tolvaptan risulti associato a un miglioramento significativo dei punteggi al Mental
Component Summary del Medical Outcomes Study 12-item Short-Form (MCS SF12), indicando un miglioramento dello stato di coscienza e della qualità di vita nel
paziente iponatremico.
13
Tolvaptan risulta pertanto un farmaco maneggevole, che consente di correggere
iponatremie sia lievi sia gravi. Gli studi di Schrier e coll. hanno fatto inoltre
rilevare tempi alla dimissione più rapidi nel gruppo tolvaptan rispetto al gruppo
placebo (4,7 vs 8,4 giorni, p=0,04 nel gruppo con iponatremia severa).
14
La FDA statunitense ha approvato tolvaptan per il trattamento dell’iponatremia
associata a insufficienza cardiaca congestizia, cirrosi epatica e sindrome da
inappropriata secrezione di ormone antidiuretico.
15
Nello studio SALTWATER (Berl T, et al. J Am Soc Nephrol 2010;21(4):705-12),
nell’ambito del quale 111 pazienti iponatremici sono stati trattati con tolvaptan
per un tempo medio di 701 giorni, l’efficacia dei vaptani nel correggere
l’iponatremia si è mantenuta nel tempo con una tollerabilità accettabile.
Nell’EVEREST Outcome Trial (Konstam MA, et al. JAMA 2007;297(12):1319-31),
condotto con tolvaptan vs placebo (tempo medio di trattamento 8 mesi; minimo
60 giorni) su 4133 pazienti ricoverati per scompenso cardiaco (classe NYHA
III/IV), sebbene non sia stato osservato un vantaggio in termini di mortalità,
sono stati rilevati effetti positivi e persistenti su dispnea, controllo del peso,
edemi e natremia (in pazienti con iponatremia iniziale). Anche in questo studio
l’efficacia del vaptano è risultata essere dose-dipendente. Tolvaptan è stato ben
tollerato, con un profilo di sicurezza favorevole.
Sulla base di questi studi, anche l’European Medicines Agency (EMA) ha
approvato tolvaptan, primo antagonista della vasopressina in formulazione orale,
per il trattamento dell’iponatremia secondaria nella sindrome da inappropriata
secrezione di ormone antidiuretico (SIADH).
16
In generale tutti i pazienti sintomatici con iponatremia acuta, cronica e severa
devono essere trattati.
Nelle forme ipovolemiche è fondamentale correggere il bilancio idrico mediante
infusione di soluzione salina isotonica, mentre in quelle eu- e ipervolemiche, severe
e/o sintomatiche, è raccomandata la somministrazione di una soluzione ipertonica,
fino alla risoluzione dei sintomi e aumento della sodiemia >120 mEq/L. Possono
anche essere usati i diuretici dell'ansa, che stimolando l’escrezione di acqua libera
contribuiscono al recupero della sodiemia. Si deve monitorare il paziente con una
certa frequenza (almeno ogni 4-6 ore), e tale correzione deve essere graduale (0,4
mEq/L/ore), per evitare mielinolisi osmotica, potenzialmente letale, e altre lesioni
neurologiche.
Nelle forme eu- e ipervolemiche pauci-/asintomatiche il trattamento è invece la
restrizione dell'apporto idrico (800-1500 ml/die). In caso di insuccesso o
impossibilità di porre in essere tale provvedimento, può essere utile l’associazione di
un diuretico dell’ansa.
Tuttavia, specie per le forme eu- e ipervolemiche, spesso si hanno risultati non
soddisfacenti. In questo caso, l’uso di antagonisti della vasopressina, come
tolvaptan, consente un approccio terapeutico più specifico, rapido ed efficace.
17
La restrizione dell’apporto idrico durante le prime 24 ore di terapia con tolvaptan
può aumentare la probabilità di una correzione troppo rapida del sodio sierico, e
ciò si dovrebbe evitare in generale. Se pazienti sottoposti a restrizione di apporto
idrico vengono trattati con tolvaptan, si dovrebbe porre particolare attenzione
affinché tali pazienti non divengano eccessivamente disidratati o che la loro
concentrazione di sodio sierico non aumenti troppo velocemente.
Tolvaptan può causare effetti indesiderati correlati alla perdita d’acqua, come
sete, secchezza delle fauci e pollachiuria.
La durata del trattamento con tolvaptan è subordinata alla patologia di base e al
suo trattamento; il trattamento con tolvaptan dovrebbe essere protratto fino al
trattamento adeguato o finché l’iponatremia non rappresenti più un problema
clinico.
I pazienti devono essere monitorati a intervalli regolari per valutare l’eventuale
necessità di un ulteriore trattamento con tolvaptan.
18
Il trattamento con tolvaptan deve essere iniziato a una dose di 15 mg una volta
al giorno.
La dose può essere aumentata fino a un massimo di 60 mg una volta al giorno,
in base alla tollerabilità, per raggiungere il livello desiderato di sodio. Durante
l’aggiustamento della dose, monitorare lo stato dei pazienti relativamente al
livello di sodio e alla volemia. In caso di insufficiente miglioramento dei livelli di
sodio, si devono considerare altre opzioni terapeutiche, a sostituzione di
tolvaptan o in aggiunta a tolvaptan.
Tolvaptan è controindicato nei pazienti anurici e non è stato studiato in pazienti
con grave insufficienza renale. L’efficacia e la sicurezza in questa popolazione
non sono state ben determinate.
Non è necessario aggiustare la dose in pazienti con insufficienza epatica lieve o
moderata (classi A e B di Child-Pugh). Non sono disponibili informazioni su
pazienti con grave insufficienza epatica (classe C di Child-Pugh). In tali pazienti si
deve gestire con cautela la posologia e monitorare lo stato dei pazienti
relativamente a elettroliti e volemia.
Non è necessario aggiustare la dose nei pazienti anziani.
Non esistono esperienze nei bambini e negli adolescenti di età inferiore a 18
anni. Quindi non è raccomandato nei pazienti pediatrici.
http://www.emea.europa.eu/ema/
19
Le concentrazioni plasmatiche di tolvaptan sono state aumentate fino a 5,4 volte
l’area sotto la curva concentrazione/tempo (AUC) in seguito alla somministrazione di
forti inibitori del CYP3A4. Si deve usare cautela nel co-somministrare inibitori del
CYP3A4 (ad es., chetoconazolo, antibiotici macrolidi, diltiazem) e tolvaptan. La
somministrazione concomitante di succo di pompelmo e tolvaptan ha portato a un
aumento di 1,8 volte nell’esposizione a tolvaptan. I pazienti che assumono tolvaptan
devono evitare l’ingestione di succo di pompelmo.
Le concentrazioni plasmatiche di tolvaptan sono state ridotte fino all’87% (AUC) in
seguito alla somministrazione di induttori del CYP3A4. Esercitare cautela nella
somministrazione concomitante di induttori del CYP3A4 (ad es., rifampicina,
barbiturici) e tolvaptan.
In soggetti sani tolvaptan, un substrato del CYP3A4, non ha avuto effetti sulle
concentrazioni plasmatiche di alcuni altri substrati del CYP3A4 (ad es., warfarin o
amiodarone). Tolvaptan ha aumentato di 1,3-1,5 volte i livelli plasmatici di
lovastatina. Sebbene tale aumento non abbia rilevanza clinica, è indicativo del
potenziale di tolvaptan nell’aumentare l’esposizione ai substrati del CYP3A4.
Non vi è evidenza di interazioni clinicamente significative con diuretici dell’ansa e
tiazidici.
Le concentrazioni di digossina allo steady-state sono state aumentate (aumento di
1,3 volte della concentrazione plasmatica massima osservata [Cmax] e di 1,2 volte
dell’area sotto la curva di concentrazione plasmatica-tempo nell’arco dell’intervallo
di dosaggio [AUCτ]) quando somministrato con dosi multiple giornaliere di dosi da
60 mg di tolvaptan. Pertanto, i pazienti che ricevono digossina devono essere
valutati per eccessivi effetti della digossina durante il trattamento con tolvaptan.
http://www.emea.europa.eu/ema/
20
Tra tutti i vaptani disponibili in commercio, la molecola su cui vi è maggiore
esperienza anche clinica è tolvaptan, quindi le conclusioni sono riferite a questo
farmaco anche se alcuni effetti possono essere condivisi con altri vaptani.
Da quanto detto è possibile concludere che:
• i vaptani rappresentano un promettente approccio terapeutico in alternativa
alla restrizione idrica (o salina ipertonica) per il trattamento dell’iponatremia
asintomatica/moderatamente sintomatica secondaria a SIADH;
• i vaptani possono essere utilizzati sia come trattamento cronico sia a breve
termine in particolari condizioni cliniche che possono dare luogo a SIADH (ad es.,
polmoniti, iponatremie postoperatorie, traumi cranici);
• l’utilizzo dei vaptani potrà verosimilmente contribuire anche a ridurre i tempi e
quindi i costi di ospedalizzazione;
• i pazienti in trattamento con vaptani devono essere sottoposti a regolare
monitoraggio della natremia e devono essere valutate le interazioni possibili con
altri farmaci.
Si rammenta infine che al momento tolvaptan trova indicazione in Italia solo per
la sindrome da inappropriata secrezione di ADH.
21
22