
Gli agenti antibatterici:
Meccanismo di azione, sviluppo ed
applicazioni cliniche, meccanismi di
resistenza
I° anno - Laurea Magistrale Farmacia - 2012-2013
Jean-Denis Docquier
Dipartimento di Biologia Mediche
Policlinico "Le Scotte", Viale Bracci, II piano, V lotto
Tel. 0577 23 3134
[email protected]
Gli agenti antibatterici
Libri di riferimento:
Antibiotics: actions, origins, resistance
C. Walsh (ASM Press)
Bacteria versus antibacterial agents:
an integrated approach
O. A. Mascaretti (ASM Press)
Studiare le diapositive!
Importanza degli antibiotici
Usati in medicina, medicina veterinaria e come promotori
della crescita (settore agro-alimentare)
Consumo: >13.000 tonnellate ogni anno nell’Unione Europea
786 t
6%
Human use
3902 t
29%
65%
8528 t
Veterinary
therapeutic
Growth promotion
Classificazione dei farmaci antibatterici
Struttura chimica
(β-lattamici, glicopeptidi)
Meccanismo di azione
(inibitori sintesi proteica, inibitori trascrizione)
Spettro di azione
(ampio spettro, spettro ristretto)
Farmacocinetica
(orali, parenterali)
Effetti biologico
batteriostatici inibizione reversibile della crescita batterica
battericidi inibizione irreversibile crescita batterica (morte cellulare)
Log cellule batteriche vitali
Antibiotico
effetto batteriostatico
effetto battericida
Tempo (ore)
Misura del potere antimicrobico
Concentrazione minima inibente
Concentrazione crescente
Misura del potere antimicrobico
Diffusione in agar
Incubazione
(solitamente
16-24 ore, 37 °C)
Farmaci antibatterici: meccanismo di azione
Funzione alterata
o bloccata
antibiotico
Bersaglio molecolare
blocco reversibile della crescita batterica
(azione batteriostatica)
I bersagli molecolari devono essere
strutture non presenti o diverse da
quelle presenti nelle cellule
eucariotiche (tossicità selettiva)
morte cellulare
(azione battericida)
Farmaci antibatterici
Sostanze che:
inibiscono la crescita batterica a concentrazioni che non
danneggiano le cellule dell’ospite (tossicità selettiva)
possono essere utilizzate per la chemioterapia delle
infezioni batteriche
Sostanze di origine naturale Antibiotici
Sostanze di sintesi Chemioterapici
Meccanismo d’azione della penicillina
La penicillina, e gli altri β-lattamici, inibiscono
la sintesi del peptidoglicano, una struttura
macromolecolare tipica dei batteri
Meccanismo d’azione della penicillina
Le caratteristiche di un buon antibiotico
Antibiotico
Porine
Membrana o parete
Bersaglio
Essere selettivo
Esibire una bassa tossicità
Presentare un buon profilo farmacologico
Farmaci antibatterici: BERSAGLI MOLECOLARI
Sintesi dei folati
DNA
topoisomerasi
Membrana
plasmatica
Trascrizione
Sintesi proteica
Sintesi del peptidoglicano
Bersagli molecolari degli antibiotici
Importanza degli antibiotici β-lattamici
Sulfonamides
Others
Quinolones
Macrolides,
lincosamides &
streptogramins
β-lactams
Tetracyclines
Goossens et al. (2005) Lancet
Gli inibitori della sintesi della parete cellulare
Numerosi antibiotici attualmente in uso nella pratica clinica
sono inibitori della sintesi della parete cellulare:
Struttura unica ai Batteri e essenziale per la loro crescita
Azione antibatterica altamente selettiva
Due distinti meccanismi di azione:
β-lattamici
Fosfomicina
Cicloserina
Inibitori di enzimi
coinvolti nella
biosintesi
Glicopeptidi
Bacitracina
Sequestro del
substrato
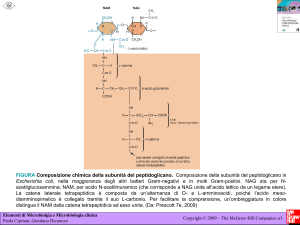
Struttura del PEPTIDOGLICANO
NAM = acido N-acetil muramico
NAG = N-acetil glucosamina
Catene
glicaniche
NAG
NAM
NAG
NAM
NAM
NAG
NAM
NAG
NAG
NAM
NAG
NAM
Componente
peptidica
L-alanina
D-glutammico
L-lisina (o meso-DAP)
D-alanina
5 x L-glicina
Biosintesi Peptidoglicano – I
(sintesi del NAM)
NAG-1-P
PP
P-enolpiruvato (PEP)
UTP
UDP-NAG
NAG = N-acetil glucosamina
NAM = acido N-acetil muramico
REDUTTASI
UDP-NAM
UDP-NAG
TRASFERASI
(PEP)
CH2OH
H
UDP
O
O
H
OH
H
H
NH
CH2OH
OH
H
C=O
CH3
H
UDP
O
O
H
OH
H
H
O
H
HC – CH3
COOH
NH
C=O
CH3
Biosintesi Peptidoglicano – II
(sintesi del pentapeptide)
NAG-1-P
UTP
PP
NAG = N-acetil glucosamina
NAM = acido N-acetil muramico
P-enolpiruvato (PEP)
UDP-NAG
UDP-NAG
(PEP)
UDP-NAM
L-Ala
RACEMASI
D-Ala
LIGASI
D-Ala-D-Ala
UMP
NAM
Membrana
plasmatica
Undecaprenil-P
P
Biosintesi Peptidoglicano – III
(completamento del monomero)
5 x L-Gly
Citosol
NAM
Undecaprenil-P
Membrana
plasmatica
Undecaprenil-P
P
NAG
P
NAG
NAM
Biosintesi Peptidoglicano – IV
(assemblaggio del monomero)
Undecaprenil-P
Membrana
plasmatica
Undecaprenil-P
Citosol
PIROFOSFATASI
Pi
TRANSGLICOSILASI
P
NAG
NAM
NAG-NAM- NAG-NAM-NAG-NAM-
Enzimi di membrana
con il dominio catalitico
all’esterno della membrana
Catena peptidoglicanica in crescita
Biosintesi Peptidoglicano – V
(cross-link delle catene)
NAM
NAM
NAM
Catene non cross-linkate
NAG
NAG
NAG
TRANSPEPTIDASI
Catene cross-linkate
(struttura rigida)
NAG
NAM
NAM
NAG
NAG
D-Ala
D-Ala
NAM
Enzimi di membrana
con il dominio catalitico
all’esterno della membrana
NAG = N-acetil glucosamina
Biosintesi Peptidoglicano
(sintesi del NAM)
NAG-1-P
UTP
PP
NAM = acido N-acetil muramico
P-enolpiruvato (PEP)
UDP-NAG
REDUTTASI
UDP-NAG
TRASFERASI
MurA
Fosfomicina
(PEP)
UDP-NAM
Fosfomicina: meccanismo di azione
O
HOOC
C
O
CH2
P
OH
OH
H
H
O
C
C
P
H3 C O
PEP
OH
OH
Fosfomicina
(analogo strutturale del PEP)
UDP-NAG enolpiruvil
trasferasi – SH
Effetto biologico: battericida
(MurA)
La fosfomicina è un
substrato “suicida”
per l’enzima MurA
La fosfomicina
compete con il substrato
naturale per l’enzima
Enzima – S
H
H
O
C
C
P
CH3
OH OH
OH
formazione di un legame
covalente stabile che
inattiva l'enzima
Biosintesi Peptidoglicano
(sintesi del pentapeptide)
O-
N
D-Ala
O
H
NAG-1-P
UTP
PP
NH3+
P-enolpiruvato (PEP)
UDP-NAG
UDP-NAG
(PEP)
UDP-NAM
D-cicloserina
L-Ala
RACEMASI
D-Ala
LIGASI
D-Ala-D-Ala
La D-cicloserina agisce
come substrato suicida
per la racemasi e la
ligasi, inattivandole
Biosintesi Peptidoglicano
(riciclo di undecaprenil-P)
Undecaprenil-P
Undecaprenil-P
Membrana
plasmatica
Undecaprenil-P
Citosol
Bacitracina
PIROFOSFATASI
Pi
P
P
NAG
NAM
Bacitracina
NAG-NAM-NAG-NAMAttiva solo sui Gram+
(non attraversa la membrana esterna dei Gram-)
Catena peptidoglicanica in crescita
Undecaprenil-P
Biosintesi Peptidoglicano – fasi tardive
Membrana
plasmatica
P
NAG
NAM
Reazione di
TRANSGLICOSILAZIONE
NAG-NAM-NAG-NAM-
Glicopeptidi
NAM
NAM
NAM
Catena peptidoglicanica in crescita
Reazione di
TRANSPEPTIDAZIONE
NAG
NAG
NAG
Cross-link delle catene peptidoglicaniche
Undecaprenil-P
Glicopeptidi – meccanismo di azione
Membrana
plasmatica
I glicopeptidi hanno
elevata affinità per il
dipeptide D-ala-D-ala
D-ala-D-ala
dipeptide
P
NAG
NAM
Reazione di
TRANSGLICOSILAZIONE
NAM
NAM
NAG-NAM-NAG-NAM-
NAM
Catena peptidoglicanica in crescita
Reazione di
TRANSPEPTIDAZIONE
NAG
NAG
NAG
Cross-link delle catene peptidoglicaniche
Glicopeptidi
• Vancomicina
• Teicoplanina
Vancomicina
Teicoplanina
(glicolipopeptide)
> Attivi solo sui Gram-positivi
> Battericidi (lentamente)
Undecaprenil-P
Biosintesi Peptidoglicano – fasi tardive
Membrana
plasmatica
P
NAG
NAM
Reazione di
TRANSGLICOSILAZIONE
NAM
NAM
NAM
b-Lattamici
NAG-NAM-NAG-NAM-
Catena peptidoglicanica in crescita
Reazione di
TRANSPEPTIDAZIONE
NAG
NAG
NAG
Cross-link delle catene peptidoglicaniche
I b-lattamici bloccano gli enzimi
che catalizzanola reazione di
transpeptidazione
b-Lattamici – meccanismo di azione
Anello b-lattamico
(mima il dipeptide D-Ala-D-Ala)
S
Transpeptidasi
N
O
OH
Membrana plasmatica
Gli enzimi bersaglio
degli antibiotici b-lattamici
sono anche detti
Penicillin-Binding Proteins
(PBP)
Attività battericida
S
HN
O O
Enzima inattivato
CH2
O
H
C
N
O
S
N
COOH
Penicillina G – il primo antibiotico (1940)
Analogia strutturale fra dipeptide D-Ala-D-Ala e le peniccilline
The discovery of natural antibiotics
"One sometimes finds what one is not looking for."
"People have called it a miracle. For once in my life as a scientist, I agree.
It is a miracle, and it will save lives by thousands."
Sir Alexander Fleming
Nobel Prize for Medicine, 1945
The discovery of natural antibiotics
Penicillium notatum produces a compound that inhibits growth of
bacteria
Staphylococcus
epidermidis
Inibizione della
crescita
Effect of penicillin on bacterial cells
TEM microscopy
Principali famiglie di b-lattamici
S
R
COOH
N
O
S
R
O
R’
N
COOH
R’
R
O
R
O
N
COOH
R’
N SO3H
Penicilline
- penicillina G
- ampicillina
- oxacillina
- ticarcillina
Cefalosporine
- cefazolina
- cefamandolo
- ceftriaxone
- ceftazidime
Carbapenemi
- imipenem
- meropenem
- ertapenem
Monobattami
- aztreonam
Le diverse molecole
differiscono per
> spettro di attività
> farmacocinetica
I b-lattamici sono gli
antibiotici più utilizzati
per la loro efficacia,
tollerabilità e
versatilità di impiego
Evoluzione delle
Cefalosporine in
“generazioni”
Gruppo “ossimmino”
Migliora attività antibatterica
e farmacocinetica
Farmaci antibatterici: BERSAGLI MOLECOLARI
Membrana
plasmatica
Polimixine
Lipopeptidi ciclici
X
DAB
6-MO - DAB - Thr - DAB - DAB
Thr
Leu
DAB
DAB
Polimixina B
Colistina
DAB = acido 2,4 diaminobutirrico
6-MO = acido 6-metil ottanoico
Thr = treonina
Leu = leucina
X = D-fenilalanina
X = D-leucina
Meccanismo: attraversano la membrana esterna dei batteri Gramnegativi e danneggiano la membrana plasmatica ricca di
fosfatidiletanolamina
(Non sono attive sui Gram-positivi la cui membrana è
povera in phosfatidiletanolamina)
Attività battericida
Daptomicina
Lipopeptide ciclico
Meccanismo: interagisce con la membrana plasmatica e la danneggia.
(E’ attiva solo sui Gram-positivi perché non attraversa
la OM dei Gram-negativi).
Attività battericida
Principali bersagli dei farmaci antibatterici:
DNA topoisomerasi
DNA topoisomerasi di tipo II:
- DNA girasi
- DNA Topoisomerasi IV
The bacterial chromosome
DNA ultrastructure is controlled by enzymes called DNA
topoisomerases:
Type I single strand break
Type II double strand break
Bacterial DNA topoisomerases
E. coli topoisomerases and their role in DNA supercoiling
and chromosome replication
Enzyme
Type
Gene(s)
Major enzyme function
Topoisomerase I
I
topA
Relaxes negative supercoils
Topoisomerase II
(DNA gyrase)
II
gyrA
gyrB
Introduces negative supercoils;
relaxes positive supercoils
I
topB
Decatenates replication
intermediates and interlinked
DNA dimers
II
parC
parE
Decatenates DNA: removes
positive and negative supercoils
Topoisomerase III
Topoisomerase IV
Catalytic cycle of DNA gyrase
Stabilize
positive (+)
node
(-)
Break
back
segment
Reseal
on front
side
(-)
(-)
(-)
Requires a double strand break, translocation of a DNA
strand while broken DNA is covalently bound to the
enzyme; ligation ensures that missing bonds are resealed
GyrB
GyrA
Mechanism of DNA gyrase
Mechanism of DNA gyrase
Double strand breakage involves a tyrosine residue, which
covalently binds each DNA extremities
Replicazione cromosoma batterico
DUPLICAZIONE
SEMICONSERVATIVA
bidirezionale; inizia
dalla regione oriC
Cromosoma
(DNA bicatenario
superspiralizzato)
Le TOPOISOMERASI di tipo II
svolgono un ruolo cruciale durante
la replica del cromosoma
La DNA TOPOISOMERASI IV
svolge un ruolo essenziale per la
segregazione dei due cromosomi
2 cromosomi
superspiralizzati
Agents targeting type II DNA topoisomerases:
the QUINOLONES
Quinolone ring
NALIDIXIC ACID
The first quinolone agent (1962)
Chinoloni:
meccanismo di azione
DNA
Attività battericida
Formazione di un complesso ternario DNA-chinolone-topoisomerasi
Frammentazione del cromosoma batterico
Interazione
con il DNA
CHINOLONI
O
Interazione
con l'enzima
COOH
CH3
N
N
CH2-CH3
interazione tra
molecole di farmaco
e farmacocinetica
O
ACIDO NALIDIXICO
COOH
CH3
N
N
CH2-CH3
- attivo solo su alcuni
Gram-negativi
- eliminato rapidamente
per via urinaria
O
N
N
N
H
N
N
COOH
ACIDO PIPEMIDICO
CH2-CH3
- spettro ampliato
include P. aeruginosa
- solo per infezioni
urinarie
O
CHINOLONI FLUORURATI
F
N
NORFLOXACINA
- spettro ampliato
(gram-negativi, stafilococchi, enterococchi)
- solo per infezioni urinarie
COOH
N
CH2CH3
N
H
O
F
COOH
CIPROFLOXACINA
- spettro ampio
(gram-negativi, stafilococchi, enterococchi)
N
- farmacocinetica migliorata
(anche per infezioni sistemiche)
N
H
N
NUOVI CHINOLONI FLUORURATI
O
F
LEVOFLOXACINA
- ampio spettro
- maggiore attività sui gram-positivi
(anche streptococchi)
COOH
N
N
O
CH3
N
H3C
O
F
GATIFLOXACINA
- ampio spettro
- maggiore attività sui gram-positivi
(anche streptococchi)
H3C
COOH
N
N
O
H3C
N
H
NUOVI CHINOLONI FLUORURATI
MOXIFLOXACINA
- maggiore attività su Gram-positivi
e anaerobi (ridotta attività sui
Gram-negativi)
F
H
COOH
N
N
N
O
H3C
CEPHALOSPORINS vs. QUINOLONES
a generational comparison
Cephalosporins
Quinolones
1st generation
1st generation
Improved activity
on gram-negatives
4th generation
Improved activity
on gram-positives
4th generation
Altri farmaci attivi su la DNA girasi:
Gli antibiotici cumarinici
Novobiocina
DNA
Novobiocina
La NOVOBIOCINA
si lega alla subunità B
della DNA girasi inibendo
l’attività ATPasica
azione batteriostatica
Principali bersagli dei farmaci antibatterici:
Via metabolica della
sintesi dei folati
The folate pathway
dihydropteridine-PP
Dihydropteroate
synthetase
p-aminobenzoic acid (PABA)
(DHPS)
dihydropteroate
Dihydrofolate
synthetase
Glutamic acid (ATP-dependent)
(DHFs)
dihydrofolic acid (DHF)
Dihydrofolate
reductase
(DHFR)
NADPH-dependent
tetrahydrofolic acid (THF)
necessary for the biosynthesis of:
- purines
- thymidine
- methionine
- glycine
Dihydropteroate synthesis
dihydropteridine-PP
p-aminobenzoic acid (PABA)
+
Dihydropteroate
synthetase
(DHPS)
dihydropteroate
Dihydropteroate synthase
Tetrahydrofolate synthesis
Dihydrofolic acid
Dihydrofolate
reductase
NADPH
(DHFR)
NADP+
Tetrahydrofolic acid
dihydrofolate reductase
Importance of THF
THF is a precursor of N5,N10-methylene-THF, a methyldonor co-factor used in many biosynthetic reactions
Example: Thimidylate synthase
TS
N5,N10-methylene-THF
dUTP
DHF
dTTP
Inhibitors of the folate pathway
dihydropteridine-PP
Dihydropteroate
synthetase
p-aminobenzoic acid (PABA)
(DHPS)
Sulfonamides
(structural analogs of PABA)
dihydropteroate
dihydrofolic acid (DHF)
Dihydrofolate
reductase
(DHFR)
tetrahydrofolic acid (THF)
necessary for the biosynthesis of:
- purines
- thymidine
- methionine
- glycine
Static activity
The sulfa drugs
The sulfa drugs
Prontosil (prodrug of sulfanilamide)
Sulfamethoxazole
Inhibitors of the folate pathway
dihydropteridine-PP
Dihydropteroate
synthetase
p-aminobenzoic acid (PABA)
(DHPS)
Sulfonamides
dihydropteroate
Sulfamethoxazole + Trimethoprim = synergism
dihydrofolic acid (DHF)
Dihydrofolate
reductase
> broadened spectrum
> cidal activity
> less prone to resistance
(DHFR)
Trimethoprim
tetrahydrofolic acid (THF)
necessary for the biosynthesis of:(structural analog of the pteridine
moiety of DHF)
- purines
- thymidine
Static activity
- methionine
- glycine
Trimethoprim and TMP-SMX
Analog of the pteridin portion of DHF:
DHF
Used in combination with SMX (same antimicrobial
spectrum and PK/PD properties, 1:5 ratio)
Inibitori della sintesi dei folati
diidropteridina-PP
Diidropteroato
sintetasi
acido p-aminobenzoico (PABA)
(DHPS)
Sulfamidici
(analoghi strutturali del PABA)
acido diidropteroico
acido diidrofolico (DHF)
Diidrofolato
reduttasi
(DHFR)
acido tetraidrofolico (THF)
necessario per la biosintesi di:
- purine,
- timidina,
- metionina
- glicina
azione batteriostatica
Inibitori della sintesi dei folati
diidropteridina-PP
Diidropteroato
sintetasi
acido p-aminobenzoico (PABA)
(DHPS)
Sulfamidici
(analoghi strutturali del PABA)
acido diidropteroico
acido diidrofolico (DHF)
Diidrofolato
reduttasi
(DHFR)
Sulfamidico + Trimethoprim = sinergismo
> spettro ampliato
> attività battericida
acido tetraidrofolico (THF)
Trimethoprim
(analogo strutturale di parte del DHF)
azione batteriostatica
Principali bersagli dei farmaci antibatterici:
Trascrizione
La trascrizione nei batteri
La trascrizione nei batteri
sigma released
Ansamicine
Rifampicina
Target: RNA polimerasi, subunità b
Effetto: blocco trascrizione
effetto battericida
Attive su:
> micobatteri
> Gram-positivi
> alcuni Gram-negativi
Antibiotics interferring with transcription
Rifamycins (ansamycins)
Only one commercial product (semi synthetic derivate of
Rifamycin B produced by Nocardia mediterranei)
Ansa bridge
CH3COO
CH3O
OH
OH
OH
O
OH
NH
O
N
O
N
N
OH
O
Naphtol ring
Rifampin
Used as a antitubercular (often in combination with isoniazid)
8-10 million cases of tuberculosis
Mycobacterium tuberculosis, leading infective agents as cause of
death
Structure of the bacterial RNA polymerase
b’ subunit
subunit
2 subunits
b subunit
Mg2+
The core enzyme (MW ~380 kDa)
Mg2+ ion plays an important role in catalysis and protein stability
Mechanism of transcription in bacteria
Three steps
Initiation, elongation, termination
The core enzyme cannot initiate transcription by itself, but require
the presence of an additional protein, the σ factor (forming the
holoenzyme)
The σ factor is released after initiation
Mechanism of action of rifampin
b’ subunit
subunit
2 subunits
b subunit
Mg2+
Binds to the b subunit of the RNA polymerase (IC50 ~ 0.005-0.01 μg/ml)
Shorter distance with catalytic Mg2+ is 12 Å
Mechanism of action of rifampin
Rif Concentration (μM)
Run-off transcript
Normal transcript
in vitro
transcription
assay
3-mer RNA (CpApU)
Rifampin does not block the formation of the initiation complex neither
inhibits catalysis
BUT
Rifampin blocks the RNA elongation
Mechanism of action of rifampin
Steric hindrance during RNA strand polymerization
WHEN
RNA transcript length is 2-3 nt
Principali bersagli dei farmaci antibatterici:
Sintesi proteica
30S
50S
complesso di pre-inizio
tRNA
mRNA
30S
Aminoglicosidi
mRNA
30S
50S
Complesso di inizio
proteina
30S
50S
Traduzione
mRNA
Errori di traduzione
Blocco traduzione
Inhibitors of protein synthesis
Aminoglycosides
30S ribosome subunit inhibitor
Tetracyclines
Macrolides
Lincosamides
Chloramphenicol
Streptogramins
Oxazolidinones
50S ribosome subunit inhibitor
Aminoglicosidi
Purpurosamina
Streptidina
2-deossistreptamina
L-streptoso
Streptomicina
Kanamicina
Tobramicina
Netilmicina
Amikacina
Garosamina
Gentamicina
N-metil-glucosamina
Bersagli
• Ribosoma (subunità 30S)
• Membrana esterna dei Gram-negativi (policationi)
- Attività battericida
- Inattivi su: > batteri anaerobi
> batteri intracellulari
30S
50S
Complesso di pre-inizio
tRNA
mRNA
30S
mRNA
30S
50S
Complesso di inizio
Oxazolidinoni
legano la subunità 50S
e bloccano la sintesi
proteica a livello del
complesso di inizio
attività
batteriostatica
Oxazolidinoni
una nuova classe
di farmaci antibatterici
Linezolid
Attivo su Gram-positivi
(non attraversa la OM dei Gram-negativi)
Altri farmaci anti-ribosomali
proteina
30S
mRNA
50S
Traduzione
Tetracicline
Cloramfenicolo
Ketolidi
attività
batteriostatica
Macrolidi
Lincosamine
Streptogramine
Tetracicline
R
Legano la subunità 30S
(rRNA 16S)
bloccano l'accesso di
aminoacil-tRNA al sito A
del ribosoma
Ampio spettro
Attività sui batteri intracellulari
Cloramfenicolo
Lega la subunità 50S (peptidil-transferasi)
Blocca la formazione del legame peptidico
Ampio spettro
Attività su batteri intracellulari
Tossicità midollare
Macrolidi
Legano la subunità 50S del ribosoma
(23S rRNA) e bloccano la
transpeptidazione e la traslocazione
Eritromicina
> Attivi principalmente sui Gram-positivi
> Attivi sui batteri intracellulari
Lincosamine
Meccanismo di azione simile ai macrolidi
Spettro ed attività simile ai macrolidi
Buona attività sugli anaerobi
Clindamicina
Ketolidi
Meccanismo di azione e
spettro simili a quelli
dei macrolidi
Maggiore affinità per il
bersaglio ribosomiale
Telitromicina
Streptogramine
30%
group B
70%
group A
Meccanismo di azione e spettro simili a
quelli dei macrolidi
Legano la subunità 50S del ribosoma in
due siti diversi (azione sinergica)
Farmaci “attivati” nella cellula batterica
Metronidazolo
Contiene un gruppo NO2 attivato da
nitroreduttasi cellulari presenti negli anaerobi
Generazione di radicali liberi e altre specie
chimiche reattive che danneggiano gli acidi
nucleici e le altre macromolecole (interferisce con
la struttura elicoidale del DNA)
Attività battericida su:
- ANAEROBI OBBLIGATI
- Helicobacter pylori
Farmaci “attivati” nella cellula batterica
Isoniazide
Metabolizzato dalla Catalasi-Perossidasi KatG
di Mycobacterium tuberculosis
Generazione di metaboliti che bloccano la sintesi
dei lipidi di membrana
Attività battericida su:
MICOBATTERI TUBERCOLARI

![mutazioni genetiche [al DNA] effetti evolutivi [fetali] effetti tardivi](http://s1.studylibit.com/store/data/004205334_1-d8ada56ee9f5184276979f04a9a248a9-300x300.png)


![(Microsoft PowerPoint - PCR.ppt [modalit\340 compatibilit\340])](http://s1.studylibit.com/store/data/001402582_1-53c8daabdc15032b8943ee23f0a14a13-300x300.png)






