Corso di Laurea Magistrale in
“Medicina e Chirurgia”
Biofisica e Fisiologia
Sinapsi
Il neurone
Caratteristica peculiare delle cellule nervose è quella di condurre e
comunicare informazioni. Le zone specializzate a livello delle quali le
cellule entrano in comunicazione sono definite sinapsi
Una sinapsi rappresenta sempre un punto di discontinuità strutturale di una via di
comunicazione intercellulare. Le membrane dei due elementi che prendono contatto sinaptico
restano sempre distinte e separate da uno spazio, la fessura sinaptica.
Tipi di sinapsi
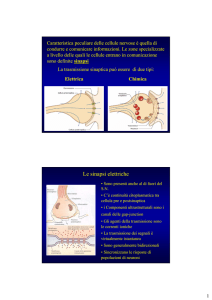
La trasmissione sinaptica può essere di due tipi:
Elettrica
Chimica
La variazione del potenziale di membrana di una cellula viene trasmesso ad
un’altra adiacente per flusso diretto di corrente.
Si trovano nel SNC e periferico dove si rende necessaria un’alta velocità di
connessione e sincronizzazione nell’attività dei neuroni vicini.
•
Le sinapsi elettriche permettono una rapida comunicazione tra neuroni adiacenti sincronizzandone
l’attività elettrica.
Quando una delle due cellule connesse da gap junctions viene eccitata, si crea un gradiente di potenziale
tra l’elemento presinaptico depolarizzato e quello postsinaptico non depolarizzato. Attraverso i connessoni
fluiscono nella cellula postsinaptica ioni lungo il gradiente di potenziale. Raggiunto il valore soglia nella
cellula postsinaptica, la depolarizzazione instaurerà il potenziale d’azione.
•
La comunicazione è bidirezionale, i connessoni trasmettono elettricamente nei due sensi e può
essere eccitatoria o inibitoria a livello della stessa sinapsi
• Le cellule pre e postsinaptiche si trovano sempre nello stesso stato di polarizzazione, cioè non è
possibile l’instaurarsi di un’inibizione a partire da un’eccitazione
• Contatti con cellule vicine, la trasmissione dell’eccitazione non è possibile nei confronti di cellule distanti
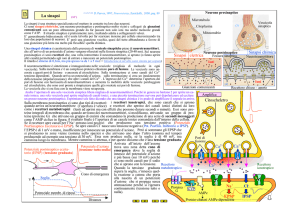
Sinapsi chimiche
-sito di contatto tra due cellule nervose
-ruolo nella trasmissione delle informazioni
-il contatto neurone-fibra muscolare prende il nome di placca
motrice o giunzione neuromuscolare
Sinapsi chimiche
-l’arrivo del potenziale d’azione nella terminazione presinaptica depolarizza la membrana;
-si aprono i canali per gli ioni Ca2+ voltaggio-dipendenti;
-le vescicole sinaptiche contenenti il neurotrasmettitore sono fissate ai filamenti di actina del
citoscheletro mediante la sinapsina o sono ancorate direttamente alla membrana presinaptica mediante la
sinaptotagmina;
-l’entrata del Ca2+ determina l’attivazione della sinaptotagmina con conseguente disancoraggio delle
vescicole alla membrana presinaptica ed esocitosi del contenuto vescicolare all’interno della fessura
sinaptica; inoltre, il Ca2+ attiva la proteinchinasi calcio-calmodulina dipendente che va a fosforilare la
sinapsina, ciò determina il rilascio delle vescicole dai filamenti del citoscheletro le quali possono
ancorarsi alla membrana presinaptica per essere utilizzate in un secondo processo di trasmissione
sinaptica;
- Il neurotrasmettitore viene rilasciato nella fessura sinaptica caratterizzata da un ampiezza di 20-50
nm. In 0,1 ms il neurotrasmettitore diffonde verso la membrana postsinaptica dove si lega ai recettori
specifici.
In caso di un attività ad alta frequenza si può determinare un affaticamento sinaptico (deplezione delle
vescicole disponibili per essere subito rilasciate)
La liberazione del neurotrasmettitore implica il
passaggio delle vescicole sinaptiche attraverso una
serie di stadi preparatori:
1. Liberazione dall’interazione con il citoscheletro
2. Direzionamento ed ancoraggio alle zone attive
3. Predisposizione alla fusione (priming)
4. Fusione con la membrana presinaptica
5. Recupero della membrana delle vescicole
6. Riformazione vescicole
Ogni processo coinvolge proteine diverse:
1. Sinapsine: famiglia di 4 proteine deputate
all’ancoraggio delle vescicole di secrezione al
citoscheletro. Quando la sinapsina I è fosforilata da
una chinasi calcio-calmodulina-dipendente, si ha il
distacco della vescicola dal citoscheletro.
2. Rab3, proteina G vescicolare specifica, e Rim
indirizzano le vescicole libere verso le zone attive
3. SNARE (sintaxina, sinaptobrevina, Snap-25),
ancorano le vescicole alle zone attive e facilitano la
fusione
4. Sinaptotagmina legata al Ca2+, promuove i
processi di fusione ed esocitosi
Liberazione dal citoscheletro
Le vescicole al di fuori delle zone attive (riserva di neurotrasmettitore) sono
ancorate ad una rete di filamenti di actina del citoscheletro, dalla sinapsina in forma
non fosforilata.
La fosforilazione da parte della PK-Ca2+/Calmodulina dipendente, in seguito a
depolarizzazione del terminale assonico ed ingresso di Ca2+ libera le vescicole che si
muovono verso le zone attive.
Indirizzamento vescicole alle zone attive: Rab3-GTP si lega alla membrana delle
vescicole ed interagisce con Rim (zone attive di membrana).
Ancoraggio ai siti attivi: per interazione proteine vescicole-proteine membrana
(SNARE)
Emifusione: SNARE vescicola-membrana creano stretto contatto tra membrana
vescicolare e presinaptica.
Fusione: La sinaptotagmina legandosi al Ca2+ cambia la sua conformazione e si lega ai
fosfolipidi di membrana determinando l’apertura di un poro di fusione.
Le proteine SNARE vescicolari e presinaptiche (sinaptobrevina, sintaxina,
snap-25) interagiscono secondo un modello a chiusura lampo (zippering)
che consente la fusione delle due membrane.
La fusione completa è frenata dalla proteina vescicolare sinaptotagmina.
Il legame sinaptotagmina-Ca2+ determina un cambiamento di
conformazione della proteina favorendo il processo di completa fusione.
Il legame Ca2+-sinaptotagmina favorisce il processo
di completa fusione e la formazione del poro di fusione
Action
potential
Axon
terminal
Synaptic
vesicle
1
Postsynaptic
cell
1 An action potential depolarizes
the axon terminal.
Action
potential
1 An action potential depolarizes
the axon terminal.
2 The depolarization opens voltagegated Ca2+ channels and Ca2+
enters the cell.
Axon
terminal
Synaptic
vesicle
1
Ca2+
Voltage-gated
Ca2+ channel
2
Ca2+
Postsynaptic
cell
1 An action potential depolarizes
the axon terminal.
Action
potential
2 The depolarization opens voltagegated Ca2+ channels and Ca2+
enters the cell.
Axon
terminal
3 Calcium entry triggers exocytosis
of synaptic vesicle contents.
Synaptic
vesicle
1
Ca2+
Voltage-gated
Ca2+ channel
2
Ca2+
Postsynaptic
cell
Docking
protein
3
1 An action potential depolarizes
the axon terminal.
Action
potential
2 The depolarization opens voltagegated Ca2+ channels and Ca2+
enters the cell.
Axon
terminal
3 Calcium entry triggers exocytosis
of synaptic vesicle contents.
Synaptic
vesicle
4 Neurotransmitter diffuses across
the synaptic cleft and binds with
receptors on the postsynaptic cell.
1
Ca2+
Voltage-gated
Ca2+ channel
2
Ca2+
Postsynaptic
cell
Docking
protein
3
4
Receptor
1 An action potential depolarizes
the axon terminal.
Action
potential
2 The depolarization opens voltagegated Ca2+ channels and Ca2+
enters the cell.
Axon
terminal
3 Calcium entry triggers exocytosis
of synaptic vesicle contents.
Synaptic
vesicle
4 Neurotransmitter diffuses across
the synaptic cleft and binds with
receptors on the postsynaptic cell.
1
Ca2+
Voltage-gated
Ca2+ channel
2
Ca2+
Postsynaptic
cell
Docking
protein
3
5 Neurotransmitter binding initiates
a response in the postsynaptic
cell.
4
Receptor
5
Cell
response
Inactivation of
Neurotransmitters
La quantità di neurotrasmettitore rilasciato dipende dalla frequenza
dei potenziali d’azione nel neurone presinaptico. Se non arriva
un’ulteriore potenziale d’azione, il rilascio di neurotrasmettitore si
arresta in pochi millisecondi perché i canali voltaggio-dipendenti per il
calcio si chiudono immediatamente dopo l’apertura ed il calcio
citoplasmatico viene attivamente pompato all’esterno del bottone
sinaptico per riportare le concentrazioni di tale ione ai valori base.
Presynaptic modulation of transmission
Axo-axonal communication (here, between A & B)
can modify classical synaptic communication
(here, between B & C); this can result in
presynaptic inhibition or presynaptic facilitation.
Note: the Terminal B must have receptors
for the signal released from A.
Membrana presinaptica
Membrana postsinaptica
Il tempo intercorrente tra l’arrivo del potenziale d’azione a livello del
bottone presinaptico e la risposta a livello postsinaptico è di 0,5-5
millisecondi. Tale intervallo di tempo è definito ritardo sinaptico.
L’unione del neurotrasmettitore al recettore innesca una serie di risposte nella cellula postsinaptica:
-molti neurotrasmettitori generano risposte rapide e di breve durata aprendo un canale ionico
chimicamente regolato, il che porta al passaggio di ioni tra la cellula e il LEC e si determina una variazione
del potenziale di membrana (potenziale sinaptico veloce, EPSP e IPSP);
-alcuni neurotrasmettitori innescano risposte lente e durature attivando sistemi di secondi messaggeri.
Queste risposte comprendono sia l’apertura che la chiusura di canali ionici, sia la modificazione di proteine
cellulari esistenti e la regolazione della sintesi di nuove proteine.
I recettori postsinaptici hanno il ruolo di:
- riconoscere il neurotrasmettitore
- attivare i rispettivi effettori
• Si
dividono in due classi principali: ionotropi e metabotropi
Recettori ionotropi
il recettore è un canale ionico
sono recettori ionotropi: nAChR, GABAA, glicina, NMDA, AMPA, kainato, P2X
azione rapida (ms)
Recettori metabotropi
Il recettore metabotropo non è un canale. E’ una proteina con 7 α-eliche transmembranali,
attiva una proteina G che a sua volta attiva altri effettori (canali e/o secondi messaggeri)
Sono recettori metabotropi: muscarinici (mAChR), GABAergici (GABAB), adrenergici
(α-AR, β-AR), glutamatergici (mGluR), dopaminergici (D1-D5), purinergici (P2Y),
serotoninergici (5-HT), neuropeptidergici (µ, δ, κ oppioidi, …)
Azione lenta (100 ms-100 s
La proteina G attivata
dal recettore, attiva
(o chiude) direttamente i canali
ionici.
La proteina G, attivata
dal recettore, attiva (o inibisce)
enzimi che producono secondi
messaggeri che, a loro volta
attivano o chiudono canali
ionici.
Tutti i recettori adrenergici sono collegati a proteine G.
α1
Si avrà un aumento della velocità della depolarizzazione spontanea ed una diminuzione
del livello di ripolarizzazione per cui la soglia per l’insorgenza del potenziale d’azione
viene raggiunta più rapidamente.
La velocità della depolarizzazione spontanea diminuisce e si avrà una iperpolarizzazione
della membrana, con conseguente allontanamento del potenziale di membrana dal livello
di soglia per l’insorgenza del potenziale d’azione.
SINAPSI ECCITATORIE
Funzionano in modo tale da portare il potenziale della membrana postsinaptica
al valore più vicini al valore soglia in modo tale da generare un potenziale
d’azione
SINAPSI INIBITORIA
Funziona in modo tale da iperpolarizzare
la membrana del neurone postsinaptico o
da stabilizzarla al valore di riposo
Un neurone riceve comunicazioni da centinaia o migliaia di neuroni; su di esso si genera pertanto
una convergenza di imput
L’integrazione sinaptica operata dal neurone fa sì che quando la sommazione dei potenziali postsinaptici
eccitatori prevale su quelli inibitori ed è in grado di portare il potenziale di membrana del monticolo
assonale al valore soglia, nasce un potenziale d’azione.
Acetilcolina
Aminoacidi: glicina – acido γ-aminobutirrico
(GABA) – glutamato - aspartato
Amine biogene: noradrenalina – adrenalina –
dopamina – serotonina - istamina
Peptidi neuroattivi
Neurotrasmettitori peptidici
(più di 100 peptidi, composti da 3 a 30 amminoacidi)
• molecole costituite da un numero variabile di aminoacidi (3-36)
• contenuti in vescicole di dimensioni maggiori
• sintetizzati come pre-proteine del reticolo endoplasmatico rugoso dove
viene rimossa la sequenza segnale. La pre-proteina risultante attraversa
l’apparato di Golgi e viene immagazzinata in vescicole. All’interno delle
vescicole si completa la formazione del peptide: scissione proteolitica,
modificazione delle estremità del peptide, glicosilazione, fosforilazione,
formazione dei ponti disolfuro.
NO è un trasmettitore non
convenzionale
che
viene
sintetizzato dalla ossido nitrico
sintasi
(NOS)
in
seguito
all’aumento di calcio nella cellula
postsinaptica.
Questo
gas
lipofilo a emivita breve diffonde
attraverso
la
membrana
presinaptica
e,
attraverso
l’attivazione di cGMP, modula la
liberazione
di
neurotrasmettitore dal bottone
sinaptico. In tal modo si genera
un segnale sinaptico retrogrado
che contribuisce alla plasticità
sinptica.
Sinapsi colinergiche: neurotrasmettitore Acetilcolina
L’ACh è il neurotrasmettitore usato da tutti gli assoni motori che originano
dal midollo spinale, dai neuroni autonomi pregangliari, dalle fibre
parasimpatiche postgangliari e dai neuroni dei gangli della base implicati nel
controllo del movimento.
Per le sinapsi colinergiche (acetilcolina) esistono due tipi di recettori:
muscarinici.
nicotinici
e
Il recettore nicotinico è esso stesso il canale per gli ioni.
Il recettore muscarinico (o metabotropo) al momento del legame con il
neurotrasmettitore scatena una cascata di reazioni chimiche, che ad opera di un
mediatore portano infine all’apertura dei canali per gli ioni
Glutammato
principale neurotrasmettitore eccitatorio del sistema nervoso centrale
•Tre tipi di recettore:
AMPA (Na+, K+) α-amino-3-idrossi-5-metil-4-isoxazolo propionato
NMDA (Na+, K+, Ca2+) N-metil-D-aspartato
kainato (Na+, K+)
Gli ioni Mg2+ ostruiscono in modo non competitivo il canale del
recettore per l’NMDA, in maniera da impedire la comparsa di
una corrente ionica anche in seguito al legame con il
glutammato.
Se il potenziale di membrana viene leggermente depolarizzato
da una sinapsi eccitatoria dotata di un recettore per l’AMPA,
diminuiscono le forze di legame che agiscono su Mg2+, il
blocco da Mg2+ viene rimosso e si permette una corrente di
entrata di ioni Na+ e Ca2+ nella cellula. Lo ione Ca2+ può
fungere da secondo messaggero ed essere implicato in altri
fenomeni quali i processi di memorizzazione.
GABA: viene sintetizzato dal glutammato mediante una decarbossilasi specifica
presente solo in certi neuroni del SNC.
-si ritrova nelle cellule dei gangli della base, nelle cellule di Purkinje del
cervelletto, negli interneuroni spinali
-funziona come neurotrasmettitore inibitorio
-è il neurotrasmettitore più diffuso nel cervello
-due diversi recettori GABAA e GABAB:
il GABAA è un canale per il Cl- , si assiste quindi ad una corrente di entrata di Clcon conseguente iperpolarizzazione e quindi formazione di un IPSP. I narcotici
barbiturici e i tranquillanti benzodiazepine (Valium) potenziano l’effetto
inibitorio dei recettori GABAA.
il recettore GABAB apre i canali per gli ioni K+ mediante le G-protein.
-l’effetto del GABA viene neutralizzato dal riassorbimento dello stesso
mediatore da parte della terminazione presinaptica e da parte delle cellule della
glia
Il recettore GABAA
Picrotossina
(antagonista)
Modulazione del GABAA
barbiturico
benzodiazepina
• sito di legame per benzodiazepine e barbiturici (ansiolitici), che potenziano l’effetto
inibitorio del GABA.
• il potenziale inibitorio è più ampio e persiste più a lungo in presenza di ansiolitici.
GABA
GABA (in presenza di barbiturico
o benzodiazepina)
20 mV
Il recettore GABAB è un recettore metabotropo (il IPSP si induce mediante
l’apertura di un canale per gli K+.)
Ammine biogene: catecolamine (dopamina, noradrenalina, adrenalina)
serotonina
istamina
Dopamina, noradrenalina e adrenalina sono catecolamine che hanno in comune la stessa via biosintetica
che parte dalla tirosina:
tirosina viene convertita in L-dopa dalla tirosina idrossilasi
L-dopa è convertita in dopamina da una decarbossilasi
nei neuroni noradrenergici la dopamina viene trasformata in noradrenalina ad opera della dopamina βidrossilasi
Le cellule cromaffini della midollare del surrene aggiungono un gruppo metilico alla noradrenalina
formando adrenalina.
La dopamina si trova nei nuclei basali e tronco encefalici, i neuroni
della sostanza nera costituiscono una via discendente dopaminergica
diretta allo striato
I recettori per la dopamina agiscono mediante G-protein e l’effetto
postsinaptico può essere eccitatorio o inibitorio.
Gioca un ruolo fondamentale nel controllo motorio e posturale e nelle
patologie di questi sistemi(morbo di Parkinson). E’ importante anche in
circuiti che presiedono al controllo del comportamento e delle
emozioni. Alterazioni del sistema dopaminergico sono implicate in vari
disturbi psichiatrici.
Nel SNP la noradrenalina e l’adrenalina sono i principali neurotrasmettitori dei neuroni simpatici
postgangliari. Anche nel SNC per modulare i processi di acquisizione delle esperienze di apprendimento,
nell’elaborazione di stimoli sensoriali, nella regolazione del sonno, nell’inibizione di dolori endogeni
I recettori per le catecolamine sono 4, α1, α2, β1 e β2
Agiscono mediante secondi messaggeri e l’effetto postsinaptico può essere eccitatorio o
inibitorio.
Possibili effetti, agonisti o antagonisti, di sostanze psicoattive (farmaci o droghe) su una
sinapsi chimica
• Molti farmaci, tossine o patologie esercitano i loro effetti alterando le diverse fasi della
trasmissione sinaptica
• Questi effetti sono esercitati attraverso:
1) alterazione del rilascio di neurotrasmettitore
2) alterazione dell’interazione neurotrasmettitore-recettore
3) alterazione della rimozione del neurotrasmettitore dallo spazio
intersinaptico
4) sostituzione
di un neurotrasmettitore
mancante
1- Alterazione
del rilascio
Tetano e botulismo
• le tossina tetanica (TeNT) e le tossine
botuliniche (BoNT) sono proteasi che
bloccano la fusione vescicolare. Distruggono
il complesso SNARE, riducono il rilascio di
ACh e determinano una riduzione dello stato
di contrazione del m. scheletrico.
vescicole
• la TeNT blocca il rilascio vescicolare di glicina dalle sinapsi inibitorie che controllano
l’attività dei motoneuroni spinali. I motoneuroni vengono permanentemente stimolati e
producono le tipiche contrazioni tetaniche dei m. scheletrici (paralisi spastica).
• le BoNT bloccano il rilascio vescicolare di ACh della giunzione neuromuscolare riducendo
l’attività elettrica e la forza di contrazione muscolare (paralisi flaccida).
2- Alterazione dell’interazione
neurotrasmettitore-recettore
• alcune terapie di patologie neurodegenerative si basano sull’uso di antagonisti recettoriali
(molecole che si legano reversibilmente al recettore bloccando l’azione del
neurotrasmettitore,)
Schizofrenia
• nella schizofrenia alcune aree
neuronali rilasciano quantità eccessive di
dopamina
agonistarecettore
• si cura con farmaci antipsicotici:
cloropromazina (Thorazine) e
aloperidolo (Haldol) che riducono i
sintomi bloccando i recettori della
dopamina
• altre terapie fanno uso di molecole che favoriscono il legame del neurotrasmettitore al
suo recettore, potenziandone l’azione.
Ansia
• le benzodiazepine (diazepam, Valium) sono ansiolitici che agiscono sui recettori
GABAA facilitando l’interazione del GABA con il recettore.
• producono un potenziamento dell’azione inibitoria GABAergica.
3- Alterata rimozione del neurotrasmettitore dallo spazio
intersinaptico
Depressione
• la depressione è una malattia neurologica
associata ad una deficienza di serotonina e
noradrenalina a livello del SNC.
• si cura con il Prozac (fluoxetina) che inibisce
il trasportatore del re-uptake (presinaptico) della
serotonina rilasciata
• in questo modo la concentrazione di serotonina
nello spazio intersinaptico e l’attività delle
sinapsi serotoninergiche aumentano.
ACh-esterasi
trasportatore
(re-uptake)
Malattia di Alzheimer
• nell’Alzheimer la perdita di memoria e l’insorgere della demenza è associata ad una forte
perdita di neuroni colinergici e riduzione del numero di recettori nicotinici dell’area cognitiva
pre-frontale con conseguente riduzione di ACh in quell’area
• le terapie più efficaci sono basate sull’uso di anticolinesterasici (tacrina, donepezil,
rivastigmina, galantamina) che aumentano i livelli di ACh nello spazio intersinaptico
riducendo la quantità di neurotrasmettitore idrolizzato dall’ACh-esterasi
Azione delle droghe stimolanti sui terminali assonici catecolaminergici.
Possiamo osservare un terminale noradrenergico sulla sinistra ed un terminale dopaminergico sulla destra.
Sia la NA che la DA sono sintetizzate a partire da tirosina. L’azione di NA e di DA si conclude normalmente
con un loro riassorbimento nel terminale assonico. Cocaina ed anfetamina bloccano tale riassorbimento,
permettendo a NA e DA di restare più a lungo nella fessura sinaptica.
4- Sostituzione di un neurotrasmettitore mancante
Morbo di Parkinson
• il parkinsonismo è causato da una
progressiva distruzione dei neuroni
dopaminergici della sostanza nigra che
innervano neuroni del caudato e del putamen
con conseguente riduzione o mancanza di
dopamina in quelle aree.
• la dopamina è rilasciata da neuroni che
inibiscono i motoneuroni che controllano la
contrazione muscolare scheletrica permettendo
in tal modo una regolazione continua e precisa
del movimento muscolare.
• nel morbo di Parkinson la perdita di inibizione produce tremore a riposo, rigidità
muscolare e in alcuni casi demenza.
• si cura farmacologicamente con la levodopa (L-dopa), un precursore della dopamina,
che è trasportato nell’assone terminale presinaptico dei neuroni dopaminergici ed è usato
come substrato per la sintesi di nuova dopamina.