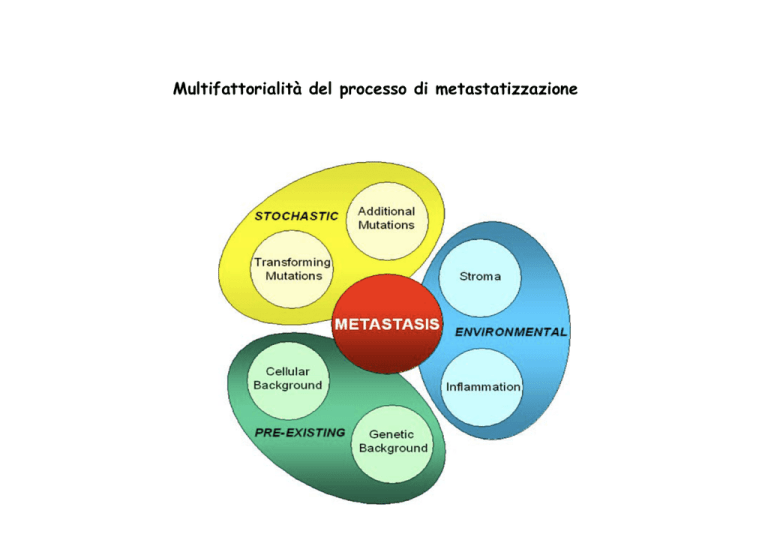
Multifattorialità del processo di metastatizzazione
che non rimargina mai
Albini and Sporn Nature Reviews Cancer 7, 139–147 (February 2007) | doi:10.1038/nrc2067
Tumor Cell Heterogeneity
Lisa Fusetti
3
Tumor Progression and Heterogeneity
• Progressione tumorale: acquisizione di cambiamenti
permanenti nelle caratteristiche di sottopopolazioni
selezionate del tumore.
Tumor Cell Invasion
TRANSIZIONE EPITELIO MESENCHIMA (EMT)
LE CELLULE TUMORALI DEVONO PERDERE I CARATTERI EPITELIALI
E ACQUISIRE I CARATTERI MESENCHIMALI
• Distacco dalle altre cellule tumorali
• Adesione alla matrice extracellulare Proteolisi
della matrice extracellulare
• Motilità e migrazione nella matrice
extracellulare.
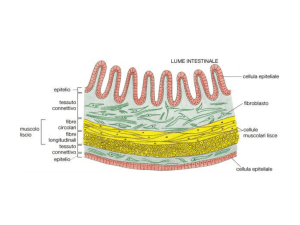
TISSUE EPITHELIUM
La cellula trasformata deve potersi staccare dalle altre cellule epiteliali e non subire
L’inibizione da contatto
microvilli
apical surface
tight junction
adherens junction
gap junction
desmosome
basal lamina
cell-matrix adhesion
e.g., focal adhesions
Integrin-dependent function
There Ci sono almeno 5 classi di molecole di adesione(CAMs)
LE CADERINE VENGONO DOWN-REGOLATE DURANTE LA
TRASFORMAZIONE EPITELIO-MESENCHIMA E LIBERANO LA BETA-CATENINA
APC è UN’UBIQUITINA-LIGASI CHE FA DISTRUGGERE LA BETA CATENINA.
QUANDO MANCA, LA BETA CATENINA SI ACCUMULA E VA NEL NUCLEO
9
Hallmarks of Cancer Cells
• Replicazione
autosufficiente
• Prolungata
sopravvivenza
• Instabilità genetica
• Capace di indurre
neoangiogenesi
• Capace di invasione e
• metastatizzazione
10
Le cellule tumorali nel distretto ematico si ricoprono di
piastrine formando dei microemboli
Lo switch angiogenetico è il frutto di un bilanciamento
Il tumore si adatta ad un ambiente ipossico upregolando il fattore HIF
…..che regola l’espressione di geni importanti
per l’angiogenesi e il movimento
FUNZIONI DI VEGF SULLE CELLULE ENDOTELIALI
• AUMENTA PERMEABILITA’ DEI VASI
formazione di fenestrature nell’endotelio o attivazione di particolari
cellule transendoteliali
• FAVORISCE LA SOPRAVVIVENZA
inibisce l’apoptosi attivando proteine anti-apoptotiche ( bcl2 ) e
inibendo le caspasi
• AUMENTA LA PROLIFERAZIONE
attiva la via mediata da PKC
• FAVORISCE L’INVASIONE E LA MIGRAZIONE
induce l’espressione delle MMPs e di uPA che degradano
la
membrana basale
Sembra che VEGF stimoli anche il reclutamento dei progenitori delle
cellule endoteliali (ECP) dal midollo osseo al sito di neovascolarizzazione
del tumore
Infiltrazione: LE CELULE TUMORALI DESPRIMONO
METALLOPROTEASI CHE DEGRADANO LA MATRICE of
ECM
Lisa Fusetti
16
Il taglio proteolitico delle proteine pro-angiogeniche della matrice genera peptidi anti-angiogenici
Endostatin
Tumstatin
Arresten
Canstatin
Endorepellin
………….che sono:
18
IL TGF BETA è UN’ARMA
A DOPPIO TAGLIO
La perdita della
segnalazione tramite
TGFβ contribuisce alla
anormale proliferazione
cellulare e alla malignità
19
• IL TGFBETA FAVORISCE LA
TRANSIZIONE EPITELIO MESENCHIMA:
FA TRASCRIVERE GLI INIBITORI DELLE
CADERINE
Lisa Fusetti
20
FIBROBLASTI ATTIVATI DAL TUMORE
TGF-β e PDGF sono induttori della DESMOPLASIA (Formazione di
tessuto fibroso; in particolare riferita ai carcinomi in cui le
cellule parenchimali stimolano la formazione di uno stroma
ricco di collagene.) attraverso i loro effetti sui fibroblasti stromali.
• Il TGF-β induce chemiotassi dei fibroblasti ed il loro
transdifferenziamento in MIOFIBROBLASTI.
• Il PDGF induce proliferazione e differenziamento dei fibroblasti in
miofibroblasti o meglio in PROTO-MIOFIBROBLASTI.
CAFs (fibroblasti attivati dal cancro)
PDGF
TGF-ß
Sono identificati
immunocitochimicamente in base
all’espressione di diversi
markers :
• α-SMA (smooth muscle actin)
• VIMENTINA
• DESMINA
• FAP (Fibroblast activation
protein)
CAFs
NELLA PROGRESSIONE DEL TUMORE
I miofibroblasti…
• Up-regolano l’espressione di
SERINE-PROTEASI e MMPs
• Esprimono un range di fattori di
crescita (GF) e CITOCHINE che
promuovono la sopravvivenza delle
cellule tumorali come pure la loro
migrazione ed invasione
• Contribuiscono alla generazione del
microambiente promuovente la
progressione del tumore mediante
l’espressione di GFs che attivano
ulteriormente lo stroma tumorale
attraverso la stimolazione
dell’angiogenesi ed il reclutamento
di cellule infiammatorie
• Secernono componenti della ECM
pro-migratori come la TENASCINAC
23
AGENTI PRO-INVASIVI SECRETI DAI MIOFIBROBLASTI
• I miofibroblasti secernono fattori pro-invasivi come TNC e SF/HGF,
ognuno dei quali necessario ma non sufficiente per la stimolazione
dell’invasione.
• Tali agenti cambiano il morfotipo delle cellule tumorali che da
rotondeggianti diventano allungate e con estensioni cellulari che
facilitano la loro invasione.
• Il morfotipo rotondeggiante è caratterizzato da un’intensa attivazione
della via RhoA/Rock.
• Il morfotipo allungato invasivo è caratterizzato da un’intensa
attivazione della via Rac e bassa RhoA/Rock.
Tumor Cell Invasion
• Distacco dalle altre cellule tumorali
• Adesione alla matrice extracellulare Proteolisi
della matrice extracellulare
• Motilità e migrazione nella matrice
extracellulare.
The Integrin Family of ECM Receptors
ECM
α
β
Extracellular
Adhesion
out
in
Intracellular Signaling
§ Transmembrane, heterodimeric cell surface proteins, consisting of
one α and one β subunit.
§ Primarily cell adhesion molecules, recognizing protein components of
the extracellular matrix (ECM).
§ Regulate multiple intracellular signal transduction pathways leading to
proliferation, differentiation, migration, and survival.
26
The Integrin Family of Receptors
Vitronectin
Fibronectin
Various genetic data identify unique functions for each integrin.
ICAM
VCAM
Regulation of Integrin Adhesion and Signaling
1.
2.
Regolazione Outside-In
-L’integrina “Active” lega la ECM (sequenze RGD) e trasmette il
segnale intracellulare.
3.
Regolazione Inside-Out
-Gli agonisti extracellulari (fattori di crescita, citochine, etc.)
stimolano segnali intracellulari che “attivano” le funzioni di attacco
delle integrine..
- La maggior parte delle integrine sulla superficie cellulare sono
inattive.
- Anticorpi ingegnerizzati distinguono “active” da “inactive”.
Model for Inside-Out Integrin Activation by Talin
Signaling
Inactive
Active, Dimer
Signaling
Active, Multimerization
β subunit cytoplasmic dimerization
The β subunit cytoplasmic sequence recruits intracellular effector proteins, leading to the activation of miultiple signaling cascades.
αvβ6
Un membro della famiglia di molecole chiamate
integrine
-…che integrano l’esterno con l’interno della
cellula
- αvβ6 è espressa soltanto dalle cellule epiteliali
- Il livello di αvβ6 aumenta nei cheratinociti
durante il riparo delle ferite.
Wound repair in normal skin
Epidermis
Basement Membrane
Dermis
Lisa Fusetti
Wound keratinocytes turn on
new molecules for movement
and enzymes for repair 31
Nella ferita I cheratinociti
aumnetano l’espressione di
αvβ6 per riparare la pelle.
Ma-quando il riparo è
completo, l’integrina
scompare
Che cosa succede di αvβ6
nel carcinoma squamoso
della pelle?
Squamous cell carcinoma della
pelle si comporta come una
ferita che non rimargina mai
Which molecules do SCC use for invasion?
αvβ6
Quali sono le caratteristiche protumorigeniche dell’integrina αvβ6?
1)Aumenta la migrazione
2) Aumenta la produzione di enzimi di
degradazione
3) Aumenta
l’invasione
How
can we prevent
the invasive process?
L’infiammazione
contribuisce allo sviluppo di un tumore
La migrazione delle cellule tumorali ricorda quella dei leucociti durante l’infiammazione
Lisa Fusetti
35
Invasione della membrana basale
• Componenti della matrice
extracellulare:
– Type IV collagen, laminin,
proteoglycans
• Le cellule trasformate (e
quelle dello stroma) secernono
delle proteasi:
•
Plasmin
•
Urokinase-type plasminogen
activator
•
Matrix metalloproteinases
(MMPs)
Matrix Metalloproteinases
(MMPs)
• MMPs – FAMIGLIA DI PROTEASI ZINCO-DIPENDENTI
• TIMPs – INIBITORI TISSUTALI DELLE METALLOPROTEASI
• Il bilanciamento tra MMPs e TIMPs è regolato e si
disregola nei carcinomi
MMPs
Increased
invasive capacity
TIMPS
Infiltration: Migration
Migrazione e metastasi
• Modello identico ai leucociti circolanti
e cellule staminali utilizzati per
l’homing in organi specifici
• Meccanismo molecolare:
– Chemochine – recettori accoppiati alle
proteine G
– CCR4/CXCL12
Model of Chemokine Regulation of Breast-Cancer
Metastasis
Murphy, P. M. N Engl J Med 2001;345:833-835
40