FS2 - Studio delle proprietà antiossidanti delle ficocianine in lievito, estrazione
delle ficocianine da Arthrospira platensis (Spirulina) e cromatografia a
scambio ionico di amminoacidi
Studio delle proprietà antiossidanti delle ficocianine in lievito
Difficoltà
Obiettivi didattici
Dimostrare che la ficocianina C estratta da Arthrospira platensis è in grado di
proteggere cellule di lievito dal danno indotto dal perossido di idrogeno.
Prerequisiti
Lieviti, radicali liberi e antiossidanti.
Descrizione
La maggior parte degli antiossidanti di provenienza alimentare con attività più o meno
marcata si trova in cibi di origine vegetale come frutta e verdura. I cianobatteri e in
particolare l’Arthrospira platensis, meglio nota come spirulina, contengono pigmenti
caratterizzati da potere antiossidante e possono quindi essere utilizzati come
integratori alimentari.
La spirulina contiene le ficocianine (di colore azzurro) che, insieme alle ficoeritrine (di
colore rosso), costituiscono le ficobiline, i pigmenti fotosintetici caratteristici
dei cianobatteri. Le ficocianine hanno una struttura molecolare lineare, analoga a
quella di un anello porfirinico aperto, perciò molto simile a quella della bilirubina e
dei pigmenti biliari; così come le cianoficine, la clorofilla, i caroteni, i tocoferoli, l'acido
ascorbico e i composti fenolici, le ficocianine sono potenti antiossidanti alimentari,
utilizzati in alte concentrazioni in alcuni integratori alimentari.
E’ stato stimato che le ficocianine possiedono un'efficacia antiossidante che supera di
40 volte quella dell’acido ascorbico (vitamina C) e dei tocoferoli (vitamina E). Sono in
studio anche le proprietà antiinfiammatorie di queste molecole.
Nell’esperimento proposto l’attività antiossidante delle ficocianine viene valutata in
cellule di lievito. Una coltura di Saccaromyces cerevisiae viene trattata con perossido
d’idrogeno che è causa di danno cellulare. Gli studenti valuteranno la protezione dal
danno in presenza di un estratto di ficocianina e di Vitamina C, usata come controllo.
Estrazione delle ficocianine da Arthrospira platensis (Spirulina)
Difficoltà
Obiettivi didattici
Osservare al microscopio ottico l’Arthrospira platensis ed estrarre la ficocianina C (cPC).
Prerequisiti
Struttura della cellula procariotica, caratteristiche e struttura generale delle proteine,
concetti fondamentali della fotosintesi e funzioni dei pigmenti fotosintetici.
Descrizione
L’Arthrospira platensis, meglio nota come spirulina, è un cianobatterio che vive in laghi
salati caratterizzati da una concentrazione di sale maggiore di 30 g/l e un pH tra 8.5 e
11, che ne favoriscono la crescita, specialmente dove sono elevati i livelli di radiazioni
solari come nelle zone tropicali.
La spirulina vista al microscopio ottico presenta cellule impilate l’una sull’altra a
formare lunghi filamenti (detti tricomi). Le singole cellule sono circondate da una
membrana citoplasmatica e da una parete cellulare pluristratificata composta da uno
strato di peptidoglicano (o mureina) e da uno più esterno di lipopolisaccaridi. Proprio
per questo tipo di organizzazione della parete cellulare, i cianobatteri sono solitamente
considerati batteri Gram-negativi.
La spirulina contiene elevate quantità di proteine: tra il 59 e il 65% del peso secco.
Quantità maggiori a quele che si ottengono dalle fonti vegetali comuni come la soia
(35%), le arachidi (25%) o il grano (8-10%). A causa dell’assenza della cellulosa nelle
pareti cellulari la maggior parte delle proteine viene digerita e assimilata in breve
tempo. Nella spirulina sono presenti numerose vitamine quali B12, C, D, E, acido folico,
grandi quantità di beta carotene che viene convertito in vitamina A, ferro e calcio. Per
tali motivi viene utilizzata come integratore alimentare nei paesi in cui è elevata la
malnutrizione infantile.
La spirulina contiene ficobiline di colore azzurro (ficocianina e alloficocianina) e di
colore rosso (ficoeritrina), che spesso mascherano il colore verde della clorofilla. Le
ficobiline, come altri pigmenti accessori fotosintetici contenuti nella spirulina quali
betacarotene e xantofille, hanno la funzione di captare radiazioni luminose di
lunghezza d’onda diversa da quella assorbita dalla clorofilla e di trasmetterle a
quest’ultima per lo svolgimento del processo fotosintetico.
In questa esperienza di laboratorio gli studenti potranno avvicinarsi alle tecniche di
estrazione di una proteina. I passaggi previsti dal protocollo sono tre: lisi delle cellule
del cianobatterio, centrifugazione e precipitazione della proteina.
Cromatografia a scambio ionico di amminoacidi
Difficoltà
Obiettivi didattici
Separare tramite cromatografia a scambio ionico alcuni amminoacidi da una miscela
complessa.
Prerequisiti
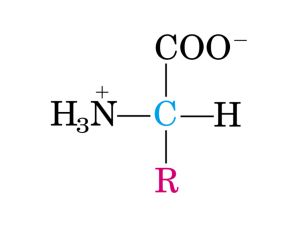
Struttura degli amminoacidi, concetti generali di cromatografia e pH.
Descrizione
La cromatografia è un metodo che permette la separazione dei componenti di una
miscela in base alle loro caratteristiche chimico-fisiche. Essa si basa sulla differente
migrazione di una soluzione (fase mobile) che contiene le molecole da separare
attraverso un mezzo (fase stazionaria) generalmente impaccato in una colonna.
Ogni soluto passa nella fase mobile tanto più rapidamente quanto meno fortemente
interagisce con la fase stazionaria.
Le tecniche cromatografiche possono essere usate a scopo preparativo, per separare
materiali in gran quantità, o a scopo analitico, per isolarne piccole quantità. I metodi
cromatografici sono classificati sulla base della natura delle interazioni che si
instaurano tra le molecole da separare e la fase stazionaria.
Il presente protocollo prevede l’isolamento e la rilevazione di alcuni amminoacidi da
una miscela utilizzando la cromatografia a scambio ionico.
Tale tecnica permette di separare i componenti di una miscela sulla base delle cariche
presenti sulle molecole in grado di interagire con lo scambiatore di ioni. Lo
scambiatore di ioni è costituito da una matrice, che può essere una resina sintetica,
una cellulosa o un destrano, che porta legati covalentemente dei gruppi in grado di
ionizzarsi in uno ione fisso, che rimane attaccato alla matrice, ed in un contro-ione
(Na+ o Cl-), che può essere scambiato con qualsiasi altro ione di egual segno, presente
in soluzione. Una volta applicato il campione sulla colonna, l’eluizione differenziale dei
componenti si otterrà modificando o la forza ionica o il pH (talvolta entrambi) del
tampone, ossia effettuando un’eluizione in gradiente.
L’esperimento permetterà di separare una miscela di amminoacidi quali Fenilalanina,
Prolina e uno zucchero su resina cationica.
Gli eluati, frazionati in diverse provette, saranno fatti reagire con la ninidrina: una
sostanza che si combina con gli amminoacidi dando un colore porpora nel caso della
Fenilalanina o giallo nel caso della Prolina.