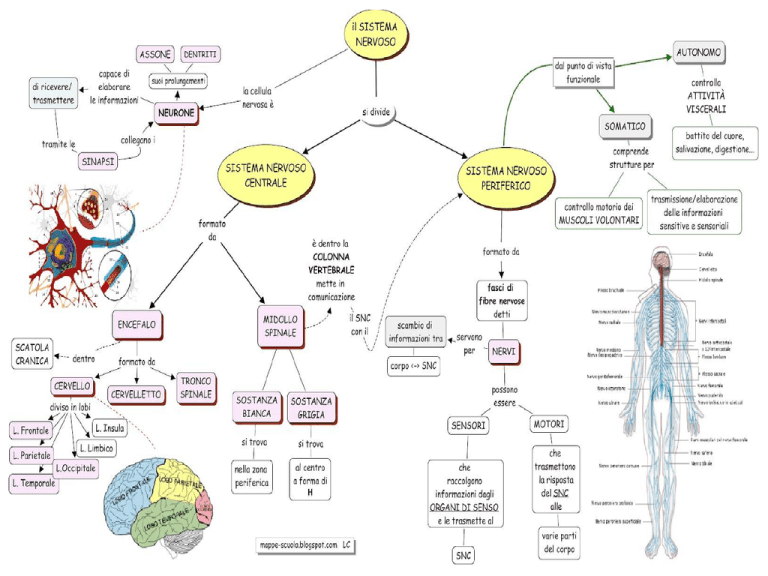
SISTEMA NERVOSO
Il sistema nervoso è la sede dell'assunzione, elaborazione e trasmissione delle informazioni;
in altre parole, assieme al sistema endocrino e immunitario, è un sistema di regolazione
delle funzioni corporee
Il sistema nervoso è un complesso sistema elettrochimico, composto da oltre 1000 miliardi di cellule, che viaggia a 400 km all’ora e che
assorbe il 20% dell’ossigeno dell’organismo
TEORIA DELLA NEUROTRASMISSIONE CELLULARE (primi studi di fisiologia sperimentale metà XIX sec.)
il passaggio dell’informazione tra cellule nervose e tra queste e le rispettive cellule effettrici
(connessioni intercellulari specializzate dette «sinapsi») è mediato dall’azione di una
sostanza chimica definita «neurotrasmettitore o neuromediatore», il quale diffonde nello
stretto spazio delimitato dalla cellula di origine e dalla cellula bersaglio giustapposta e,
attraverso l’interazione con il suo recettore, assicura la trasmissione dell’informazione (si
parla quindi di sinapsi chimica ≠ sinapsi elettrica)
SISTEMA
NERVOSO
PERIFERICO
SOMATICO
CENTRALE
AUTONOMO
SISTEMA NERVOSO CENTRALE
Encefalo e Midollo Spinale formano il sistema
nervoso centrale (SNC) o asse cerebrospinale (o
nevrasse o tubo neurale) che è in grado di
raccogliere, trasmettere e integrare le informazioni.
Custodito
all'interno
della
scatola
cranica
(encefalo) e del canale vertebrale (midollo spinale),
il SNC, viene protetto ulteriormente e nutrito dal
sistema delle meningi, dal liquor cerebrospinale e
dal proprio sistema di vascolarizzazione (barriera
emato-encefalica,
emato-liquorale
e
emato-
retinica)
to be continued…….
SISTEMA NERVOSO PERIFERICO
Il sistema nervoso periferico (SNP) è formato dai nervi cranici o cefalici e dai nervi spinali
(formanti assieme i nervi encefalospinali) e dai relativi gangli
Il sistema nervoso periferico viene suddiviso funzionalmente (non solo) in:
❖ volontario o somatico
❖ involontario o vegetativo o autonomo
Neurotrasmettitori del SNP
•Acetilcolina
•Noradrenalina
•Adrenalina
•Dopamina
•Serotonina
•Istamina
•GABA
•NO
7
I muscoli sono i principali organi effettori del sistema
nervoso (ma non solo!) e attivano il loro sistema
contrattile in risposta ai segnali inviati attraverso le fibre
nervose
Il controllo nervoso della contrazione può essere
volontario o involontario, a seconda del tipo di fibre
muscolari
L’innervazione involontaria riguarda le fibre muscolari
lisce degli organi viscerali e le fibre striate del
miocardio; viene effettuata dal sistema
neurovegetativo e gli effetti sull’organo innervato
possono essere eccitatori o inibitori
L’innervazione volontaria riguarda solo i muscoli
scheletrici ed è effettuata dai motoneuroni, che
collegano il sistema nervoso centrale con le fibre
muscolari. Gli effetti sul muscolo innervato sono
eccitatori
SISTEMA NERVOSO SOMATICO
Il sistema nervoso somatico (SNS) trasporta le informazioni relative ai movimenti e ai sensi
dal sistema nervoso centrale al resto del corpo e viceversa
È formato dalle fibre nervose periferiche che portano le informazioni sensoriali (provenienti
dalla pelle e dagli organi di senso) al sistema nervoso centrale e dalle fibre nervose motorie
che dal sistema nervoso centrale viaggiano verso i muscoli scheletrici
All'interno del sistema nervoso somatico si trovano principalmente due tipi di neuroni:
❖ neuroni sensitivi o afferenti
❖ motoneuroni o efferenti
I neuroni sensitivi portano le informazioni dalla periferia al sistema nervoso centrale
I motoneuroni trasportano invece le informazioni dal cervello e dal midollo spinale alle fibre
muscolari
Il segnale nervoso, rappresentato da impulsi elettrochimici, viaggia lungo i prolungamenti
dei neuroni per essere trasmesso dal cervello o dal midollo spinale alla pelle, agli organi di
senso o ai muscoli e da qui al sistema nervoso centrale
Il termine somatico deriva dalla parola greca soma (corpo)
In effetti il sistema nervoso somatico si fa carico proprio di aspetti prettamente fisici,
essendo responsabile:
❖ dei movimenti dei muscoli volontari
❖ del processamento delle informazioni sensoriali associate a stimoli esterni, incluse
quelle legate all'udito, al tatto e alla vista
Il sistema nervoso somatico è inoltre associato ai
movimenti involontari anche detti arco riflesso
spinale: in questo caso i muscoli si muovono
involontariamente, senza ricevere un comando dal
cervello
Questo fenomeno si realizza quando una via
nervosa si connette direttamente al midollo spinale
(l'istinto a ritirare la mano dopo aver toccato un
oggetto bollente o il movimento involontario della
gamba quando viene stimolato un punto specifico
del ginocchio)
Il riflesso nervoso, definito arco riflesso, è una reazione del sistema nervoso
centrale a stimolazioni esterne o interne (rilevate tramite i recettori sensoriali), atta a
modificare lo stato di contrazione muscolare o di secrezione ghiandolare (reazione
motoria, vasomotoria o ghiandolare) Rappresenta il meccanismo più semplice con cui il
sistema nervoso può dare una risposta pronta e adeguata a determinati stimoli
I riflessi interessano sia il sistema nervoso volontario che quello vegetativo
Meccanismo di base, elementare, di un arco riflesso:
recettore sensoriale > via nervosa afferente o sensitiva >
centro nervoso (posto nel sistema nervoso centrale) > via
nervosa efferente o motoria > effettore (muscolo o ghiandola)
I riflessi nervosi vengono suddivisi in:
❖ semplici (detti anche incondizionati o congeniti)
❖ complessi (o condizionati o acquisiti)
Quando i riflessi nervosi hanno come centro nervoso
il midollo spinale, si definiscono riflessi spinali
(monosinaptici o polisinaptici)
gli archi riflessi monosinaptici sono principalmente adibiti al controllo dei movimenti
gli archi riflessi polisinaptici (interneuroni) sono in genere determinati da stimoli dolorifici
GIUNZIONE NEURO-MUSCOLARE
struttura di collegamento tra terminale del motoneurone
e fibra muscolare scheletrica (SINAPSI CHIMICA)
Gli assoni dei motoneuroni fuoriescono dalle corna
ventrali del midollo spinale o da alcuni nuclei motori di
nervi cranici, e terminano, senza far sinapsi intermedie,
sulla fibra muscolare formando un tipo di sinapsi molto
specializzata, detta giunzione neuromuscolare
La terminazione assonale è rigonfia (bottone sinaptico)
di neurotrasmettitore (Ach) ed entra in contatto con
una regione specializzata, ricca di recettori, della fibra
muscolare (placca motrice)
Gli effetti sul muscolo innervato sono eccitatori
Ciascun motoneurone innerva più fibre muscolari,
formando insieme un’unità motrice
MECCANISMO DELLA TRASMISSIONE NEURO-MUSCOLARE
Una volta che un impulso nervoso proviene alla giunzione, l’Ach viene
estrusa dalle vescicole negli spazi sinaptici.
Ciò è dovuto a un flusso di ioni calcio che dal liquido extracellulare
entrano nelle membrane dei terminali al momento dell’arrivo del
potenziale di azione (apertura dei canali del calcio voltaggio-dipendenti).
La messa in libertà del mediatore avviene in modo rapido, in meno di 1
millisecondo, e si ritiene che per ogni impulso si liberino un milione di
molecole di Ach a livello di ogni terminazione nervosa.
L’Ach liberata viene rapidamente inattivata per distruzione ad opera della
acetilcolinesterasi, ma il tempo per il quale essa rimane a contatto con la
membrana della fibra muscolare, è quasi sufficiente ad eccitarla, mentre
la rapida rimozione dell’Ach impedisce la rieccitazione della fibra, una
volta che si sia esaurito il primo potenziale d’azione.
L’acetilcolina viene idrolizzata dalla acetilcolinesterasi in colina e acetato:
la colina viene conservata tramite riassunzione attiva all’interno della
terminazione nervosa, dove viene riconvertita in acetilcolina dall’enzima
colin-acetiltranferasi
L’Ach si fissa a recettori (detti nicotinici) della membrana muscolare, con
conseguente aumento della permeabilità agli ioni sodio con loro
ingresso all’interno della cellula, che come risultato ha una
modificazione locale (cioè a livello della placca motrice)del potenziale di
membrana, che aumenta di circa 50-75 millivolt, detto potenziale di
placca
i recettori nicotinici sono recettori
associati a canale ionico
SISTEMA NERVOSO AUTONOMO
Il sistema nervoso autonomo (SNA), è quell’insieme di cellule e fibre che innervano gli organi
interni e le ghiandole, controllando le cosiddette funzioni vegetative, ossia quelle funzioni
che generalmente sono al di fuori del controllo volontario (meglio dire cosciente)
Il SNA è parte del sistema nervoso periferico ed ha la funzione di regolare l’omeostasi
dell’organismo. Il suo sistema neuromotorio non è influenzabile dalla volontà. Opera con
meccanismi appunto autonomi, relativi a riflessi periferici, sottoposti al controllo centrale
(Ipotalamo)
La comprensione di questo sistema ha un’importanza profonda nella pratica clinica
Esempio: nel 1960 la sopravvivenza dei pazienti che andavano incontro a infarto miocardico non
superava i cinque anni, soprattutto perché era molto difficile riuscire a controllare l’ipertensione che
spesso si accompagna a questa patologia, essendone spesso anche la causa primitiva. Oggi, molti
pazienti reduci da un infarto riescono a condurre una vita del tutto normale. Il cambiamento, in termini
di sopravvivenza e qualità di vita, è dovuto proprio al fatto che abbiamo imparato a controllare il SNA
mediante l’uso di farmaci e di procedure mediche
COSTITUITO DA PORZIONI ANATOMICAMENTE E FUNZIONALMENTE DISTINTE MA SINERGICHE
(singolarmente composte da una porzione sensitiva, o afferente, ed una motoria, o efferente)
❖ sistema nervoso simpatico o ortosimpatico
❖ sistema nervoso parasimpatico
❖ sistema nervoso metasimpatico o enterico (fibre nervose che innervano i visceri)
Le due principali componenti del sistema nervoso vegetativo (orto e parasimpatico)
scatenano negli organi bersaglio degli effetti in parte contrastanti
In buona sostanza l’ortosimpatico svolge una funzione di stimolazione e reazione (due
sono i termini che sintetizzano questa reazione: combatti o fuggi)
Il parasimpatico svolge una funzione contraria, infatti ha la proprietà di coordinare il riposo
e le fasi digestive
ORGANIZZAZIONE ANATOMICA DELLE EFFERENZE AUTONOMICHE
I centri per il controllo dell’attività autonoma si trovano nell’IPOTALAMO,
il quale è collegato indirettamente con la corteccia cerebrale (attraverso di
esso, la vita affettiva e di relazione può condizionare l’attività vegetativa), BULBO e
PONTE
Le vie efferenti del sistema nervoso autonomo si compongono di due
neuroni: neurone pregangliare e di neurone postgangliare
I corpi cellulari dei neuroni pregangliari si trovano nella colonna grigia
intermedio-laterale del midollo spinale, gli assoni dei postgangliari (detti
fibre postgangliari) vanno a terminare sugli effettori viscerali
Le fibre pregangliari abbandonano il SNC e fanno sinapsi con i neuroni
postgangliari, cioè con i neuroni motori viscerali che si trovano all’interno di
gangli periferici. Tali gangli, che contengono dalle centinaia alle migliaia di
neuroni gangliari, vengono chiamati gangli autonomi
I neuroni postgangliari innervano effettori viscerali quali il muscolo
cardiaco, i muscoli lisci, le ghiandole e il tessuto adiposo
Gli assoni dei neuroni postgangliari vengono chiamati fibre postgangliari,
cioè fibre che partono dai gangli autonomi estendendosi fino agli organi
bersaglio periferici
GANGLIO AUTONOMO
funziona come una corsa a
staffetta Nel ganglio, il primo
staffettista (fibra pregangliare)
passa
il
testimone
(il
neurotrasmettitore) al successivo
corridore (fibra postgangliare),
che poi lo porta al traguardo
(organo bersaglio)
La trasmissione a livello delle giunzioni sinaptiche fra i neuroni pregangliari e
postgangliari, e fra i neuroni postgangliari ed effettori autonomici è mediata da
sostanze chimiche, e più precisamente da acetilcolina (Ach) e noradrenalina (in
minima parte anche da dopamina)
sistema simpatico
sez. toraco-lombare del midollo
spinale
Fibre pregangliari corte, fibre
postgangliari lunghe (azione estesa)
sistema parasimpatico
sez. cranio-sacrale (craniale e sacrale) del
midollo spinale
Fibre pregangliari lunghe, fibre
postgangliari corte
SIMPATICO
Sistema nervoso simpatico
Organizzato in modo da inviare impulsi generalizzati.
Interviene nell’adattamento all’ambiente e nelle
situazioni di stress (pericolo, rabbia, paura…),
pertanto:
-aumenta la frequenza cardiaca
-aumenta la pressione arteriosa
-determina vasocostrizione cutanea e splancnica, e
vasodilatazione muscolare
-causa dilatazione della pupilla e dei bronchioli
-Non è essenziale per la vita se il soggetto viene
mantenuto in un ambiente controllato
23
EFFETTI DELL’ATTIVAZIONE SIMPATICA
L’innervazione simpatica viene tradizionalmente descritta come una componente che
svolge una funzione di attacco o fuga (fight or flight)
Fa capo a reazioni spesso opposte rispetto all’innervazione parasimpatica:
broncodilatazione, vasocostrizione, tachicardia, costrizione degli sfinteri, contrazione della
muscolatura delle vie spermatiche (quindi contribuisce all’eiaculazione)
La componente simpatica decorre con i rami anteriori dei nervi spinali compresi fra C8 e L2
(alcuni testi riportano T1 ed L3)
Le fibre mieliniche pregangliari si portano ai gangli del sistema toraco-lombare; da qui le
fibre postgangliari amieliniche (grigie) si portano ai territori di innervazione
L’innervazione degli organi è composita:
❖ i gangli cervicali innervano la faccia e in parte il cuore
❖ i gangli toracici vanno a innervare la componente polmonare e ghiandolare
❖ le regioni inferiori sono innervate da fibre che fuoriescono da tre gangli prevertebrali
(celiaco, mesenterico superiore e mesenterico inferiore)
CONDIZIONI SPERIMENTALI DI SIMPATECTOMIA
RECETTORI ADRENERGICI
❖ I recettori α1 sono accoppiati a una proteina G con effettore la fosfolipasi C e
producono i loro effetti principalmente grazie al rilascio di Ca2+ intracellulare
(EFFETTO ECCITATORIO)
❖ I recettori α2 sono accoppiati a una proteina Gi (proteina G inibitrice) la quale inibisce
l'azione dell'adenilato ciclasi riducendo pertanto la formazione di cAMP inibendo i
canali del calcio
(EFFETTO INIBITORIO)
❖ I recettori β1 sono accoppiati a Proteine G stimolatrici che innalzano il livello di cAMP
attivando delle proteinchinasi che innalzano il livello di calcio intracellulare
(EFFETTO ECCITATORIO)
❖ I recettori β2 sono accoppiati a una proteina G stimolatrice e attivatrice della
Proteinchinasi A che ha come substrato la chinasi della catena leggera della miosina
(MLCK), generando così un rilassamento muscolare (liscia bronchiale e vasale)
(EFFETTO ECCITATORIO)
POSIZIONE E FUNZIONE DEI RECETTORI ADRENERGICI
α1: è un recettore di tipo eccitatorio postsinaptico presente in prevalenza sulla muscolatura liscia dei
piccoli vasi (resistenze periferiche), la cui stimolazione genera contrazione della muscolatura liscia
vasale generando un aumento della pressione. Presente anche sulla muscolatura del sistema
urogenitale e degli sfinteri (sembra inoltre che questo recettore abbia dei ruoli importanti per il
controllo dell'umore e del comportamento)
α2: è un recettore presinaptico, presente sulle terminazioni nervose, è deputato alla regolazione della
secrezione di neurotrasmettitori catecolaminergici: la sua attivazione determina una diminuzione della
produzione di noradrenalina - feedback negativo. (il suo antagonista yohimbina è utilizzato per la cura
dell'eiaculazione tardiva)
β1: è un recettore di tipo eccitatorio, importantissimo per l'attività cardiovascolare, è principalmente
presente a livello cardiaco e renale, la sua stimolazione genera a livello cardiaco un effetto inotropo e
cronotropo positivo mentre a livello renale stimola la secrezione di renina da parte delle cellule
juxtaglomerulari
β2: è un recettore di tipo eccitatorio accoppiato a proteina Gs come tutti i beta recettori; è presente a
livello della muscolatura liscia di alcuni apparati: muscolatura liscia bronchiale, muscolatura liscia
gastrointestinale ed è inoltre presente sulla muscolatura liscia di coronarie e grandi vasi che irrorano la
muscolatura scheletrica. L'attivazione di questo recettore genera quindi il rilassamento della
muscolatura liscia bronchiale, gastrointestinale e dei grandi vasi periferici. Inoltre è importante per il
metabolismo glucidico conducendo ad un innalzamento della glicemia. (questo recettore sembra essere
il mediatore degli effetti di vasodilatazione ortosimpatica che si evidenziano al livello del tessuto
muscolare scheletrico)
β3: è un recettore di tipo eccitatorio, presente soprattutto a livello del tessuto adiposo. Qui attiva
l'enzima lipasi che libera acidi grassi dai trigliceridi. Eventuali agonisti di questo recettore potrebbero
essere target terapeutici potenziali per la cura dell'obesità
Muscolatura vasale
PARASIMPATICO
Sistema nervoso parasimpatico
Organizzato per inviare impulsi ben definiti e
localizzati. Implicato nella conservazione
dell’energia e della funzionalità degli organi nei
periodi di bassa attività, pertanto:
-rallenta la frequenza cardiaca
-diminuisce la pressione arteriosa
-Stimola motilità e secrezione gastrointestinale
-Facilita l’assorbimento delle sostanze nutritive
-Protegge la retina dalla luce eccessiva
-Favorisce le funzioni della vescica
37
EFFETTI DELL’ATTIVAZIONE PARASIMPATICA
Il parasimpatico è dato da quella parte del sistema nervoso autonomo che provvede a
funzioni viscero-sensitive e somato-sensitive oltre a:
❖ broncocostrizione, peristalsi della muscolatura gastroenterica, eccitosecrezione di
ghiandole salivari, lacrimali nonché ghiandole extramurarie annesse al tubo digerente
(pancreas e fegato)
❖ interviene nell’innervazione del muscolo detrusore della vescica, la cui contrazione,
accompagnata dal rilassamento del muscolo sfintere liscio della vescica, porta alla
minzione
Le fibre parasimpatiche decorrono in molti nervi cranici quali: nervo oculomotore, nervo
faciale, nervo glossofaringeo, nervo vago. Quest’ultimo (uno dei nervi più lunghi) concorre
all’innervazione viscerale di tutto il tratto digerente fino al colon discendente, del cuore e
dei polmoni, nonché della regione faringo-laringea
Le fibre parasimpatiche per l’innervazione della porzione terminale del tubo digerente e
delle porzioni caudali dell’apparato urinario originano dai nervi S2, S3, S4 ed S5
Al fine della risposta degli organi effettori agli impulsi dei nervi autonomici, è necessario
sapere che la muscolatura delle pareti degli organi cavi è normalmente innervata sia da
fibre noradrenergiche e colinergiche; avremo allora una fase eccitatoria sulla
muscolatura liscia in un caso, ed una fase inibitoria nell’altro caso. Questo processo,
comunque, non deve essere interpretato come unico ed assoluto: se prendiamo l’area
degli sfinteri, questa riceve impulsi eccitatori sia dalle fibre noradrenergiche che da
quelle colinergiche, con la sola differenza che le fibre noradrenergiche agiscono sui
muscoli costrittori degli sfinteri, mentre le fibre colinergiche sui muscoli dilatatori.
Questo esempio ci ricorda, quindi, che non esiste una regola ferrea in relazione a quale
sia il sistema che stimola e quale quello che inibisce
La liberazione di noradrenalina ha la funzione di aumentare l’attività simpatica del
sistema nervoso autonomo, quindi la scarica noradrenergica entra in azione nel
momento in cui si presenta una situazione di emergenza. Questa condizione determina
una midriasi pupillare, aumento del battito cardiaco e pressione arteriosa con relativo
miglioramento dell’irrorazione ematica ai muscoli ed organi vitali, per contro
restringimento dei vasi sanguigni della cute con netta riduzione del sanguinamento delle
ferite. Rinforza lo stato di vigilanza ed innalza la concentrazione di glucosio ed acidi
grassi nel sangue, aumentando in questo modo l’energia
L’azione colinergica favorisce la digestione e l’assorbimento intestinale, ciò dovuto al
fatto che aumenta la secrezione gastrica e la motilità intestinale con rilascio dello
sfintere pilorico. È a causa di ciò che viene chiamata anabolica la componente
colinergica del sistema nervoso autonomo, in contrasto con la fase catabolica, di
pertinenza noradrenergica.
riepilogo dell’organizzazione anatomo-funzionale dei sistemi simpatico e parasimpatico
L’organizzazione di base è costituita da un neurone pre-gangliare e da un neurone postgangliare (mente nel sistema somatico vi è un singolo motoneurone che connette il SNC con la muscolatura scheletrica)
❖ fibre pre-gangliari parasimpatiche e simpatiche: rilasciano acetilcolina, che agisce sui
recettori nicotinici
❖ fibre post-gangliari parasimpatiche: rilasciano acetilcolina, che agisce sui recettori
muscarinici
❖ fibre post-gangliari simpatiche: rilasciano noradrenalina, che agisce sui recettori α o βadrenergici
FIBRE COLINERGICHE e FIBRE ADRENERGICHE
sono neuroni colinergici:
❖ tutti i neuroni pregangliari, sia parasimpatici che simpatici;
❖ i neuroni postgangliari parasimpatici;
❖ i neuroni postgangliari simpatici che innervano le ghiandole sudoripare;
❖ i neuroni postgangliari simpatici che terminano sui vasi sanguigni dei muscoli con
funzione di vasodilatazione
sono neuroni adrenergici:
❖ tutti gli altri neuroni simpatici postgangliari
SISTEMA NERVOSO METASIMPATICO o ENTERICO o INTRAMURALE
Il sistema nervoso enterico (SNE) rappresenta la terza divisione anatomica del SNA
È quella porzione di sistema nervoso che sta dentro la parete dei visceri (costituito da
neuroni i cui corpi cellulari sono localizzati nei plessi intramurali della parete intestinale)
Al sistema nervoso intramurale giungono fibre ortosimpatiche e parasimpatiche del sistema
extramurale
Strettamente connesso con i sistemi simpatico e parasimpatico, possiede capacità
integrative sufficienti da consentire il proprio funzionamento in assenza di informazioni
provenienti dal sistema nervoso centrale (sistema intrinseco «secondo cervello o cervello intestinale»)
Il SNE è organizzato in due principali plessi neuronali:
❖ plesso mienterico (o di Auerbach)
Il plesso mienterico è localizzato tra
❖ plesso sottomucosale (o di Meissner)
muscolare longitudinale più esterno
lo strato
e quello
circolare ed interessa il tratto gastrointestinale in
tutta la sua lunghezza, mentre il plesso
sottomucosale, che interessa solo il tratto
intestinale, è localizzato tra lo strato muscolare
circolare e la sottomucosa
I due plessi mienterico e sottomucosale sono
organizzati a formare un complesso circuito
neuronale comprendente neuroni sensoriali,
interneuroni, motoneuroni, neuroni secretori e
vasomotori che utilizzano come neurotrasmettitori:
Ach, adrenalina, serotonina, purine e peptidi
riepilogo dell’organizzazione delle vie efferenti del sistema nervoso somatico e autonomo
In entrambi i casi si tratta di compartimenti efferenti che trasportano comandi motori
Il SNS controlla i muscoli scheletrici, mentre il SNA controlla gli effettori viscerali
La principale differenza strutturale fra i due sistemi sta nel fatto che nel SNS i motoneuroni
del sistema nervoso centrale esercitano un controllo diretto sui muscoli scheletrici
mentre, nel SNA i motoneuroni del sistema nervoso centrale fanno sinapsi con i
motoneuroni viscerali che si trovano all’interno di gangli i quali, a loro volta, sono quelli
che controllano gli effettori viscerali
Recettore accoppiato a canali ionici
recettore colinergico nicotinico (e gabaergico)
Recettori accoppiati all’adenilato ciclasi (chinasi)
recettore ß-adrenergico e a2-adrenergico
Struttura ed meccanismo d'azione simile a quello dei recettori tirosin chinasici. Al contrario di questi, non hanno attività tirosin
chinasica intrinseca, ma l'attività è mediata da una chinasi cellulare
Recettori accoppiati alla proteina G
(con effettore fosfolipasi C - PLC)
recettore a1-adrenergico e colinergico muscarinico
ACETILCOLINA
NORADRENALINA
L’acetilcolina è fondamentalmente racchiusa in
La noradrenalina è immagazzinata nei bottoni
piccole vescicole sinaptiche chiare, molto
sinaptici dei neuroni che la secernono
concentrata nei bottoni terminali dei neuroni
(vescicole granulate).
colinergici.
La noradrenalina ed il suo metil-derivato, che è
L’arrivo di un impulso ad un bottone sinaptico
l’adrenalina, vengono secrete dalla midollare
aumenta la permeabilità della membrana al
surrenalica, anche se comunque neuroni che
Ca++, e l’afflusso di questo che ne risulta
secernono noradrenalina, dopamina ed
provoca la liberazione di acetilcolina nella
adrenalina sono anche presenti nel cervello
fessura sinaptica mediante un processo di
esocitosi.
Acetilcolina (Ach)
E’ un neurotrasmettitore centrale e periferico
In periferia è il neurotrasmettitore primario
nelle giunzioni neuromuscolari scheletriche,
nel sistema nervoso parasimpatico e nel
sistema simpatico pregangliare
I recettori colinergici sono di due tipi
principali:
Muscarinici (accoppiati a proteine G)
Nicotinici (canali del cloro)
N.B.: i recettori nicotinici muscolari si differenziano dai recettori nicotinici presenti sui gangli, perciò i farmaci
che agiscono su tali recettori devono avere un'azione selettiva, viceversa si rischierebbe di compromettere
l'intera trasmissione simpatica pre-gangliare
56
Noradrenalina (nor-epinefrina)
È un neurotrasmettitore centrale e periferico
In periferia è il neurotrasmettitore primario nel
sistema nervoso simpatico (postgangliare).
I recettori adrenergici sono di due tipi principali:
a (alfa; accoppiati a proteine G)
b (beta; accoppiati a proteine G)
57
Trasmissione adrenergica
1. La nor-adrenalina (NA) viene sintetizzata
nel citosol dei neuroni adrenergici. La
sintesi avviene in più stadi; il precursore è
l’aminoacido tirosina.
2. La NA viene trasportata all’interno di
vescicole (granuli cromaffini), insieme a ATP
(co-trasmettitore)
(Il trasportatore viene inibito dall’alcaloide vegetale reserpina,
che determina deplezione dei depositi di NA (e altre
catecolamine): inibendo il trasporto, la NA rimane nel
citoplasma dove viene metabolizzata dalle MAO)
3.
L’arrivo di un impulso nervoso provoca il rilascio di NA
dalla terminazione nervosa, processo Ca++-dipendente.
Il rilascio di NA dalle vescicole è inibito dalla guanetidina
4.
5.
La NA rilasciata interagisce con i recettori postsinaptici e pre-sinaptici.
La fine del segnale di trasmissione è determinata
dalla ri-captazione (re-uptake) di NA all’interno dei
neuroni (fino 80%). NA viene trasportata all’interno
dei neuroni da un trasportatore definito uptake 1
(trasportatore ad alta affinità). Esiste anche un
trasportatore nelle cellule non neuronali (uptake 2, a
bassa affinità)
(Diversi farmaci inibiscono l’uptake 1 - antidepressivi triciclici, cocaina)
Una parte della NA viene metabolizzata nello spazio
intersinaptico dalle catecol-O-metiltrasferasi (COMT)
• Nel citoplasma del neurone, la NA in parte viene
immagazzinata nelle vescicole pronta per essere
riutilizzata ed una parte viene metabolizzata e
inattivata da enzimi denominati MAO (Mono Amino
Ossidasi). Le MAO metabolizzano anche altre
ammine neurotrasmetitrici (dopamina, serotonina,
adrenalina)
61
CATECOLAMINE
amina + gruppo chimico detto CATECOLO
la noradrenalina è il principale neurotrasmettitore nei neuroni simpatici ……..
adrenalina (epinefrina) e dopamina
Localizzazione dei recettori α1
PRINCIPALE LOCALIZZAZIONE
RISPOSTA
Muscolatura liscia vascolare
contrazione
Muscolatura liscia genitourinaria
contrazione
Muscolatura liscia gastrointestinale
rilasciamento
Cuore
Aumento della forza di contrazione,
tachicardia, aritmie
Fegato
Glicogenolisi, gluconeogenesi
Muscolatura radiale dell’iride
Contrazione
SONO ACCOPPIATI A PROTEINA G STIMOLATORIA, ATTIVANO LA
FOSFOLIPASI C CHE PROMUOVE UN INCREMENTO INTRACELLULARE DI Ca++
Localizzazione dei recettori α2
PRINCIPALE LOCALIZZAZIONE
RISPOSTA
Terminazione nervose
Riduzione del rilascio di
neurotrasmettitori
Muscolatura liscia vascolare
Contrazione (postsinaptici)/ rilasciamento
(presinaptici)
Isole di Langherans
Riduzione secrezione insulina
Piastrine
Aggregazione
SONO ACCOPPIATI A PROTEINA G INIBITORIA, MODULANDO IN SENSO NEGATIVO
L’ATTIVITA DELL’ADENILATO CLICLASI, OSTACOLANDO LA FORMAZIONE DI AMPc E DI
CONSEGUENZA L’INGRESSO DEL Ca++
• Nel SNA i recettori a2 sono principalmente presinaptici; la loro stimolazione determina
diminuzione del rilascio di NA dalle terminazione
simpatiche
(apertura dei canali K+ iperpolarizzazione
diminuita suscettibilità allo stimolo depolarizzante)
Localizzazione dei recettori β1
PRINCIPALE LOCALIZZAZIONE
RISPOSTA
Cuore
Aumento della forza di contrazione,
tachicardia, aritmie
Cellule iuxtaglomerulari
Aumento della secrezione di renina
Localizzazione dei recettori β2
PRINCIPALE LOCALIZZAZIONE
RISPOSTA
Muscolature lisce (tutte)
Rilasciamento
Muscolatura scheletrica
Glicogenolisi, captazione K+
Fegato
Glicogenolisi, gluconeogenesi
TUTTI I RECETTORI β PROMUOVONO L’ATTIVAZIONE DELL’ADENILATO CICLASI
CHE A SUA VOLTA ATTIVA SPECIFICHE FOSFOCHINASI CELLULARI
PROMUOVENDO EVENTI POST-SINAPTICI DIFFERENTI
I recettori b-adrenergici
• I recettori b1 sono localizzati principalmente nel
cuore, i b2 nella muscolatura liscia dei vasi, dei
bronchi e di altri organi, i b3 nel tessuto adiposo.
• Tutti i recettori b sono accoppiati a proteine Gs; la
loro stimolazione attiva l’adenilato ciclasi.
• La stimolazione dei recettori b1 cardiaci
determina: aumento della forza di contrazione,
della frequenza, della velocità di conduzione e
dell’eccitabilità uso dei ß1 agonisti selettivi
nell’insufficienza cardiaca
Riduzione della risposta a seguito di trattamenti
protratti con agonisti
• La somministrazione cronica di agonisti ß provoca
tolleranza (diminuzione della risposta). La
tolleranza rappresenta un serio problema
terapeutico.
• La tolleranza è dovuta a tre meccanismi, che
hanno cinetiche diverse e dipendono tutti dalla
fosforilazione del recettore.
La tachifilassi è invece legata ad una diminuzione della risposta senza
interferenza diretta con i recettori (meccanismi presinaptici). In seguito alla
riduzione della sintesi dei neurotramettitori (esaurimento delle riserve
sinaptiche del neurotrasmettirore)
Meccanismi di tolleranza rapida (secondi-minuti)
✓ Riduzione dell’affinità per l’agonista e riduzione della
capacità del complesso agonista-recettore di attivare la
proteina G: la fosforilazione del recettore su particolari
aminoacidi intracellulari provoca diminuzione dell’affinità
per il ligando. Inoltre, una proteina, la ß-arrestina, si lega al
recettore fosforilato impedendo l’interazione recettoreproteine G.
✓ Il recettore può essere fosforilato da:
•
una chinasi specifica (ßARK, ß-Adrenergic Receptor Kinase),
che fosforila solo il recettore occupato dall’agonista è il
legame agonista –recettore a innescare la desensitizzazione
desensitizzazione omologa;
• la fosforilazione del recettore può essere causata da altri
trasmettitori, in grado di attivare PKA o PKC (proteinchinasi
A e C) desensitizzazione eterologa.
✓ Down-regulation
• Down-regulation rapida. Il recettore fosforilato, legato alla
ß-arrestina, viene ‘internalizzato’ con un processo di
endocitosi riduzione del numero di recettori sulla
membrana. Il recettore internalizzato può essere
defosforilato (da una fosfatasi) e ritornare sulla membrana
(riciclo o turn-over) oppure essere degradato dalle
proteasi.
In ogni cellula vi è una quota di recettori internalizzati (pool intracellulare) che può ritornare sulla
membrana in assenza di agonista
• Down-regulation tardiva. Determina la riduzione a lungo
termine dei recettori. È causata da un aumento della
degradazione del recettore e/o da una diminuzione della
sua sintesi.
Farmaci attivi sulla neurotrasmissione
ADRENERGICA
• Il sistema simpatico modula importanti funzioni:
✓ Attività cardiaca
✓ Pressione sanguigna
✓ Sistema respiratorio
• Agonisti ed antagonisti adrenergici hanno grande
importanza terapeutica.
FARMACI LITICI e FARMACI MIMETICI
Tra i recettori muscarinici si distinguono tre categorie, strutturalmente simili, ma differenti
per la sequenza amminoacidica e per la localizzazione:
❖ M1 localizzati soprattutto a livello nervoso (gangli, corteccia cerebrale, ippocampo,
cellule parietali della mucosa gastrica), con azione eccitatoria per aumento dell'AMPc,
IP3 e DAG;
❖ M2 localizzati prevalentemente a livello cardiaco, dove inducono una riduzione
della frequenza cardiaca per inibizione dell'adenilatociclasi;
❖ M3 anch'essi di tipo eccitatorio e situati nelle ghiandole esocrine (salivari, lacrimali,
bronchiali...) e nei muscoli lisci
………M4 (SNC), M5 (poco caratterizzato)
L'Ach agisce indifferentemente su ognuno di questi recettori, ma i composti di sintesi ad
azione farmacologica possono essere formulati in modo da avere un'azione selettiva
La presenza del gruppo metilico ne determina la selettività verso il recettore muscarinico rispetto al nicotinico
Gli organo fosfati si legano inizialmente all'enzima e vengono idrolizzati; ne risulta un enzima fosforilato al sito
attivo. Il legame fosforo-enzima è estremamente stabile e l'idrolisi richiede tempi molto lunghi (centinaia di
ore); inoltre, l'enzima fosforilato può subire il processo di “invecchiamento”, questo implica la rottura di uno
dei due legami ossigeno-fosforo dell'inibitore ed un ulteriore rafforzamento del legame fosforo-enzima. La
velocità di invecchiamento varia a seconda della natura chimica dell'organo fosfato, ad esempio i gas nervini,
costituenti delle più pericolose armi chimiche, hanno un tempo di invecchiamento estremamente ridotto.
Sostanze fortemente nucleofile, come la pralidossima (ANTIDOTO), sono in grado di scindere il legame fosforoenzima, a patto che vengano somministrate prima che sia avvenuto l'invecchiamento
INSETTICIDI ANTICOLINESTERASICI (organofosforici e carbammati)
FONTI
Foraggi contaminati in campo per trattamenti diretti o indiretti
Foraggi contaminati durante la conservazione
Contaminazione dell’acqua o dei recipienti
Disinfestazione dei locali
Trattamenti antiparassitari sistemici o topici degli animali
Origine dolosa
Pesticidi Anticolinesterasici
Tossicocinetica
Gastroenterica
Assorbimento
Cutanea
Respiratoria
Distribuzione
Maggiore affinità per i tessuti adiposi
Metabolizzazione
Rapida metabolizzazione a livello epatico
Escrezione
Rene
Pesticidi Anticolinesterasici
Fattori che condizionano la tossicità
Fattori intrinseci o legati all’ambiente
Fattori chimico-fisici:
•
Luce
•
Umidità
•
pH ambiente
•
pH soluzioni
•
Preparati tecnici
•
Temperatura
•
Adiuvanti tecnologici
Pesticidi Anticolinesterasici
Fattori che condizionano la tossicità
Fattori estrinseci
•
Specie
•
Età
•
Sesso
i bovini sono più sensibili degli ovini
i giovani meno sensibili al parathion
le femmine più sensibili al parathion
Pesticidi Anticolinesterasici
Sinergismo
Fenomeni di sinergismo con:
Organoclorurati
Miorilassanti
Farmaci parasimpaticomimetici
Inibizione secondaria dell’ACh
Induttori enzimatici
Fenomeni di antagonismo con:
Induttori enzimatici
Composto
Specie
Parathion
Bovino
50
Suino
25
Forate
Ratto
3
Cane
3
DT os
mg/kg
Bovino
1
Pecora
0,75
Ratto
Ronnel
DL50 os
mg/kg
1
Bovino
125
Pecora
400
Ratto
906
Topo
2000
Aldicarb
Ratto
0,6-1
Propoxur
Ratto
100
Benomyl
Ratto
9500
Tossicità dei
pesticidi
anticolinesterasici
più comuni
Pesticidi Anticolinesterasici
Sintomatologia
Accumulo di ACh nei siti recettoriali
Effetti
Sindrome dei “rubinetti aperti”
1.
•
•
•
•
•
•
•
•
Muscarinici
Scialorrea
Lacrimazione
Scolo nasale sieroso
Miosi
Sudorazione
Aumento della pèeristalsi intestinale
Vomito
Diarrea
•
Minzione involontaria
•
Secrezione brinchiale
•
Bradicardia
Pesticidi Anticolinesterasici
Pesticidi Anticolinesterasici
Sintomatologia
Accumulo di ACh nei siti recettoriali
Effetti
Sindrome dei “rubinetti aperti”
2.
Nicotinici
•
Fascicolazioni
•
Tremori muscolari
•
Barcollamento
•
Tachicardia
3. Centrali
•
Irrequietezza
•
Eccitazione
•
Atassia
•
Depressione dei centri respiratori e circolatori
•
Convulsioni
MORTE PER INSUFFICIENZA RESPIRATORIA
Pesticidi Anticolinesterasici
Sintomatologia
Neurotossicità ritardata
Se assunto in piccole dosi, nell’uomo ed in alcuni animali (pollo, gatto, vitello)
determinano degenarazione retrograda dei nervi motori. La sintomatologia
compare dopo 10-20 giorni.
NON E’ STATA OSSERVATA PER I CARBAMMATI
Inizia dalle porzioni distali dell’assone e progredisce fino ad interessare le zone
spinocerebellari e vestibolospinali.
Patogenesi
Non chiara.
Possibile legame a delle esterasi specifiche della mielina con modificazione del
flusso intracellulare di enzimi e principi nutritivi
alterazioni guaina
mielinica
Pesticidi Anticolinesterasici
Terapia
Trattamento differenziato
Atropina solfato: 0,2-0,5 mg/Kg
(antagonista)
Ossime: Pralidossima
Pralidossina metilsolfato
Piccoli animali 15-40 mg/Kg IV (lentamente)
Grandi animali: 25-50 mg/kg IV (lentamente)
LE OSSIME NON VANNO SOMMINISTRATE NELL’AVVELENAMENTO DA CARBAMMATI
Trattamento sintomatico
FARMACI ATTIVI SUL SISTEMA SIMPATICO
DIRETTI (agonisti recettoriali selettivi e non)
❖ SIMPATICOMIMETICI
❖ SIMPATICOLITICI
ANTAGONISTI RECETTORIALI
AGENTI DI
BLOCCO
NEURONALE
INDIRETTI
•
•
•
•
liberazione catecolamine dai depositi endogeni
inibizione re-uptake
riduzione attività MAO e COMT
colinergici ad attività nicotinica gangliare (ma
effetti finali complessi perché non distingue tra
simpatico e parasimpatico)
DIRETTI
❖ l’attività dipende dalla selettività dell’agente verso i vari tipi e sottotipi
recettoriali
tale caratteristica permette di modulare selettivamente le funzioni regolate da quel particolare
recettore limitando gli effetti dovuti alla concomitante attivazione di altri sottotipi recettoriali
❖ la selettività avviene solo a particolari intervalli di concentrazione, poiché si
perde a concentrazioni maggiori
struttura di base: β-feniletilamina
maggiore affinità recettoriale se anello catecolico integro e presente –OH sul C β della
catena laterale
minore affinità recettoriale se manca uno dei due ma molecola meno aggredibile dalle
COMT e più lipofila (SNC)
a1
Agonisti adrenergici
a2
b1
adrenalina
noradrenalina
metossamina
fenilefrina
clonidina
b2
isoprenalina
dobutamina clenbuterolo
Noradrenalina e Adrenalina: vasocostrizione generalizzata (dovuta alla stimolazione
degli α recettori presenti sulla fibrocellula muscolare liscia vasale)
Adrenalina anche β (gli effetti dipendono dalla distribuzione dei recettori α e β …. in
alcuni distretti vascolari predomina la popolazione di tipo α es. sottocute, in altri si
manifesta vasodilatazione conseguente alla stimolazione della predominante
popolazione β es. vasi muscolatura scheletrica)
FARMACI SIMPATICOMIMETICI AD AZIONE DIRETTA
Farmaci simpaticomimetici a struttura catecolica:
Adrenalina, Noradrenalina e Dopamina – Dobutamina
(sintesi)
Farmaci simpaticomimetici a struttura non catecolica:
Fenilefrina, Clonidina
Clenbuterolo, Salbutamolo, Terbutalina
Adrenalina
Fiale 1mg/ml ADRENALINA®
Catecolamina endogena agonista a e b adrenergico non
selettivo
Effetti cardiovascolari:
- vasocostrittore arteriolare e venoso
- azione inotropa e cronotropa positiva
- del consumo miocardico di ossigeno
- della pressione arteriosa sistolica e differenziale
- resistenze arteriose e venose polmonari
Effetti polmonari: potente broncodilatatore
Effetti metabolici: glicemia, consumo di ossigeno
Effetto antagonista all’Istamina
Adrenalina
FARMACOCINETICA
➢ Emivita: 1-2 minuti
➢ Onset time: 1-2 minuti
➢ Durata d’azione: 2-5 minuti
➢ Metabolismo: fegato (MAO e COMT)
➢ Eliminazione: renale
Adrenalina
INDICAZIONI D’IMPIEGO:
➢ Arresto cardiaco
➢ Anafilassi
CONTROINDICAZIONI:
Assolute:
➢ Ipersensibilità al farmaco
Relative:
➢ Ipertensione
➢ Ipertiroidismo
➢ Malattie vascolari occlusive
➢ Diabete mellito
➢ Feocromocitoma
➢ Uso di b bloccanti
➢
Gravidanza a termine (vasocostrizione
flusso utero-placentare e aritmie fetali)
INTERAZIONI FARMACOLOGICHE DELL’ADRENALINA
Alfa-bloccanti: antagonizzano l’azione farmacologica dell’adrenalina (in particolare l’aumento della pressione
arteriosa). La co-somministrazione di adrenalina e tolazolina non è raccomandata.
Anestetici generali (alotano, ciclopropano): la somministrazione di anestetici liquidi volatili in associazione con
adrenalina può determinare la comparsa di aritmie gravi e di fibrillazione ventricolare.
Anestetici locali: l’adrenalina potenzia l’attività anestetica perchè, tramite vasocostrizione, rallenta l’assorbimento
dell’anestetico e ne prolunga l’azione farmacologica.
Anfetamina: la co-somministrazione con adrenalina potrebbe precipitare l’insorgenza di aritmia.
Antidepressivi triciclici: può aumentare la risposta pressoria indotta dall’adrenalina (2-4 volte). Poichè gli
antidepressivi possono causare aritmie, la co-somministrazione con adrenalina potrebbe precipitare l’insorgenza di
aritmia.
Antipsicotici: possono antagonizzare l’effetto ipertensivo dei simpaticomimetici.
Antistaminici (clorfenamina, difenidramina, tripelennamina): possono potenziare gli effetti simpaticomimetici
dell’adrenalina.
Beta-bloccanti: in associazione con adrenalina può manifestarsi ipertensione grave (per predominanza del tono alfa) e
bradicardia (per aumento del riflesso vagale). I beta-bloccanti potrebbero diminuire la risposta all’adrenalina.
Chinidina, glucosidi cardioattivi: in associazione con adrenalina possono provocare fibrillazione ventricolare.
Clonidina: possibile rischio di ipertensione con adrenalina.
Guanetidina, levotirosina sodica, MAO-inibitori, reserpina: possono potenziare gli effetti simpaticomimetici
dell’adrenalina.
Entacapone: è possibile un aumento degli effetti farmacologici dell’adrenalina.
Ergotamina, ergometrina: in associazione con farmaci simpaticomimetici aumenta il rischo di ergotismo.
Dopexamina: può potenziare l’effetto della adrenalina.
Doxapram: con adrenalina può verificarsi aumento del rischio di ipertensione
Insulina e ipoglicemizzanti orali: l’adrenalina ne riduce l’effetto terapeutico per aumento della glicemia indotto
dall’inibizione dell’uptake periferico di glucosio e dalla stimolazione della glicogenolisi.
Oxitocina: in associazione ad adrenalina si può avere un effetto additivo di vasocostrizione con aumento della
pressione arteriosa.
Propanololo: può inibire la risposta pressoria e la broncodilatazione indotte dall’adrenalina.
Noradrenalina
Fiale 2 mg/ml NORADRENALINA TARTRATO ®
Agonista dei recettori a e b adrenergici
farmacocinetica
➢ Eliminazione: epatica
➢ Onset time e durata d’azione: 1-2 minuti
INDICAZIONI D’IMPIEGO:
➢ Shock cardiogeno
➢ Shock settico
➢Arresto cardiaco
CONTROINDICAZIONI:
➢ Trombosi arteriosa
➢ Ipercapnia e/o ipossia grave
Dobutamina
Catecolamina sintetica
miscela racemica l’enantiomero (-) presenta attività α1 e β1 agonista,
l’enantiomero (+) antagonista per gli α1 e agonista β1 10 volte maggiore del (-)
Agente simpaticomimetico sintetico selettivo sui recettori b1.
Ha potente attività inotropa positiva e lieve attività cronotropa positiva (la
minor stimolazione della frequenza e quindi minor consumo di O2 la rende
più idonea della dopamina nel trattamento dell’insufficienza congestizia
acuta grave)
Dobutamina
Farmacocinetica
➢ Emivita: 2 minuti
➢ Onset time: 1-2 minuti
➢ Massima azione dopo la somministrazione: 10 minuti
➢ Durata azione: non superiore a 10 minuti
➢ Metabolismo: fegato ed in altri tessuti (COMT e
glicuronazione per i 2/3 della dose)
➢ Escrezione sotto forma di metaboliti urinari entro 48 ore
Farmaci simpaticomimetici a struttura non catecolica:
Fenilefrina (α1 agonista)
Clonidina, Xilazina, Detomidina, Medetomidina (α2 agonisti)
Clenbuterolo, Salbutamolo, Terbutalina (β2 agonisti)
FENILEFRINA
Amina non catecolica agonista α1 (nonostante la sostituzione sul gruppo amminico della
catena etilaminica di un H con CH3 fornisce a regola maggiore selettività β!!)
Ha durata d’azione più prolungata per l’assenza di un ossidrile (OH) dell’anello benzenico che
la rende meno degradabile da parte delle COMT, ma meno potente dell’adrenalina
Ipertensivo per intensa vasocostrizione se somministrato per via parenterale
Principale uso: decongestionante delle mucose per uso topico
midriatico in oftalmologia
α2 agonista impiegato nella terapia dell’ipertensione
arteriosa
Azione legata alla interazione con i recettori α2
presinaptici periferici e α2 postsinaptici localizzati nei
centri di controllo cardiovascolare del SNC (nucleo
del tratto solitario), la cui stimolazione sopprime il
tono simpatico
Prevale quindi il tono parasimpatico determinando
ipotensione e bradicardia
La somministrazione endovenosa determina in una
prima fase ipertensione transitoria (α1 e α2
postsinaptici….mantiene una certa affinità per α1)
L’attivazione dei recettori α2 presinaptici centrali è
responsabile delle proprietà sedative della clonidina
CLONIDINA
Xilazina
Detomidina
Medetomidina
agiscono in modo analogo alla clonidina seppur con qualche differenza relativamente ad es.
alla risposta della muscolatura uterina (la xilazina nelle bovine può dare contrazioni del
miometrio, raramente la detomidina e la medetomidina)
Impiegati in Medicina Veterinaria come
SEDATIVI (SNC)
Clenbuterolo
Salbutamolo
Terbutalina
Sono simpaticomimetici agonisti b2 selettivi
Rispetto alle catecolamine classiche (isoprenalina) sono ridotti
gli effetti collaterali indesiderati legati all’attivazione dei recettori
b1 cardiaci.
In medicina veterinaria il clenbuterolo trova impego:
• in numerose patologie dell’apparato polmonare del cavallo
(malattia polmonare ostruttiva cronica COPD)
• come tocolitico nel bovino (minaccia aborto, parto prematuro)
AGENTI PROMOTORI DI CRESCITA «RIPARTITORI DI ENERGIA»
Nella muscolatura striata sono presenti recettori b2 la cui
attivazione promuove un effetto che indirizza il metabolismo dei
principi attivi assunti con la dieta verso la sintesi proteica
muscolare piuttosto che verso la sintesi di grasso di deposito
(effetto metabolico anabolizzante)
Questo effetto è coadiuvato dalla vasodilatazione b2 mediata del
distretto vascolare muscolare
Tale effetto si consegue però con trattamenti cronici e dosaggi 10 –
20 volte quelle impiegate per il trattamento terapeutico che deve
essere protratto fino al momento della macellazione (RESIDUI
rischiosi, la cui assunzione cronica può causare una downregulation della popolazione b2 del consumatore condizionandone
la risposta in caso di patologie, quali l’asma, trattate con b2
bloccanti
DIVIETO D’USO DEI β2 AGONISTI PER SCOPI ZOOTECNICI
Farmaci simpaticomimetici ad azione indiretta
Farmaci che per la loro somiglianza alle catecolamine endogene, penetrano
all’interno del terminale nervoso utilizzando l’uptake1 si localizzano nelle
vescicole determinando l’estrusione della NA nel citoplasma che, in parte,
viene liberato nello spazio intersinaptico
Tiramina, amfetamina, efedrina, fenilpropanolamina; cocaina e antidepressivi
triciclici (Farmaci che modulano i meccanismi di interruzione del segnale)
Tiramina
Efedrina
Amfetamina
Fenilpropanolamina
La Tiramina è un’ammina biogena (nell’organismo come prodotto
del metabolismo della Tirosina) è non ha alcun impiego
terapeutico.
I formaggi stagionati possono contenere concentrazioni elevate e se assunti da pazienti
trattati con farmaci anti MAO, possono dare crisi ipertensive!
Farmaci simpaticomimetici ad azione indiretta
Amfetamina
Efedrina
Fenilpropanolamina
L’amfetamina è un potente liberatore di noradrenalina dalle fibre nervose
Noradrenergiche del SNA e grazie alla presenza del metile che lo rende
liposolubile questo effetto è particolarmente pronunciato nel SNC.
Nel SNC provoca la liberazione di ammine endogene quali dopamina e 5-HT,
che spiega la maggior parte degli effetti comportamentali
L’amfetamina inoltre limita il re-uptake della NA nel terminale assonico
potenziandone ulteriormente gli effetti
In veterinaria uso limitato (narcolessia del cane)
Farmaci simpaticomimetici indiretti ad azione mista
L’efedrina è un alcaloide
estratto da Piante del genere
Ephedra
L’assenza degli – OH
sull’anello aromatico
e dei due gruppi metilici
ne giustifica la durata d’azione
e gli effetti centrali.
Efedrina Fenilpropanolamina
(nor-efedrina)
Il meccanismo d’azione è definito misto
perché agisce sia promuovendo la
liberazione della NA (predominante) che
direttamente con agonismo non selettivo
sugli ae b
In Medicina Veterinaria viene impiegata raramente.
Nelle sindromi respiratorie ostruttive; per
applicazioni topiche come decongestionante delle
mucose (TACHIFILASSI per depauperamento NA)
Farmaci simpaticolitici recettoriali e neuronali
I farmaci che bloccano o inibiscono gli effetti delle
ammine simpaticomimetiche si dividono in due gruppi:
a) Farmaci antagonisti dei recettori adrenergici o
simpaticolitici
Antagonisti dei recettori a
Antagonisti dei recettori b
b) Farmaci agenti di blocco neuronale adrenergico o
antiadrenergici
Antagonisti adrenergici
a1
a2
b1
b2
labetololo
fenossibenzamina
prazosina
yohimbina
propranololo
atenololo
butoxamina
Farmaci antagonisti dei
recettori a-adrenergici
I farmaci antagonisti dei recettori a-adrenergici sono
strutturalmente molto eterogenei le principali classi
chimiche sono:
Antagonisti a -adrenergici non selettivi (fenossibenzamina)
Antagonisti a1 – adrenergici selettivo (prazosina)
Antagonisti a2 – adrenergici selettivo (Yoimbina)
Altri farmaci con effetti a-adrenergico antagonisti
Farmaci antagonisti dei recettori a-adrenergici
Antagonisti a -adrenergici non selettivi
Fenossibenzamina,
Fentolamina
La fenossibenzamina è una aloalchilamina (derivato imidazolinico) che promuove
effetti di blocco a1- e a2-adrenergici. Inoltre ha attività anticolinergica ed
antiserotoninergiche. Gli effetti sono di lunga durata – legame covalente.
La fentolamina è un imidazolina ad attività più selettiva verso i recettori aadrenergici, l’azione è di tipo competitivo-reversibile. Effetti di breve durata.
L’effetto farmacologico più importante è l’ipotensione sistemica (blocco dei
recettori adrenergici vasali.
La fenossibenzamina è impiegata nel cane e nel gatto per ridurre il tono della
muscolatura dell’uretra e nel cavallo per ridurre lo spasmo amediato nel corso
della laminite acuta
Farmaci antagonisti dei recettori a-adrenergici
Antagonisti a1 – adrenergici selettivo (prazosina)
Antagonisti a2 – adrenergici selettivo (Yoimbina)
La prazosina è un derivato piperazonil chinazoline di elevata
selettività vs gli a1- recettori e provoca intensa vasodilatazione
e ipotensione. L’aumento della frequenza e della gittata cardiaca sono meno
imponenti degli antagonisti non selettivi. Impiegato nel trattamento dell’ipertensione
sistemica e dll’insufficienza congestizia.
La yoimbina è un alcaloide naturale ricavata dall'albero Pausinystalia yohimbe
(Fam. Rubiaceae), particolarmente diffuso nelle regioni dell'Africa occidentale.
(burundanga) a2 selettivo competitivo, efficace nell’antagonizzare gli effetti centrali e
periferici della xilazina.
Farmaci antagonisti dei recettori b-adrenergici
Farmaci capaci di antagonizzare, in modo competitivo, il legame delle catecolamine
Endogene con i recettori adrenergici.
Sono molecole caratterizzati dall’avere una struttura chimica simile alla
isoprenalina - Agonista b non selettivo.
Isoprenalina
Propanololo
Propanololo – Antagonista selettivo per i recettori b,privo di selettività nei
confronti delle differenti popolazioni b1e b2 recettoriali.
Le modifiche chimiche effettuate intorno alla struttura “attiva b” ha permesso di
ottenere farmaci:
Antagonisti selettivi b1 – metoprololo, atenololo.
Antagonisti non selettivi con capacità di bloccare recettori a.labetololo
Con residua attività simpatico mimetica –agonisti parziali - pindololo
Farmaci antagonisti dei recettori b-adrenergici
Antagonisti selettivi b1 – metoprololo, atenololo.
Antagonisti non selettivi con capacità di bloccare recettori a.labetololo
Con residua attività simpatico mimetica –agonisti parziali - pindololo
metoprololo
atenololo
Gli effetti più importanti sono riconducibili al blocco dei recettori b1 cardiaci, con
Conseguente riduzione della forza di contrazione, della gittata e della frequenza.
Effetti evidenti soprattutto nei soggetti con simpatico attivato (attività fisica,
Stress o patologie come l’ipertensione e l’ischemia miocardica).
Farmaci antagonisti dei recettori b-adrenergici
Antagonisti selettivi b1 – metoprololo, atenololo.
Antagonisti non selettivi con capacità di bloccare recettori a.labetololo
Con residua attività simpatico mimetica –agonisti parziali - pindololo
I farmaci di blocco hanno anche effetti sul ritmo e sull’automatismo del cuore:
Riducono la frequenza di scarica del nodo del seno;
Diminuiscono la velocità di depolarizzazione di focolai ectopici di eccitazione;
Rallentano la conduzione atriale e la conduzione atrio-ventricolare;
Aumentano il periodo refrattario del nodo atrio-ventricolare.
Sul sistema vascolare, il propanololo, determina un iniziale innalzamento
delle resistenze periferiche per vasocostrizione riflessa a- mediata.
Effetto che non è accompagnato da un”ovvio” aumento della pressione sistemica:
Blocco dei recettori b1 cardiaci;
Probabile effetto inibitorio sugli autorecettori b2 presinaptici (centrali e periferici);
Riduzione della produzione di renina b-mediata (cellule justaglomerulari rene);
Farmaci antagonisti dei recettori b-adrenergici
Antagonisti selettivi b1 – metoprololo, atenololo.
Antagonisti non selettivi con capacità di bloccare recettori a.labetololo
Con residua attività simpatico mimetica –agonisti parziali - pindololo
In medicina veterinaria Il propanololo viene impiegato per il trattamento
dell’ipertensione associata al feocromocitoma (tumore cellule cromaffini
midollare surrene).
L’atenololo ed il metoprololo sono impiegati nel trattamento di patologie
Broncopolmonari di varia natura.
Nel gatto l’atenololo è impiegato nelle aritmie sopraventricolari.
Il carazololo antagonista b-adrenergici impiegato nel suino nella gestione
dello stress da trasporto e per facilitare il parto e l’espulsione della placenta
(blocco dell’effetto tocolitico b2 mediato.
Farmaci di blocco neuronale adrenergico o
antiadrenergici.
Sono definiti antiadrenergici quei farmaci capaci di bloccare le
attività delle sinapsi adrenergiche.
I meccanismi con cui avvengono queste interruzioni possono essere
diversi ma il risultato finale è l’interruzione della liberazione di
neurotrasmettitori nello spazio sinaptico.
Reserpina (impiegata in passato nei cavalli- blocca l’entrata della NA
all’interno delle vescicole per interferenza sul meccanismo di Mg e ATP
dipendente)
Guanetidina (entra nelle sinapsi tramite uptake1 si concentra nelle vescicole
e stabilizza le membrane impedendo l’esocitosi)
Bretilio (determina la deplezione del neurotrasmettitore)
Farmaci di blocco neuronale adrenergico o
antiadrenergici.
La reserpina è un alcaloide estratto dalla Rauwolfia serpentina, usato in passato per
trattare soggetti con disturbi mentali. In veterinaria per sedare cavalli “nevrili”.
La reserpina blocca il trasporto della noradrenalina all’interno delle vescicole
Interferendo con il trasporto Mg++ e ATP dipendente. Con accumulo in sede
Citoplasmatica di NA demolita dalle MAO.
Farmaci di blocco neuronale adrenergico o
antiadrenergici.
guanetidina
La guanetidina è il prototipo dei farmaci che inibiscono l’attività dei
Neuroni adrenergici postgangliari periferici.
Non presenta effetti centrali non attraversando la barriera
ematoencefalica.
La guanetidina entra nel bottone simpatico con lo stesso
meccanismo Di uptake della NA si concentra nelle vescicole e si
sostituisce ad essa.
Per un meccanismo di stabilizzazione delle membrane ne
impedisce la Liberazione nello spazio sinaptico (simile ad un’azione
anestetica locale).
FARMACI CHE AGISCONO SULLA PLACCA NEURO-MUSCOLARE
Diverse sostanze chimiche possono influenzare la trasmissione dell’impulso nervoso sulla placca motrice con vari
meccanismi
1)Sostanze che bloccano la trasmissione a livello della placca motrice
Esistono sostanze come il curaro , capaci di impedire la propagazione degli impulsi attraverso la GNM
Esse esplicano un’azione competitiva con l’Ach, bloccando i recettori della placca ai quali questa si dovrebbe fissare,
pertanto essa non è più in grado di estrinsecare la sua attività stimolante
Altre sostanze come la tossina del bacillo botulinico, agiscono invece a livello presinaptico, bloccando i canali del
calcio, determinando una riduzione o abolizione del rilascio dell’Ach
2)sostanze che eccitano la fibra muscolare per azione acetilcolino-simile
Varie sostanze come la metacolina, il carbacol, e la nicotina, hanno sulla fibra muscolare un’azione simile a quella
dell’Ach; la differenza tra queste sostanze e l’Ach, sta nel fatto che esse non vengono distrutte dalla colinesterasi,
sicché una volta applicate alla fibra muscolare, la loro azione persiste per molti minuti o per molte ore
Queste sostanze creano aree circoscritte di depolarizzazione, ed ogni volta che la rimanente fibra muscolare si
ripolarizza, queste aree depolarizzate, a causa della loro permeabilità agli ioni, fanno esplodere nuovi potenziali
d’azione, provocando perciò una condizione di spasmo
3)sostanze che eccitano la placca motrice mediante inattivazione della colinesterasi
Esistono tre sostanze la fisostigmina, la neostigmina ed il diisopropilfluorofosfato, che si combinano con la
colinesterasi rendendola inattiva, per cui questa non degrada l’Ach liberata nella placca motrice.
Conseguentemente l’Ach si accumula nella GNM, determinando un susseguirsi di nuovi impulsi nervosi con spasmo
muscolare.
FISOSTIGMINA
Physostigma venenosum
(fava del Calabar -Africa occidentale)
droga: semi
p.a.: alcalodie fisostigmina o eserina
Inibitore reversibile
dell’acetilcolinesterasi
NEOSTIGMINA derivato semisintetico
(non passa la BEE)
MIORILASSANTI
Sostanze in grado di ridurre il tono della muscolatura, scheletrica (volontaria) o liscia (involontaria)
a) ad azione centrale
b) ad azione periferica
1. miorilassanti competitivi o non depolarizzanti
2. miorilassanti polarizzanti
a) agiscono soprattutto a livello del midollo spinale, deprimendo i riflessi mono e poli-sinaptici, sono
utilizzati come antispastici e bloccanti neuromuscolari nelle anestesie chirurgiche
(tiocolchicoside, baclofen, pridinolo-anche periferico)
b) 1. I miorilassanti competitivi entrano in competizione con l'acetilcolina, poiché sono in grado di
occupare gli stessi siti recettoriali posti sulla placca motrice, inibendo così la funzione dell'acetilcolina
di attivare la contrazione muscolare. In questo modo, in seguito ad un egual impulso nervoso, si avrà
una risposta in termini di contrazione muscolare minore. Questi farmaci sono utilizzati nelle
operazioni maggiori in quanto la loro azione è piuttosto prolungata
(metocurina, il pancuronio, la tubocurarina, l'alcuronio, l'atracurio, la gallamina e il vecuronio)
b) 2. I miorilassanti depolarizzanti agiscono invece producendo una iniziale depolarizzazione della
placca motrice (fascicolazioni) e dopo si ha paralisi della muscolatura per blocco (desensibilizzazione
recettoriale)
Questi farmaci vengono utilizzati nelle operazioni di più breve durata e nelle manipolazioni
(decametonio e succinilcolina)
ANESTETICI LOCALI
L'anestesia locale è una perdita della sensibilità in una
determinata regione senza perdita della coscienza o
compromissione del controllo di funzioni vitali
❖ Bloccano la generazione e la propagazione degli impulsi della fibra nervosa
in maniera prevedibile e reversibile
❖ Eliminano la sensibilità, e quindi anche la percezione degli stimoli
nocicettivi, solo nelle aree corporee innervate dalla fibra bloccata
❖ Gli anestetici locali bloccano transitoriamente e reversibilmente la
conduzione assonica dell'impulso nervoso a livello sia degli assoni che di
altre membrane eccitabili in cui i canali del Na+ rappresentano lo
strumento principale per la generazione del potenziale d'azione
MECCANISMO D’AZIONE
Disattivazione dei canali del sodio dell’assolemma per ancoraggio
all’interno del canale ed impedimento al transito del Na+
AL
In condizioni di riposo la porta d’ingresso del Na+ è
chiusa; con la depolarizzazione si apre e permette il
transito di Na+ all’interno della cellula.
Contemporaneamente ed in maniera molto lenta il
canale raggiunge una configurazione inattivata (porta
esterna aperta, porta interna chiusa), che resta tale
fintanto che la membrana non si è completamente
ripolarizzata. Il canale in questo stato è
completamente refrattario alle variazioni di potenziale.
MECCANISMO D’ AZIONE
Gli anestetici locali si legano a recettori situati sull'estremità intracellulare dei canali del
sodio, bloccandone l'attività (apertura) in maniera tempo- e voltaggio-dipendente. Ne
conseguono un aumento della soglia di eccitazione, il rallentamento della velocità di
conduzione dell'impulso, la riduzione dell'ampiezza del potenziale d'azione e infine
l'estinzione della formazione del potenziale d'azione stesso.
Per agire (legarsi al sito all’interno
del canale ionico) l’anestetico
locale deve essere in forma
dissociata = idrofilica, ma per
oltrepassare la membrana delle
strutture adiacenti al nervo
(epinevrio,perinevrio,
endonevrio) deve essere in
forma neutra = lipofila
L'azione degli anestetici locali non è limitata alla perdita di sensibilità, in quanto
essi sono in grado di bloccare i nervi di ogni tipo. Tuttavia, vengono bloccate
preferenzialmente le fibre più piccole. In generale, vengono bloccate prima le
fibre mieliniche più piccole e poi quelle amieliniche. Inoltre, la dipendenza
dell'azione degli anestetici locali dalla frequenza favorisce il blocco delle piccole
fibre sensitive (e di quelle dolorifiche in particolare) che hanno una frequenza di
firing (unità di stimolazione elettrica) più elevata di quelle motorie
Le funzioni sensitive scompaiono nel seguente ordine. Il ripristino è in maniera inversa :
dolore
freddo
caldo
tatto
sensibilità articolare
pressione profonda (barestesica)
La struttura della maggior parte degli anestetici locali è caratterizzata da un GRUPPO
LIPOFILO (generalmente un anello aromatico) unito ad una CATENA INTERMEDIA a cui
è legato un GRUPPO IONIZZABILE (generalmente un'amina terziaria)
Caratteristiche chimiche degli A.L
Gli anestetici locali
sono amine terziarie
debolmente basiche
Gli AL sono in genere costituiti da tre porzioni:
• Polo lipofilo
rappresentato spesso da un anello aromatico. Responsabile
della liposolubilità del prodotto, della diffusione nei tessuti e nelle membrane,
del legame alle proteine plasmatiche e dell'attività.
• Polo idrofilo
condiziona la diffusione della forma non ionizzata, e la
ionizzazione della molecola dell'anestetico locale.
• Catena intermedia
permette la classificazione degli AL. a seconda del
legame presente in :
Amino-esteri (leg.estereo) procaina, clorprocaina, tetracaina
Amino-amidi
(leg.amidico) lidocaina, mepivacaina, prilocaina, bupivacaina,
etidocaina, ropivacaina
La natura della catena intermedia condiziona il
metabolismo di queste sostanze:
• Amino-esteri
rapidamente idrolizzati nel
plasma dalle pseudocolinesterasi
• Amino-amidi degradati meno rapidamente e
catabolizzati a livello dei microsomi epatici.
Questo conferisce a queste molecole una
stabilità e una durata d'azione maggiore.
PROPRIETA’ FISICO-CHIMICHE
I fattori che influenzano l’attività farmacologica
(POTENZA, LATENZA, DURATA DEL BLOCCO):
▪ LIPOSOLUBILITA’
▪ COSTANTE DI DISSOCIAZIONE Pka
▪ BINDING PROTEICO
DURATA
POTENZA
ONSET
PROPRIETA’ FISICO-CHIMICHE CHE CONDIZIONANO LA
CINETICA E DINAMICA
LIPOSOLUBILITA’
pKa
I composti più liposolubili sono
i più potenti, per la maggior
diffusibilità tra le membrane
biologiche.
Possono essere sequestrati da
tessuto adiposo peridurale o
perinevrio
È il grado di dissociazione a pH
fisiologico.
Tanto più il pH è lontano dal pKa,
tanto minore è il farmaco in
forma neutra, quindi tanto
maggiore sarà la latenza
BINDING PROTEICO
È direttamente proporzionale alla durata d’azione dell’anestetico.
Definisce l’affinità di legame del farmaco con la proteina di
membrana dove risiede il sito d’azione del farmaco
L'ASSORBIMENTO SISTEMICO degli anestetici
locali è influenzato da: dose, sede di iniezione,
legame farmaco-tessuti, sostanze
vasocostrittrici, proprietà fisico-chimiche e
farmacologiche della molecola
METABOLISMO ED ESCREZIONE: gli anestetici
locali vengono trasformati nel fegato o nel
plasma in metaboliti più idrosolubili che
vengono poi escreti per via urinaria.
ASSOCIAZIONE CON VASOCOSTRITTORI
La durata d'azione degli anestetici locali è
proporzionale al tempo in cui rimangono a
contatto con il nervo
Nella pratica clinica, le preparazioni di
anestetici locali contengono spesso anche
una sostanza vasocostrittrice (di solito
adrenalina) che ha una duplice azione:
diminuire la velocità con cui l'anestetico
locale viene rimosso dal sito desiderato e
limitare la tossicità sistemica.
EFFETTI SISTEMICI
Gli anestetici locali sono in grado di interferire con l'attività di TUTTE le fibre nervose e
possono quindi avere importanti effetti anche sul sistema nervoso centrale, sui gangli del
sistema autonomo, sulla giunzione neuromuscolare e su tutta la muscolatura.
Effetti sul SNC: agitazione, tremore, convulsioni cloniche, depressione dell'attività
neuronale, arresto respiratorio.
Effetti sul sistema cardiovascolare: tachicardia, fibrillazione, collasso e morte.
Effetti sulla muscolatura liscia: aumento del tono gastrointestinale, rallentamento delle
contrazioni uterine.
Ipersensibilità agli anestetici locali: dermatite allergica, asma.
Tecniche di anestesia
Anestesia di superficie o topica
applicazione diretta sulla pelle o mucose con paralisi
delle strutture nervose affioranti. Inefficace su cute integra
Anestesia di infiltrazione
iniezioni nel sottocute di piccoli volumi di anestetico. Usato
per caudectomia (no associazione con vasocostrittori per non provocare necrosi)
Anestesia di blocco (nervoso regionale)
si inietta l’A.L nelle vicinanze del nervo, il
farmaco diffonde e anestetizza tutta l’area innervata
Anestesia epidurale o peridurale
si inietta l’A.L nello spazio extradurale del canale
spinale in regione lombosacrale. Azione sui nervi prima che questi fuoriescano dalla
colonna vertebrale
Anestesia paravertebrale
tipo di anestesia da conduzione. Viene applicato sui nervi
prima della loro emergenza dai fori intervertebrali. Usato per la ruminotomia.
Anestesia intratecale o spinale
farmaco nel liquido spinale
poco usata negli animali, si pratica iniettando il
Procaina
Di largo impiego per scarsa tossicità. Rapidamente
assorbito ma azione breve perché è idrolizzato da
pseudocolinoesterasi o metabolizzato nel fegato e
metaboliti escreti con urine
Impiego clinico: 1)A.di infitrazione 2)A.di
conduzione 3)A. epidurale
Lidocaina
Potenza anestetica maggiore di quella della
procaina e più rapida velocità di azione.
Rapidamente metabolizzata dal fegato ed
eliminata con le urine.
Impiego clinico: 1)A.topica 2)A.di infiltrazione
3)A.di conduzione 4)A.epidurale
Sia nei grossi animali che nei piccoli.
Possiede anche un’azione antiaritmica
(depressione dell’eccitabilità miocardica)
Benzocaina
Proprietà anestetiche
limitate e poco solubile.
Impiego clinico:
1)sedazione nei pesci
Carbocaina
Potenza anestetica maggiore di
quella della procaina ed uguale a
quella della lidocaina. Impiego
clinico: 1)A.epidurale
Cavallo e cane
Bupivacaina
2-4 volte più potente di
lidocaina. Impiego
clinico: 1)A.spinale
pecora
Dibucaina
Molto potente e tossica.
Stretto margine di
manegevolezza.
Impiego clinico:
1)pomata
CARBONAZIONE
• Alcalinizzando la soluzione si ottiene una quota
maggiore di farmaco in forma neutra e quindi
maggiormente in grado di attraversare le membrane
fosfolipidiche.
• Da ciò ne deriva un aumento dell’onset, della durata e
della potenza.
• La quantità di bicarbonato da aggiungere dipende
dalla pKa del farmaco
▪ LIDOCAINA pKa 7.9
– 1 ml bicarbonato 8.4% ogni 10 ml di soluzione
▪ BUPIVACAINA pKa 8.1
– 0.1 ml bicarbonato 8.4% ogni 10 ml di soluzione
MISTURE DI ANESTETICI LOCALI
Il razionale è quello di sfruttare la rapidità di onset di
uno e la lunga durata d’azione di un altro:
1. MEPIVACAINA + BUPIVACAINA
2. LIDOCAINA + BUPIVACAINA
3. MEPIVACAINA + ROPIVACAINA
4. MEPIVACAINA + L-BUPIVACAINA
CARAZOLOLO
Farmaco indicato nel bovino e suino per proteggere l'animale in situazioni di stress
Farmaco beta-bloccante (antagonista dei recettori beta-adrenergici, betasimpatolitico)
Legandosi in modo reversibile impedisce alle catecolamine ( adrenalina e noradrenalina )
liberate in caso di stress di esplicare la loro azione
Viene usato per prevenire gli effetti dello stress da trasporto o da costituzione dei
nuovi gruppi di animali di qualsiasi età e sesso.
Trova impiego anche nel campo ostetrico-ginecologico: inibendo l'azione tocolitica
dell'adrenalina permette all'ossitocina di indurre le contrazioni ampie e regolari necessarie
per il parto e espulsione della placenta.
L'assorbimento è rapido, l'efficacia clinica rimane circa 10 ore dopo la
somministrazione, l'eliminazione in parte per via epatica in parte via urinaria.
Somministrazione per via IM e EV in forma di sale (carazololo cloridrato)
Tempo di attesa :
carne 24 ore
latte 12 ore
Specialità registrate : SIMPANORM 100 ml
XYLAZINA
agonista alfa 2-adrenergico usato ampiamente in medicina veterinaria.
Nel cane, gatto e cavallo viene usato come pre-anestetico riducendo fino a 50% l’uso di barbiturici o anestetici inalatori.
I Bovini sono estremamente suscettibili agli effetti della xylazina, 10 volte più sensibili in confronto con altri animali.
Nel gatto può essere usato come emetico in caso di bisogno.
Nella cattura degli animali esotici viene usata con fucile-siringa.
Xylazina è agonista dei recettori alfa 2 adrenergici. Attraverso la stimolazione dei questi recettori provoca sedazione,
analgesia e rilasciamento muscolare (effetto miorilassante).
Assorbimento di xylazina rapido, come anche la metabolizzazione epatica .
L'escrezione avviene tramite l’urina.
Dopo assorbimento i sintomi possono comprendere effetti clinici dose-dipendenti (depressione respiratoria, bradicardia,
ipertensione, aritmia..)
Xylazina può essere usata:
via IM o SC con effetto dopo 10-15 min.
via EV effetto più immediato, dopo 3-5 min.
Tempo di attesa : bovini carne 1 giorno latte 0 giorni
equini carne 1 giorno latte 0 giorni
Specialità registrate :NERFASIN 20mg/ml cani, gatti, bovini =< 200kg
NERFASIN 100mg/ml cavalli, bovini => 200kg
MEGAXILOR
ROMPUN
MEDETOMIDINA
Viene ampiamente utilizzata nel cane e nel gatto per suo effetto sedativo
ed analgesico. Permette il risparmio degli anestetici.
Agonista altamente selettivo dei recettori alfa 2-adrenergici:
MEDETOMIDINA >>> ROMIFIDINA > XYLAZINA.....(selettività)
specialità:
MEDETOR
DOMITOR
DORMILAN
SEDATOR
(solo ad uso del veterinario no vendita al pubblico)
Antagonista alfa 2: atipamezolo (ANTISEDAN, REVERTOR) …risveglio
DETOMIDINA (DOMOSEDAN)
ALFA-2-AGONISTA ; ALFA-SIMPATOMIMETICO
La detomidina stimola direttamente i recettori alfa-2-adrenergici al livello del SNC , blocca trasmissione dell'impulso dolorifico a livello
centrale esplicando potente effetto analgesico. Inoltre, la detomidina possiede notevoli proprietà sedative e tranquillanti senza essere
ipnotica.
In forma di sale, detomidina cloridrato ,si somministra per via IM o EV. Si assorbe rapidamente (Tmax 15-30 min) , la distribuzione è veloce
(Vd 0,75l/kg-1,89l/kg); legame proteico 75%-85%; è metabolizzata principalmente nel fegato e una parte nel rene. La maggior parte dei
metaboliti viene escreta con le urine. L'emivita della molecola è di 1-2 ore.
INDICAZIONI: Sedazione e analgesia dei equini e bovini al fine di facilitare l'esecuzione di esami clinici(endoscopia, raggi x, esplorazione
rettale e ginecologica) e di interventi di piccola chirurgia (trattamenti di ferite, tendini, capezzoli, trattamenti odontoiatrici, castrazione....)
La durata e l'intensità sono dose-dipendenti. Negli animali al di sotto dell'anno di età e nei soggetti anziani e consigliato impiego del
dosaggio minimo.
CONTROINDICAZIONI: Insufficienza cardiaca (detomidina ,alfa 2-agonista riduce frequenza cardiaca ), problemi renali ed epatici.
AVVERTENZE SPECIALI PER CIASCUNA SPECIE DI DESTINAZIONE:
BOVINI: Per evitare l'aspirazione di cibo o saliva devono essere tenuti in decubito sternale , con la testa e il colo abbassati. Inibizione della
motilità del rumine, meteorismo, possibile leggero timpanismo paralisi della lingua e aumento di glicemia e salivazione
.
CAVALLI: Aritmia cardiaca, blocco atrioventricolare, e blocco senoatriale. Qualora si vuole ottenere un buon livello di analgesia perianale
utilizzare esclusivamente la via EV. In modo transitorio detomidina inibisce la motilità intestinale quindi si dovrebbe utilizzare con cautela
nei cavalli con sintomi di colica o di occlusione intestinale.
SOVRADOSAGGIO: In caso di sovradosaggio si possono verificare : aritmia cardiaca, ipotensione, ritardo del risveglio, depressione del SNC e
respiratoria. In cavallo si può osservare la sudorazione e pilo erezione. Nello stallone e nel castrone si può inoltre notare un parziale e
transitorio prolasso del pene .
Trattare ,in caso di sovradosaggio con atropina e fentolamina
TEMPO DI ATTESA: Bovini -carne e visceri :48 ore
latte 48 ore (4 mungiture)
Equini-carne e visceri: 48 ore
uso non consentito in equidi che producono latte per consumo umano..
Lezione di medicina
Prof: "Il paziente si è fratturato un femore e zoppica; tu
cosa faresti?»
Studente: «Zoppicherei anch'io!»

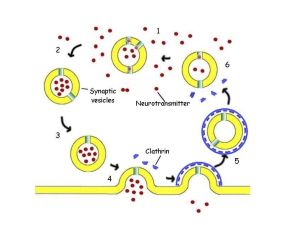









![Programma Neurofisiologia_2010-11[1].](http://s1.studylibit.com/store/data/000071347_1-39cbf1a3601124c6f49c1089fb9f3492-300x300.png)
