Informazioni dal
Servizio Farmaceutico Territoriale
Anno XII, N°4
Periodico di informazione per Medici & Farmacisti
A cura del
DIP. INTERAZIENDALE
ASSISTENZA FARMACEUTICA
Dicembre 2012
La nuova scheda di
Farmacovigilanza
Via Berchet, 10 - Padova
Dir. Dr.ssa Anna Maria Grion
Segreteria: 049-821.5101
Fax:
049-821.5105
[email protected]
Regolamento UE n. 1235/2010, Regolamento di esecuzione UE n. 520/2012, Direttiva UE 2010/84
La nuova normativa europea in materia di farmacovigilanza è stata modificata con l’adozione nel 2010, del Regolamento UE 1235/2010, la cui applicazione è divenuta operativa dal 2 luglio 2012, e della Direttiva 2010/84/UE, attualmente in fase di recepimento.
Farmacisti:
- Dr.ssa Francesca Bano
- Dr.ssa Michela Galdarossa
- Dr Umberto Gallo
- Dr.ssa Francesca Mannucci
Di seguito si riportano alcune novità apportate dalle nuove direttive europee che interessano il medico.
Il presente notiziario e i precedenti
numeri sono consultabili al sito
www.ulss16.padova.it
nella sezione servizi sovradistrettuali
⇒ Assistenza Farmaceutica Terr.
Nuova definizione di reazione avversa
È cambiata la definizione di reazione avversa intesa ora come “effetto nocivo e non voluto conseguente all’uso di un medicinale”. Questa nuova definizione consente al medico di segnalare, oltre alle reazioni avverse che derivano dall’uso di un medicinale entro i
termini di autorizzazione all’immissione in commercio (AIC), anche tutte quelle che si
manifestano a seguito dell’uso di un medicinale al di fuori dei termini dell’AIC, ossia:
Sommario:
Overdose: somministrazione di una quantità di medicinale, assunta singolarmente
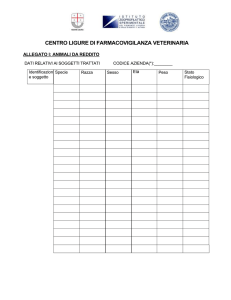
Nuova scheda di Farmacovigilanza
1
Informazioni su medicinali
a base di topiramato e
levetiracetam
4
Abolizione Piano Terapeutico per gli inibitori dell’aromatasi
4
Esenzione 013 e prescrizioni di dispositivi per
diabetici
4
o cumulativamente, superiore alla massima dose raccomandata secondo le informazioni presenti nell’AIC.
Uso off-label: impieghi del medicinale usato intenzionalmente per finalità medi-
che non in accordo con le indicazioni di impiego autorizzate. In questo ambito ricadono anche le reazioni avverse che si manifestano per impieghi terapeutici con
dosaggi o vie di somministrazione diverse da quelle riportate nell’AIC del farmaco.
Misuso: situazioni in cui il medicinale è usato intenzionalmente ed in modo inap-
propriato secondo le indicazioni di impiego autorizzate (es. inosservanza da parte
del paziente della posologia prescritta dal medico).
Abuso: intenzionale uso eccessivo del medicinale, sporadico o persistente, accom-
pagnato da effetti dannosi fisici o psicologici.
Esposizione occupazionale: esposizione ad un medicinale come risultato di un
Allegato: scheda di
farmacovigilanza
impiego professionale o non professionale.
È stato stimato che il 5% di tutti gli accessi in ospedale sono dovuti a reazioni avverse
(ADRs), che il 5% di tutti i pazienti già ricoverati in ospedale presenta una ADR e che le ADRs
sono al quinto posto tra le cause di morte in ospedale. Pertanto, la nuova regolamentazione
europea in tema di farmacovigilanza ha come obiettivo quello di promuovere e proteggere la
salute pubblica, riducendo il numero e la gravità delle ADRs e migliorando l’uso dei medicinali
attraverso diversi tipi di intervento.
Pagina 2
Anno XII, N°4
La nuova scheda di farmacovigilanza
Attualmente, e fino al completamento da parte dello Stato
italiano dell’iter normativo di recepimento della normativa
europea, è consentito utilizzare indifferentemente sia il
precedente che il nuovo modello di scheda di segnalazione. Entrambi i modelli sono presenti sul portale AIFA, uno
come scheda cartacea l’altra come scheda “elettronica”
entrambe di fatto utilizzabili su carta.
covigilanza (RNF) da parte del referente di farmacovigilanza individuato in ciascuna Azienda ULSS/Ospedaliera. Periodicamente, tutte le informazioni presenti nella RNF sono trasmesse all’ente europeo Eudravigilance che provvede all’analisi di tutte le reazioni avverse comunicate dai
Paesi membri dell’UE per l’aggiornamento del profilo di
sicurezza di tutti i medicinali commercializzati.
In questa fase di transizione è comunque preferibile
usare già la nuova scheda in quanto più completa (v.
allegato).
La scheda di segnalazione, dopo una valutazione della sua
completezza, viene inserita nella Rete Nazionale di Farma-
I dati delle reazioni avverse sono accessibili a
qualunque
operatore
sanitario
al
sito
www.adrreports.eu
La qualità e la completezza delle informazioni riportate nella scheda sono fondamentali dal momento che una scheda
incompleta non consente di valutare il nesso di causalità tra farmaco e reazione osservata. In particolare, l’inserimento di
una scheda nella RNF, da parte del referente di Farmacovigilanza, impone la compilazione obbligatoria - da parte del
medico segnalatore - dei campi di seguito riportati (tra parentesi quadrata sono indicati i punti corrispondenti nella scheda).
Data di nascita o età del paziente [2] e Sesso [3]
Data di insorgenza della reazione [4]
A questo proposito si precisa che l’indicazione della data
di nascita invece dell’età, risulta essere particolarmente
importante in caso di segnalazione di reazioni avverse a
vaccino: infatti, le vaccinazioni dell’età evolutiva vengono somministrate, di norma, ad età prestabilite. Le iniziali, insieme alla data di nascita e il sesso, consentono di
distinguere i casi, operazione necessaria soprattutto in
occasione di segnalazioni di cluster di reazioni avverse da
vaccini derivanti da una stessa struttura.
La data di insorgenza della reazione insieme alle date di
inizio e fine terapia sono indispensabili perché consentono di stabilire la correlazione temporale tra assunzione
del farmaco e reazione avversa.
Descrizione della reazione avversa [6; 7]
− è fatale;
È opportuno che tale descrizione avvenga nel modo più
chiaro possibile considerato che la descrizione dovrà poi
essere interpretata e codificata da un altro operatore
all’atto dell’inserimento della scheda nella RNF.
Come precedentemente indicato, la nuova definizione di
reazione avversa prevede che vengano segnalate anche
le reazioni osservate per effetto di abuso, misuso, uso
off-label, sovradosaggio ed esposizione professionale. In
questi casi, nel punto 7 della scheda, il segnalatore dovrà
biffare la fattispecie. Se si sospetta che la reazione sia da
imputarsi a una interazione con altri farmaci concomitanti, andrà segnalata nell’apposita casella.
Si ricorda infine che anche la mancanza di efficacia va
considerata come una reazione avversa e come tale segnalata.
Gravità della reazione [8]
La gravità di una reazione non deve essere stabilita su
base soggettiva; una reazione si definisce grave solo se:
− ha provocato o prolungato l’ospedalizzazione;
− ha provocato invalidità grave o permanente;
− ha messo in pericolo la vita del paziente;
− ha provocato anomalie congenite o difetti alla nascita
in neonati le cui madri avevano assunto i farmaci sospetti in gravidanza.
In quest’ultimo caso la scheda andrà compilata con i dati
della madre, ma alla scheda stessa dovrà essere allegata
un’accurata relazione clinica oltre ai dati anamnestici
dettagli la reazione a carico del feto o del neonato e l’esito della stessa.
E’ stata aggiunta anche la voce “altra condizione clinicamente rilevante” per poter specificare i casi di reazioni
avverse clinicamente importanti che non necessariamente determinano un ricovero (es. broncospasmo allergico
trattato a domicilio, comparsa di discrasia ematica, ecc.).
Pagina 3
Anno XII, N°4
Farmaco sospetto [12]
La segnalazione spontanea di una sospetta reazione avversa consente di raccogliere importanti informazioni sulla sicurezza dei medicinali e di individuare precocemente possibili segnali di allarme correlati al loro uso.
Si ricorda l’importanza di segnalare ogni volta si sospetti che il farmaco usato possa aver causato un
effetto non voluto, tenendo presente che non è richiesta la completa certezza.
È importante riportare il nome commerciale del farmaco (e relativo dosaggio) e non solo il principio attivo sia per consentire eventuali accertamenti legati alla produzione dello stesso sia per consentire alle aziende farmaceutiche titolari
del farmaco sospetto di assolvere ai numerosi obblighi di farmacovigilanza nazionale ed internazionale previsti dalla normativa. Pertanto, nel caso dei farmaci equivalenti, al nome del principio attivo deve essere aggiunto il nome dell’azienda. Senza questa informazione non sarà possibile procedere all’identificazione del medicinale coinvolto.
⇒ Segnalazione di reazioni avverse da vaccini: in questo caso è necessario riportare anche l’ora della somministrazione
ed il numero di dose (I, II III o di richiamo), la sede dove è avvenuta la vaccinazione (ASL, studio privato, scuola, ecc.)
ed il sito di inoculo del vaccino.
⇒ Segnalazione di reazioni avverse da farmaci biologici: anche in questo caso è necessario che il segnalatore riporti il
numero del lotto.
Qualifica del segnalatore [36] e identificazione [37]
Data di inizio e fine terapia [16]
Analogamente alla data di insorgenza di reazione, anche
la data di inizio e fine di terapia sono elementi necessari
per l’attribuzione di causalità tra reazione e farmaco. Se
non è noto l’esatto giorno di inizio della terapia è sufficiente riportare il primo giorno del mese.
Il segnalatore deve essere chiaramente identificabile,
anche se i suoi dati sono tutelati, in primo luogo perché
spesso c’è la necessità di contattare il segnalatore per
chiarimenti o follow-up ed inoltre non sono accettabili
schede anonime. Qualora la fonte venga riportata come
“Altro” deve essere specificato chiaramente la tipologia
di segnalatore.
A chi inviare la scheda di farmacovigilanza
Per inviare una segnalazione di sospetta reazione avversa si potrà utilizzare il modulo allegato (fronte-retro) o, in alternativa, la scheda “elettronica” che può essere scaricata dal sito dell’AIFA al seguente indirizzo:
http://www.agenziafarmaco.gov.it (sezione: “Segnalazioni reazioni avverse”)
La scheda dovrà essere quindi inviata al proprio referente aziendale di farmacovigilanza tramite fax o per posta elettronica.
Di seguito sono riportati i nominativi dei referenti di farmacovigilanza di Padova con relativi recapiti.
Referente
Struttura/Sanitari
Umberto Gallo
Tel.
Fax
Mail
Ospedali e strutture dell’ULSS 049-821.5116
16, (compresi MMG, PLS, medici privati e convenzionati, farmacie del territorio)
049-821.5105
[email protected]
Antonella Alberti
Azienda Ospedaliera di Padova
049-821.2343
049-821.2827
[email protected]
Angelo Palozzo
Istituto Oncologico Veneto
049-821.5840
049-821.5836
[email protected]
Pagina 4
Anno XII, N°4
Medicinali a base di levetiracetam e topiramato
Circ. Regione Veneto n. 475889 del 19/10/2012
In data 17/09/2012 è scaduto il brevetto delle specialità
Keppra® (levetiracetam) e Topamax® (topiramato) con
conseguente immissione nel ciclo distributivo dei farmaci
equivalenti il cui prezzo risulta inferiore rispetto a quello
delle specialità suddette.
Con nota prot. n. 475889 del 19/10/2012 la Regione Veneto, al fine di esonerare i pazienti dal sostenere la compartecipazione alla spesa, ha previsto che - nei casi in cui il
medico ritenga indispensabile ricorrere/mantenere la
prescrizione della specialità - il medicinale venga erogato
tramite distribuzione diretta dell’azienda ULSS di appartenenza dell’assistito limitatamente ai soggetti in possesso
dell’esenzione per reddito 6R2. In questi casi, il medico
dovrà indicare in ricetta la non sostituibilità del medicina-
le e indirizzare l’assistito a ritirare il farmaco tramite distribuzione diretta.
Alla luce di quanto sopraesposto si chiede ai medici prescrittori:
per i pazienti naive a intraprendere il trattamento con
il medicinale equivalente;
per i pazienti già in trattamento con la specialità di va-
lutare la sostituzione con il farmaco equivalente, mantenendo l’uso del prodotto “brand” solamente quando
necessario (soggetti in trattamento completamente
stabilizzati o che abbiano sensibili miglioramenti in termini di frequenza e tipologia delle crisi). In questi casi il
paziente potrà essere inviato alla distribuzione diretta
solo se in possesso di un’esenzione per reddito “6R2”.
Abolizione del Piano Terapeutico
per gli inibitori dell’aromatasi
Determinazione AIFA 30 ottobre 2012 (G.U. n. 267 del 15/11/2012)
Circ. Regione Veneto n. 548566 del 03/12/2012
Con Determinazione del 30/10/2012 l’AIFA ha provveduto ad abolire l’obbligo del Piano Terapeutico per tutti i seguenti
medicinali a base di inibitori dell’aromatasi (specialità e relativi generici): anastrozolo (Arimidex®), exemestan
(Aromasin®) e letrozolo (Femara®).
Questi farmaci, pertanto, restano prescrivibili in classe A nel trattamento del carcinoma mammario in pazienti con recettori estrogenici positivi.
Esenzione 013 e presidi per diabetici
DGRV n. 1806 del 08/11/2011
Si ricorda a tutti i medici che, con DGR n. 1806 del 08/11/2011, la Regione Veneto ha provveduto a modificare le tariffe
di rimborso dei presidi diabetici (strisce reattive, aghi pungidito/iniettori e siringhe) sulla base di un parere della Direzione Centrale dell’Agenzia delle Entrate in merito al regime di IVA applicabile alle forniture effettuate a carico del SSR.
In particolare, con risoluzione del 25/05/2010, l’Agenzia ha provveduto a chiarire che l’aliquota IVA del 4%, in luogo di
quella ordinaria del 21%, può essere applicata qualora l’acquisto dei prodotti in oggetto venga effettuato esclusivamente
a favore di “soggetti diabetici con menomazione funzionale permanente”.
La Regione Veneto, con la succitata delibera, ha ritenuto che tale condizione sia soddisfatta solamente qualora nella ricetta il medico indichi la codifica dell’esenzione per patologia 013.
Pertanto - ferme restando le vigenti modalità di prescrizione e dispensazione dei dispositivi in oggetto affinché questa Azienda ULSS possa beneficiare della suddetta agevolazione fiscale, i medici prescrittori sono
tenuti ad apporre, nel relativo campo della ricetta SSN, il codice di esenzione 013 per tutti i soggetti
diabetici che ne sono in possesso.