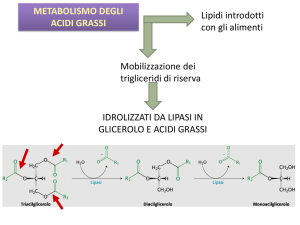
LEZIONE DEL 15/05/2017
PRIMA DELLA BETA OSSIDAZIONE – L'INTERVENTO DEL
TRASPORTATORE
Dato che un acido grasso non può attraversare
direttamente la prima e la seconda membrana usufruirà
di una CARNITINA ACIL TRANSFERASI 1 per la prima e
una CARNITINA ACIL TRANSFERASI 2 per la seconda.
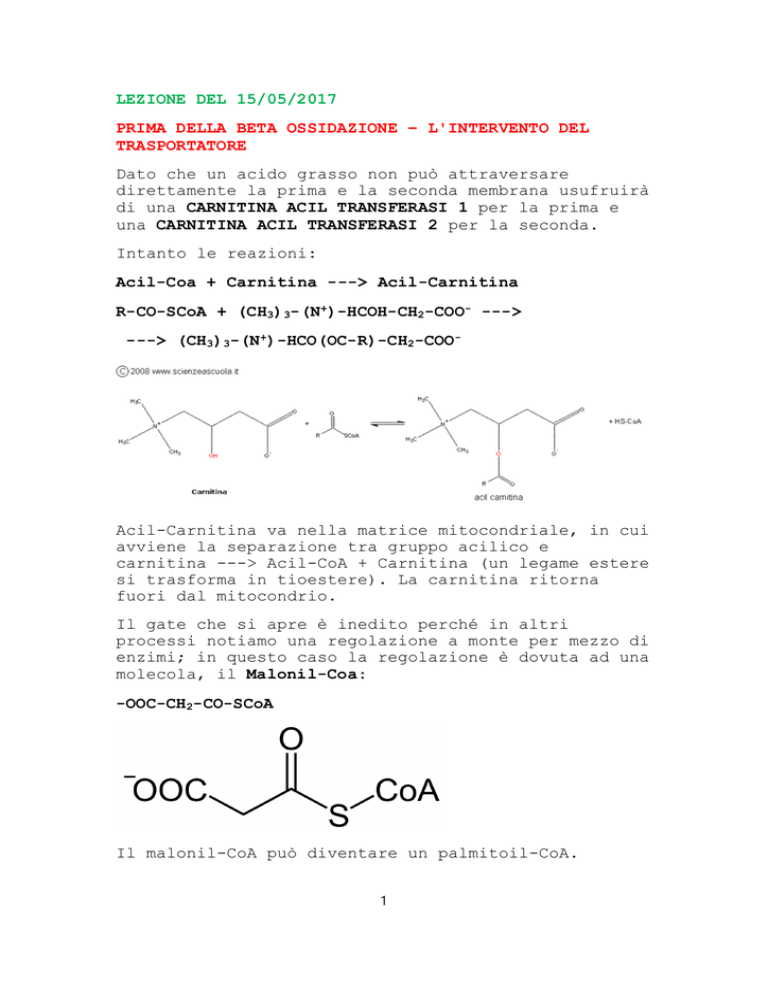
Intanto le reazioni:
Acil-Coa + Carnitina ---> Acil-Carnitina
R-CO-SCoA + (CH3)3-(N+)-HCOH-CH2-COO- --->
---> (CH3)3-(N+)-HCO(OC-R)-CH2-COO-
Acil-Carnitina va nella matrice mitocondriale, in cui
avviene la separazione tra gruppo acilico e
carnitina ---> Acil-CoA + Carnitina (un legame estere
si trasforma in tioestere). La carnitina ritorna
fuori dal mitocondrio.
Il gate che si apre è inedito perché in altri
processi notiamo una regolazione a monte per mezzo di
enzimi; in questo caso la regolazione è dovuta ad una
molecola, il Malonil-Coa:
-OOC-CH2-CO-SCoA
Il malonil-CoA può diventare un palmitoil-CoA.
1
Tramite desaturasi e longasi in generale gli acidi
grassi si possono allungare, accorciare, cambiare
natura. Il massimo di carboni di un acido grasso
sintetizzabile nel corpo umano è di 20-22. Oltre i 22
dobbiamo assumerli.
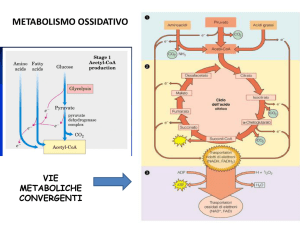
Acetil-CoA:
⦁ Ricomincia;
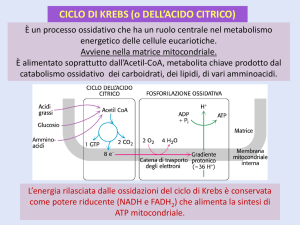
⦁ Krebs;
⦁ Biosintesi di altre sostanze (tipo biosintesi
colesterolo);
⦁ Corpi chetonici.
CARENZA DI ZUCCHERI : IPOGLICEMIA - per una dieta
sbagliata o per induzione da diabete. In tale
condizione le cellule sono costrette a estrarre
energia dai grassi per produrre acetil-CoA. Inoltre
manca l’ossalacetato in quanto è stato usato per la
gluconeogenesi (se non c'è, non inizia Krebs). Si
crea un intasamento di acetil-CoA nel fegato.
CHETOGENESI
E' il processo che permette di risolvere due
problemi:
1. L’eliminazione dell’acetil-CoA in eccesso;
2. La produzione di un nuovo combustibile, diverso
dai carboidrati ( 3 molecole di acetil-CoA sono
impiegate per sintetizzare).
LA CHETOGENESI (via che porta alla formazione di
copri chetonici a partire da acetil-CoA); due
molecole di acetil-CoA vengono usate all'inizio; solo
insieguito, abbiamo l'intervento di una terza.
Quando i livelli di ossalacetato sono bassi due
molecole di acetil-coA vengono unite per formare
aceto-acetil-CoA , liberando CoA-SH in una reazione
inversa alla tiolasi sostenuta da β-chetotiolasi. Se
si aggiunge un’altra acetil-CoA, con la catalisi
dell’HMG-CoA SINTASI si ottiene il β-idrossi-βmetilglutaril-CoA . Questo è avvenuto nel
mitocondrio. Nel citosol avviene una reazione
analoga, in cui l'HMG citosolico, per mezzo di un
2
isoenzima alla sintesi di colesterolo.
Notiamo quindi che i processi sono
compartimentalizzati. L'HMG-CoA implica perdita di
energia per rigenerazione di grassi. Questo CoA
potrebbe essere infatti implicato nel ciclo di Krebs.
L'HMG-COA per mezzo dell'HMG-CoA liasi libera AcetilCoA e dà un corpo chetonico, l'acetoacetato. Per ogni
3
corpo chetonico si perdono 2 acetil-CoA; uno lo
recupero alla fine attraverso questa reazione.
L'acetoacetato si può trasformare in altri corpi
chetonici, mediante strade differenti. Nella prima
diventa acetone (propanone) per decarbossilazione in
parte spontanea. L'acetone è volatile – arriva nei
polmoni e viene espulso. Quando lo zucchero non
riesce ad entrare nel muscolo o nel tessuto adiposo
sono di fronte a problemi del trasportatore GLUT 4
nel fegato a causa di insulina. Se l'insulina la
produco male, non la produco, il recettore è
rovinato, oppure le cellule di Langrance non
funzionano, allora posso considerare le rispettive
casistiche di diabete. Quindi, se non c'è
trasferimento di zucchero, ciò induce la chetogenesi.
Vediamo la seconda strada dell'acetoacetato. Avviene
in tale contesto una deidrogenazione NADH dipendente
in cui ottengo NAD ridotto e beta-idrossi-butirrato
(è improprio chiamarlo gruppo chetonico).
I corpi chetonici sono rilasciati dal fegato nel
sangue affinché raggiungano tessuti extraepatici.
Sono dunque trasportati facilmente ad altre cellule e
vengono facilmente intercettate in particolare dalle
cellule nervose in assenza di zucchero. Nei tessuti
extraepatici i chetonici sono riconvertiti in acetilCoA, che vanno a finire in Krebs.
Ora il betaidrossibutirrato è riconvertito ad
acetoacetato tramite ossidazione di NAD (che a
livello energetico vale 2.5 ATP) e tramite il
prestito di CoA-SH da succinil-CoA si formano
succinato e acetoacetil-CoA. Sto facendo in pratca il
processo a ritroso. Il prestito del succinil-CoA
maschera la perdita di un GTP e dunque la mancata
produzione di un ATP. L'acetoacetil CoA tramite
tiolasi e intervento di un altro CoA-SH mi dà 2
molecole di acetil-CoA.
Ma come fa il CoA-SH ad entrare nel ciclo di Krebs se
non c’è ossalacetato? In realtà l’ossalacetato non
manca: nelle cellule è presente in piccole quantità
in modo costante. Infatti è il fegato che non fa
entrare il CoA-SH nel TCA. Siamo in due luoghi
diversi.
Il diabete non curato porta all'accumulazione di
acetil-CoA che accelera la produzione di corpi
chetonici ben oltre la capacità dei tessuti
4
extraepatici (in cui in parte sono riconvertiti in
acetil-CoA). L'eccesso mi fa aumentare la
concentrazione di corpi chetonici, che sono acidi
quindi inducono acidosi del sangue (abbassamento di
pH che mi denatura proteine, enzimi fondamentali) e
infine coma (eventualmente diabetico).
La beta-ossidazione mi produce NAD, FAD che vanno
nella catena respiratoria; viene immesso ossigeno con
produzione di acqua se proviene da acidi grassi.
β – OSSIDAZIONE DI ACIDI GRASSI MONOINSATURI
consideriamo l’acido oleico 18: 1 Δ9 la cui forma
attivata è l’oleil-CoA
CH3-(CH2)7-HC=CH-(CH2)7-CO-SCoA
Dopo tre cicli la catena si ritrova con il doppio
legame sul carbonio α (in posizione cis) questo
composto non può subire un’ulteriore β-ossidazione in
quanto l’enzima che reagirebbe normalmente riconosce
solo i legami trans. Allora abbiamo il seguente
processo:
5
OSSERVAZIONE: in questo caso il primo passaggio della
β- ossidazione non è stato effettuato: una molecola
di FADH2 manca ed è stata prodotta meno energia. Per
questo motivo possiamo notare che l’acido stearico è
più energetico dell’acido oleico ( si perde
l’ossidazione del FADH2)
ESEMPI.
1. RESA ENERGETICA DELL'ACIDO STEARICO 18:Δ0
18/2 = 9 acetil-CoA ---> 9 x 3NADH x 2,5 = 67,5 ATP;
9 x 1FADH2 x 1,5 = 13,5 ATP; 9 x 1GTP = 9ATP
18/2 -1 = 8 FADH2 x 2,5 = 20 ATP
18/2-1 = 8 NADH x 1,5 = 12 ATP
67,5+13,5+9+20+12= 122
ATTIVAZIONE: - 2ATP perché ATP ---> AMP ALLORA 122-2=
120
2 . RESA ENERGETICA DELL’ACIDO OLEICO 18: 1Δ9
18/2 = 9 acetil-CoA ---> 9 x 3NADH x 2,5 = 67,5 ATP;
9 x 1FADH2 x 1,5 = 13,5 ATP; 9 x 1GTP = 9ATP
18/2 -1 = 8 FADH2 x 2,5 = 20 ATP
18/2-2 = 7 NADH x 1,5 = 10.5 ATP
67,5+13,5+9+20+10,5= 120,5 . ATTIVAZIONE: 120,5 -2 =
118,5
β – OSSIDAZIONE DEGLI ACIDI GRASSI A CATENA DISPARI
In questo caso sono necessarie altre tre reazioni per
concludere la β – ossidazione. Procede per n-1 cicli
producendo n-1 FADH2, n-1 NADH, n-1 acetil-CoA e una
molecola di propionil-CoA. Il propionil-CoA, tramite
la carbossilasi viene trasformato in metimalonilCoA :
propionil-CoA + HCO3 - + ATP ---> D-metilmalonil-CoA
+ ADP + Pi
il D-metilmalonil-CoA viene epimerizzado dalla
metilmalonil-CoA epimerasi in L-metilmalonil-CoA.
6
Quest’ultima viene trasformata in succinil-CoA
tramite una metilmalonil-CoA mutasi.
Il succinil-CoA:
1) nel fegato: ossalacetato ---> sintesi Glc;
entriamo già con succinil-CoA, produciamo dunque più
ossalacetato, che non riutilizzerò nel ciclo di
Krebs;
2) non produco ossalacetato – vado nel citosol -->
piruvato --> mitocondrio,
REAZIONI DELLA MUTASI – GENERALMENTE NON NECESSITANO
DI COFATTORI
1. Il protone viene scambiato con il solvente;
2. Il cofattore richiede il coenzima derivante
dalla vitamina B12 contenente il cobalto;
7
3. La vitamina B12 è intercettata dal FATTORE
INTRINSECO (sintetizzata da alcuni
microorganismi);
4. La vitamina B12 ha una struttura molto
complessa (sono presenti nucleotidi)
5. L’ATP perde 3 gruppi Pi, legandosi al CO3+ .
Curiosità: D. Hodking risolse la struttura della
vitamina B12 nel 1956, due anni prima che venisse
risolta quella della mioglobina!!!
L’ANEMIA PERNICIOSA
Si tratta di una forma di anemia megaloblastica,
ipercromica, cronica e progressiva per gli adulti
dovuta ad un diminuito assorbimento della vitamina
B12, importante per la maturazione degli eritrociti,
contenuta nella carne e nel latte. In questo caso il
fattore intrinseco intestinale è assente. A tele tipo
8
di anemia sono collegate:
1. Una scarsa produzione di eritrociti
2. Bassa emoglobina
3. Danni al sistema nervoso.
Oggi si pone rimedio al problema sintetizzando B12 in
laboratorio.
9