OGGETTO: FARMACOVIGILANZA
- Nota informativa AIFA-EMEA sulla revisione delle raccomandazioni per il trattamento con Fabrazyme®
(Agalsidasi Beta) in seguito alla ulteriore riduzione della disponibilità del medicinale
- Pandemia influenzale – segnalazioni di reazioni avverse a vaccini pandemici e farmaci antivirali
- Nota informativa AIFA-EMEA sulla sicurezza d’uso di INTELENCE® (Etravirina)
- Nota informativa AIFA-EMEA sulla sicurezza d’uso di RELENZA® (Zanamivir) e di METHOTREXATE®
PAROLE CHIAVE:
METHOTREXATE®
FABRAZYME® –
PANDEMIA INFLUENZALE - INTELENCE® - RELENZA® -
ABSTRACT- NOVITA’ DI RILIEVO
FABRAZYME®: specialità medicinale classificata H OSP1, a base del principio attivo Agalsidasi Beta,
indicata per il trattamento della malattia di Fabry.
L’EMEA segnala che la carenza delle scorte di Fabrazyme® è più grave di quanto previsto e sono pertanto
necessarie ulteriori restrizioni alle raccomandazioni per il trattamento, indicate precedentemente ( Nota ASL
prot. n. U/111439 del 27/7/2009).
PANDEMIA INFLUENZALE: la Direzione Generale Sanità della Regione Lombardia raccomanda a tutti i
professionisti sanitari di segnalare eventuali reazioni avverse insorte a seguito di somministrazione di vaccini
pandemici e di farmaci antivirali.
La tempestiva conoscenza di eventuali gravi reazioni avverse insorte a seguito della somministrazione di
vaccini pandemici e di farmaci antivirali, soprattutto in segmenti di popolazione di norma non esposta a questi
farmaci (bambini, donne gravide, immunodepressi, ecc) consentiranno alle Autorità Regolatorie di adottare
misure utili a migliorarne il profilo di sicurezza.
L’AIFA ha predisposto una scheda apposita per la segnalazione di reazioni avverse a vaccini pandemici che è
disponibile sul portale dell’AIFA e che alleghiamo alla presente Nota.
Sul portale dell’AIFA è inoltre disponibile una sezione dedicata all’influenza A(H1N1), ai Vaccini, agli Antivirali
e alla Farmacovigilanza, che viene costantemente aggiornata e che invitiamo a consultare.
INTELENCE®: specialità medicinale classificata in classe “C”, a base del principio attivo Etravirina, antivirale
per uso sistemico.
Si segnala che, associati all’uso di INTELENCE, sono stati segnalati casi di rash da farmaco, con eosinofilia e
sintomatologia sistemica (sindrome di DRESS) e casi di necrolisi tossica epidermica (TEN). Data l’importanza
clinica di tali reazioni avverse è stato aggiornato il Riassunto delle Caratteristiche del Prodotto.
RELENZA®: specialità medicinale in classe “C”, a base del principio attivo Zanamivir, antivirale per uso
sistemico.
A seguito della segnalazione di un errore terapeutico che ha causato il decesso di un paziente affetto da
influenza, trattato con il farmaco solubilizzato e somministrato attraverso ventilazione meccanica, si evidenzia
che la formulazione di Relenza® in polvere per inalazione non è idonea alla ricostituzione per l’impiego in
nebulizzatori o nella ventilazione meccanica.
METHOTREXATE®: specialità medicinale classificata in classe “A”, a base del principio attivo Methotrexate
appartenente al gruppo dei farmaci antineoplastici e immunomodulatori.
A seguito della segnalazione di casi di tossicità, alcuni dei quali con esito fatale, insorti in pazienti trattati con
farmaco sovradosato, si forniscono importanti informazioni di sicurezza relativamente al dosaggio e alla
somministrazione appropriata del Methotrexate®.
ADEMPIMENTI
FABRAZYME®: I Medici devono tenere presente le nuove raccomandazioni straordinarie per il trattamento,
concordate con l’EMEA, che prevedono che debbano ricevere un dosaggio ridotto di Fabrazyme® non solo le
pazienti di sesso femminile, ma anche i pazienti di sesso maschile. Le segnalazioni di eventi avversi relativi a
Fabrazyme® devono essere trasmesse seguendo la normale prassi e riportando il numero di lotto utilizzato.
PANDEMIA INFLUENZALE: Medici, Farmacisti e gli altri operatori sanitari devono segnalare gli eventi
avversi/reazioni al vaccino FOCETRIA® (utilizzato nella prima fase della pandemia) o a vaccino della
Sanofi (disponibile dal 2010) utilizzando la scheda semplificata, predisposta dall’AIFA e allegata alla
presente Nota, compilabile anche a video.
Devono essere obbligatoriamente segnalate:
- reazioni avverse mortali o che mettono in pericolo di vita
- reazioni avverse gravi ed inattese
- eventi avversi noti di particolare interesse: neuriti, convulsioni, anafilassi, encefalite, vasculiti, sindrome di
Guillain-Barrè, paralisi di Bell, disordini demielinizzanti, fallimenti vaccinali.
Medici, Farmacisti e gli altri operatori sanitari devono segnalare ogni sospetta reazione avversa a farmaci
antivirali, utilizzando la scheda unica di segnalazione di reazione avversa ai medicinali attualmente in
uso (D.M. 12/12/2003), allegata alla presente Nota, compilabile anche a video.
Nella scheda, il nome del farmaco dovrà essere riportato nel seguente modo:
- Tamiflu® per il farmaco prodotto dalla ditta Roche S.p.A.
- Oseltamivir se si tratta del farmaco prodotto dallo Stabilimento Chimico Farmaceutico Militare di Firenze
- Relenza® per il farmaco prodotto dalla ditta Glaxo Smith Kline S.p.A.
Rimangono invariate tutte le altre modalità di segnalazione di reazioni avverse a farmaci e a vaccini,
attualmente in uso.
Medici, Farmacisti e gli altri operatori sanitari, devono segnalare eventuali sospette reazioni avverse al
Responsabile di Farmacovigilanza della Struttura Sanitaria di appartenenza che, per l’ASL di Bergamo è:
Dr.ssa Laura Spoldi – Via Borgo Palazzo 130, Bergamo – tel: 035/2270304, fax: 035/270035.
INTELENCE®: i Medici devono tenere conto delle nuove informazioni di sicurezza
RELENZA®: i Medici devono utilizzare Relenza® polvere inalatoria, come previsto nel Riassunto delle
Caratteristiche del Prodotto, mediante l’uso del dispositivo Diskhaler fornito con il prodotto stesso.
METHOTREXATE®: i Medici devono scrupolosamente informare i pazienti e il personale sanitario, per
assicurarsi che il farmaco sia somministrato nella maniera appropriata. I Medici devono prestare attenzione
nel calcolo dell’area di superficie corporea al fine di prevenire il sovradosaggio, specialmente nei giovani e
nei pazienti trattati per malattia neoplastica.
E’ indispensabile la consultazione del “Modello semplificato per le segnalazioni di sospette reazioni
avverse a vaccini pandemici “
- Nota informativa AIFA-EMEA: “Comunicazione diretta agli operatori sanitari sulla revisione delle
raccomandazioni straordinarie per il trattamento con Fabrazyme® (agalsidasi beta) in seguito alla ulteriore
riduzione della disponibilità medicinale”
- Comunicato stampa EMEA: “Carenza delle scorte del medicinale Fabrazyme®. Aggiornamento delle
raccomandazioni per il trattamento nei pazienti adulti di sesso maschile”
- Domande e risposte sulle raccomandazioni aggiornate per il trattamento con Fabrazyme®.
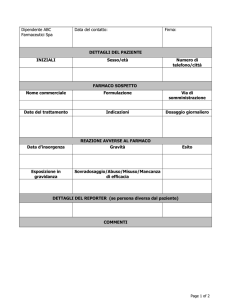
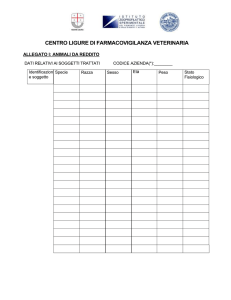
- Modello semplificato per le segnalazioni di sospette reazioni avverse a vaccini pandemici, compilabile a
video
- Scheda unica di segnalazione di reazione avversa ai medicinali ( D.M. 12/12/2003), compilabile a video
- Nota informativa AIFA-EMEA : “Necrolisi tossica epidermica (TEN) e rash da farmaco con eosinofilia e
sintomatologia sistemica (sindrome DRESS) associati all’uso di INTELENCE® (Etravirina)
- Nota informativa AIFA-EMEA : “RELENZA® (Zanamivir) polvere per inalazione, non deve essere utilizzata
per la nebulizzazione
- Informazioni importanti sulla sicurezza relative al dosaggio del Methotrexate®
- Allegato 1 Posologia Methotrexate®
RESPONSABILE DEL PROCEDIMENTO: Dr.ssa Laura Spoldi tel 035.2270755
Per informazioni rivolgersi a:
FARMACISTA DELEGATA PER LA FARMACOVIGILANZA: Dr.ssa Maria Pia Orsi tel 035.2270763 e-mail:
[email protected]