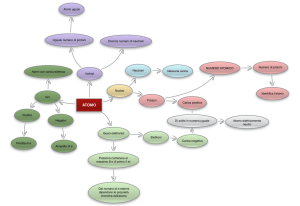
ATOMI E MOLECOLE
La materia è costituita da piccolissime particelle: GLI ATOMI
che si possono raggruppare formando MOLECOLE
GLI ELEMENTI
Gli elementi sono formati da uno o più atomi tutti uguali (idrogeno, ossigeno, azoto..)
Un elemento è una sostanza pura che non può essere scomposta in sostanze più
semplici e non può essere ottenuta per unione di altre sostanze. Attualmente si
conoscono 111 elementi, di cui 90 naturali e 20 artificiali o sintetici.
LA TAVOLA PERIODICA DEGLI ELEMENTI
Fu inventata dal chimico russo DIMITRI MENDELEEV per esigenza di classificare
gli elementi secondo le loro proprietà chimiche. In essa si possono distinguere 18
colonne (gruppi) e 7 righe (periodi). Gli elementi appartenenti allo stesso gruppo
hanno caratteristiche chimiche simili
I COMPOSTI
I composti sono sostanze formate da due o più atomi diversi, combinati in rapporti
determinati
(ammoniaca , acqua, glucosio...)
LA VALENZA
La valenza è il numero di legami che un atomo può formare con altri atomi :
l’ idrogeno ha valenza 1, l’ ossigeno ha valenza 2 , l’ azoto ha valenza 3…
Es.
L’ ossigeno ha valenza 2 perciò per formare la sua molecola i 2 atomi devono essere
legati da 2 legami
LA STRUTTURA DELL’ ATOMO
Dopo averlo considerato per molto tempo un sistema indivisibile oggi sappiamo che è
composto da particelle ancora più piccole:
I PROTONI: particelle dotate di carica elettrica positiva
I NEUTRONI: privi di carica elettrica
GLI ELETTRONI: particelle dotate di carica elettrica negativa
PROTONE
NEUTRONE
ELETTRONE
L’ atomo è un sistema elettricamente neutro.
Gli elettroni, protoni e neutroni si chiamano PARTICELLE SUBATOMICHE
Protoni e neutroni si trovano nel NUCLEO
Il numero dei protoni (e quindi degli elettroni) presenti in un atomo si chiama
NUMERO ATOMICO = Z
La somma dei protoni e dei neutroni contenuti nel nucleo si chiama
NUMERO DI MASSA = A
GLI ISOTOPI
ATOMI CHE HANNO STESSO NUMERO DI PROTONI,MA DIVERSO
NUMERO DI NEUTRONI NEL NUCLEO SI CHIAMANO ISOTOPI
(DAL GRECO ISOS = UGUALE E TOPOS = LUOGO).
Es.
L ‘ idrogeno ha 3 isotopi: idrogeno comune (PROZIO)
Idrogeno pesante (DEUTERIO)
Idrogeno radioattivo (TRIZIO)
I LEGAMI CHIMICI
I legami chimici possono essere di 2 tipi:
Legame ionico: quando gli elettroni vengono ceduti da un atomo a un altro
che li acquista
Legame covalente: quando uno o più elettroni vengono condivisi
FINE
(Sappiamo che vi è piaciuto)
Lorenzo Costantini
E
Marco Radicchi
IA
prof. Marinella Borruso