caricato da
common.user3924
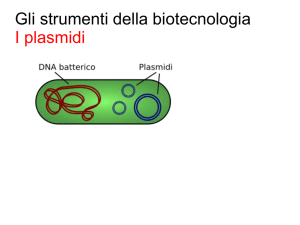
Appunti di Biotecnologie: DNA, OGM, Bioremediation

BIOTECNOLOGIE Sommario DNA e RNA (struttura, replicazione e sintesi)...............................................................................................................2 LE BIOTECNOLOGIE .......................................................................................................................................................5 Storia.........................................................................................................................................................................6 Bioetica .....................................................................................................................................................................7 BIOTECNOLOGIE TRADIZIONALI ...................................................................................................................................9 Fermentazioni ...........................................................................................................................................................9 Selezione artificiale di animali e piante ..................................................................................................................10 BIOTECNOLOGIE INNOVATIVE ....................................................................................................................................13 DNA ricombinante ..................................................................................................................................................13 Tecnica del DNA ricombinante ...........................................................................................................................13 Cellule staminali......................................................................................................................................................15 Classificazione delle cellule staminali .................................................................................................................16 Malattie curate con le cellule staminali..............................................................................................................17 Clonazione ..............................................................................................................................................................17 Tecnica di clonazione ..........................................................................................................................................18 Terapia genica.........................................................................................................................................................19 Tipologie di terapia genica..................................................................................................................................19 Stato attuale e prospettive .................................................................................................................................20 OGM agricoli e animali ...........................................................................................................................................21 Tecniche principali ..............................................................................................................................................21 Tecniche di miglioramento genetico ..................................................................................................................21 OGM nel mondo .................................................................................................................................................22 Quadro normativo ..............................................................................................................................................22 Bioremediation .......................................................................................................................................................23 Rimozione Dei Metalli.........................................................................................................................................23 Rimozione di altri composti inorganici ...............................................................................................................23 Rimozione di composti organici..........................................................................................................................23 Casi di studio .......................................................................................................................................................24 Progetto Genoma ...................................................................................................................................................25 1 DNA e RNA (struttura, cenni su replicazione e sintesi) Prima di passare a trattare in modo più approfondito i vari aspetti delle biotecnologie innovative si vuole riprendere la struttura del DNA e dell’RNA. L'acido desossiribonucleico o deossiribonucleico (DNA) è un acido nucleico che contiene le informazioni genetiche necessarie alla biosintesi di RNA e proteine, molecole indispensabili per lo sviluppo ed il corretto funzionamento della maggior parte degli organismi viventi. Dal punto di vista chimico, il DNA è un polimero organico costituito da monomeri chiamati nucleotidi (deossiribonucleotidi). Tutti i nucleotidi sono costituiti da tre componenti fondamentali: un gruppo fosfato, il desossiribosio (zucchero pentoso) e una base azotata che si lega al deossiribosio con legame N-glicosidico. Le basi azotate che possono essere utilizzate nella formazione dei nucleotidi da incorporare nella molecola di DNA sono quattro: adenina, guanina, citosina e timina. L'acido ribonucleico (RNA) è un polimero organico, risultante dalla polimerizzazione di ribonucleotidi. Chimicamente l'RNA è molto simile al DNA. Anch'esso è una catena polinucleotidica contenente quattro nucleotidi diversi. Le molecole di RNA differiscono da quelle di DNA perché: contengono lo zucchero ribosio (con un gruppo OH legato al carbonio 2') anziché il deossiribosio (da qui il nome); una delle basi, la timina (T), è sostituita dall'uracile (U). In questo caso è l'uracile la base complementare all'adenina, mentre la guanina è sempre complementare alla citosina; La catena dell’RNA è singola e non doppia come nel DNA Le molecole di RNA vengono sintetizzate attraverso un processo, conosciuto come trascrizione del DNA, dove un filamento di DNA viene ricopiato nel corrispondente filamento di RNA. Vi sono tre tipi di RNA comuni a tutti gli organismi cellulari: mRNA (RNA messaggero) che contiene l'informazione per la sintesi delle proteine; rRNA (RNA ribosomiale), che entra nella struttura dei ribosomi; tRNA (RNA transfer) necessario per la traduzione nei ribosomi. 2 Negli eucarioti, il DNA si complessa all'interno del nucleo in strutture chiamate cromosomi. Negli altri organismi, privi di nucleo, esso può essere organizzato in cromosomi o meno (nei batteri è presente un'unica molecola di DNA circolare a doppia catena, mentre i virus possono avere genomi a DNA oppure ad RNA). All'interno dei cromosomi, le proteine della cromatina come gli istoni, le coesine e le condensine, organizzano il DNA e lo avvolgono in strutture ordinate. Queste strutture guidano l'interazione tra il codice genetico e le proteine responsabili della trascrizione, contribuendo al controllo della trascrizione genica. 3 Fondamentalmente possono avvenire 2 processi legati al DNA: Replicazione del DNA (o duplicazione del DNA); Sintesi proteica; Nel primo processo l'informazione genetica è duplicata prima della divisione cellulare, attraverso un processo noto come replicazione del DNA (nella fase S della vita della cellula, passando nell’uomo, da 46 cromatidi a 46 cromosomi); con questo processo quindi, nella divisione cellulare i 46 cromosomi si divideranno in 2 gruppi di 46 cromatidi che andranno ognuno nelle due cellule figlie. Nella sintesi proteica l’informazione nel DNA viene tradotta, viene cioè utilizzata come un manuale d’istruzione per assemblare la sequenza di amminoacidi che forma le proteine (in sintesi il DNA contiene le informazioni per creare le proteine). Il processo di traduzione genetica (comunemente chiamata sintesi proteica) è possibile solo in presenza di una molecola intermedia di RNA (m-RNA o RNA messaggero), che è generata per complementarità con le quattro basi dei nucleotidi del DNA in un processo noto come trascrizione. Tale processo non genera solo filamenti di RNA destinati alla traduzione, ma anche frammenti già in grado di svolgere svariate funzioni biologiche (ad esempio all'interno dei ribosomi, dove l'RNA ha una funzione strutturale, r-RNA cioè RNA ribosomiale). 4 Riepilogando: m-RNA copia, all’interno del nucleo, il frammento di DNA. Migra verso il citoplasma (passando quindi attraverso la membrana nucleare) fino ai ribosomi (formati anche dal r-RNA). Qui inizia il processo che, traducendo il frammento di m-RNA sintetizza la proteina. Per fare ciò servono materialmente dei nucleotidi da assemblare. Questi sono sparsi nel citoplasma e vengono portati ai ribosomi dal t-RNA; qui vengono appunto assemblati per formare la nuova proteina. LE BIOTECNOLOGIE La parola “biotecnologia” è formata dal confisso “bio” (dal greco “vita”) e da “tecnologia” (da tecno che deriva dal greco “arte”, anche se in questo caso il senso è “dotato di capacità tecniche”, cioè l’uso di conoscenze e strumenti anche scientifici per la risoluzione di problemi pratici o alla presa di decisioni). La biotecnologia si riferisce quindi all'integrazione delle scienze naturali, di organismi, cellule, loro parti o analoghi molecolari, nei processi industriali per la produzione di beni e servizi (definizione del European Federation of Biotechnology, EFB). Sostanzialmente la biotecnologia consiste nella decifrazione e nell'utilizzo pratico delle conoscenze biologiche. Già nell’antichità possiamo trovare alcune forme di biotecnologia, utili ad ottimizzare il ruolo dei microrganismi. Basta pensare all’uso dei batteri lattici e lieviti per ottenere la lievitazione del pane, al caglio per produrre il formaggio o ai processi fermentativi di birra e vino. Ci sono due scuole di pensiero su cosa sia la biotecnologia. Entrambi usano gli organismi per aiutare l’uomo. La biotecnologia moderna maneggia i geni degli organismi e li inserisce in altri organismi per acquistare la caratteristica voluta, la biotecnologia tradizionale usa invece i processi degli organismi, come per esempio la fermentazione. Pertanto possiamo classificare i principali processi di Biotecnologia secondo il seguente schema: 1. Biotecnologie tradizionali 1.1. Fermentazioni 1.2. Selezione artificiale di animali e piante 2. Biotecnologie innovative 2.1. Ingegneria genetica (DNA ricombinante) 2.2. Cellule staminali 2.3. Clonazione 2.4. Terapia genica 5 2.5. OGM agricoli e animali 2.6. Bioremediation Storia Date fondamentali per la biotecnologia (tutte queste date sono importanti, quelle evidenziate rappresentano più di altre un passo cruciale): 1750 AC.- I Sumeri fermentano la birra. 500 AC.- I cinesi usano la soia come antibiotico per trattare malattie della pelle. 1590.- Janssen inventa il microscopio. 1675.- Leeuwenhoek scopre i protozoi ed i batteri. 1797.- Jenner inietta ad un bambino un vaccino virale per proteggerlo dalla vaiolo. 1830.- Vengono scoperte le proteine. 1833.- Viene scoperto il nucleo delle cellule. 1855.- Pasteur comincia a lavorare il lievito, provando per la prima volta che si tratta di organismi viventi. 1863.- Mendel, nel suo studio sui piselli, scopre che le caratteristiche sono state trasmesse dai genitori alla progenie da unità indipendenti, denominate successivamente geni. Le sue osservazioni pongono le fondamenta nel campo della genetica. 1879.- Flemming scopre le cromatine, le strutture ad asta all'interno del nucleo delle cellule che successivamente vengono chiamate "cromosomi." 1888.- Waldyer scopre il cromosoma. 1907.- E’ segnalata la prima coltura in vivo delle cellule animali. 1909.- Alcuni geni vengono collegati alle malattie ereditari. 1911.- Viene scoperto il primo virus che causa il cancro. 1919.- La parola "biotecnologia" viene usata per la prima volta da un assistente tecnico agricolo ungherese. 1920.- Evans e Long scoprono l’ormone della crescita. 1928.- Fleming scopre la penicillina, il primo antibiotico. 1953.- Watson e Crick rivelano la struttura tridimensionale del DNA (* vedere nota al fondo su R. Franklin) 1955.- Viene isolato per la prima volta un enzima addetto alla sintesi di un acido nucleico 1961.- Per la prima volta viene compreso il codice genetico. 1969.- Viene per la prima volta sintetizzato in vitro un enzima. 1972.- La composizione del DNA degli esseri umani viene scoperto essere per il 99% simile a quelle degli scimpanzé. 1973.- Cohen e Boyer effettuano il primo esperimento ricombinante del DNA, usando geni dei batteri. 1977.- Batteri geneticamente costruiti vengono utilizzati per sintetizzare la proteina umana della crescita. 1979.- Vengono prodotti i primi anticorpi monoclonali. 1982.- Humulin, l'insulina umana prodotta dalla Genentech, utilizzando batteri geneticamente modificati, è il primo farmaco biotech che viene approvato dalla FDA per il trattamento del diabete 1984.- Viene sviluppata la tecnica dell’impronta genetica del DNA. Viene sviluppato il primo vaccino geneticamente modificato. 1987.- Humatrope viene usato per curare la deficienza del fattore di crescita. 1988.- Il Congresso USA costituisce un fondo per il progetto del genoma umano allo scopo di tracciare ed ordinare il codice genetico umano. 1989.- Epogen della Amgen è approvato per il trattamento dell'anemia collegata a malattie renali. 1993.- Betaseron della Chiron è approvato come il primo trattamento per la sclerosi multipla. 1997.- Scienziati scozzesi clonano la pecora Dolly, usando il DNA di cellule di pecore adulte. La pelle umana viene prodotta in vitro. 1999.- Viene decifrato il codice genetico completo del cromosoma umano. 2001.- Viene pubblicata la sequenza del genoma umano, che permette ai ricercatori di tutto il mondo di cominciare a sviluppare nuove cure per malattie finora incurabili. 2004.- Viene approvato l’Avastin della Genentech, primo farmaco anti-angiogenesi per il trattamento del cancro al colon. 6 2007.- Vengono ottenute le prime cellule staminali embrionali senza utilizzare embrioni, risolvendo importanti questioni etiche. La Biotecnologia moderna è destinata a rivoluzionare ampi settori del mondo, analogamente a come è stato molti anni fa con lo sviluppo della chimica. La portata dei cambiamenti in arrivo spazia dalla produzione industriale alla produzione agricola, dalle problematiche ambientali, al mondo della salute. In quest’ultimo settore, i cambiamenti sono senza dubbio i più rilevanti. E’ mutato il modo di fare ricerca di nuovi farmaci e gli stessi farmaci sono diversi rispetto al passato. Con la biotecnologia, i ricercatori si avvalgono della comprensione dei meccanismi biologici che governano una determinata malattia e delle banche dati genetiche, per individuare molto più rapidamente molecole efficaci per trattare altri disturbi. Se tests e sperimentazioni hanno tempi analoghi a quelli del passato, l’individuazione di nuove molecole candidate è velocizzata, con un incremento nella produzione di nuovi e più efficaci farmaci, di cui già diversi sono sul mercato. I nuovi farmaci biotecnologici, inoltre, sono più precisi e più mirati perché basati su una maggiore conoscenza dell’organismo. Nota: Rosalind Franklin è meglio conosciuta per il suo lavoro sulle immagini di diffrazione a raggi X del DNA che ha portato alla scoperta della doppia elica del DNA. I suoi dati, secondo Francis Crick, sono stati effettivamente utilizzati per formulare l’ipotesi di Crick e Watson nel 1953 riguardante la struttura del DNA. Inoltre, i suoi progetti inediti mostravano che aveva di fatto individuato la generale B-forma dell’elica del DNA. Tuttavia, il suo lavoro è stato pubblicato terzo nella serie dei tre articoli Nature articles, preceduto dall'articolo di Watson e Crick dove il suo contributo appare come un sostegno alla loro ipotesi. Wilkins, Watson e Crick hanno ricevuto il premio Nobel insieme, alcuni anni più tardi, dopo la morte di Franklin, ma il lavoro di Franklin non ha avuto il suo adeguato riconoscimento durante la sua vita. Dopo aver terminato la sua parte di lavoro del DNA, Franklin ha condotto un lavoro pionieristico sul mosaico del tabacco e virus della polio. Morì a 37 anni per le complicazioni derivanti da cancro ovarico. La sua memoria ha ricevuto molti riconoscimenti da grandi istituzioni scientifiche. Ma, come spesso è capitato nella storia, il vero riconoscimento non è mai stato consegnato a lei personalmente Bioetica Le biotecnologie rappresentano una delle frontiere più promettenti della scienza contemporanea, in grado di fornire all'umanità nuove opportunità per combattere le malattie e la denutrizione, e per allargare gli orizzonti della nostra conoscenza dei sistemi viventi. 7 Al tempo stesso, queste tecniche implicano delle incognite e dei rischi per l'ambiente e la salute umana. Sono in particolare le biotecnologie applicate alle cellule germinali animali e vegetali a rappresentare una delle frontiere più promettenti e insieme più temute. La sperimentazione biotecnologica a livello cellulare sta diventando importante per studiare le diverse fasi della vita cellulare e l’interazione tra cellule (es. la biologia cellulare del cancro, la determinazione delle predisposizioni genetiche per le malattie comuni, le basi molecolari dell'attività dei farmaci, le strategie di modificazione genetica di animali e di piante per renderle più efficienti, ecc. ecc…). Tuttavia la loro utilizzazione sta sollevando crescenti riserve etiche a livello di opinione pubblica, in quanto si teme che possano condurre ad abusi contrari alla dignità umana o possano produrre gravi danni all'ambiente. Basti pensare ad alcuni temi molto dibattuti nella società: Clonazione; Sperimentazione clinica; Eutanasia; Manipolazione genetica; Fecondazione assistita; Accanimento terapeutico; Embrione umano; Cure palliative (cure di accompagnamento in Aborto e questioni bioetiche relative caso di morte); all'inizio della vita umana; Ingegneria genetica; Trapianti d'organi; Bioetecnologie (in senso lato, legate non Eugenetica (selezione della specie migliore); solo all’organismo umano). I temi sopraccitati evidenziano come sia necessario (e non solo importante) che la società compia un cammino di conoscenza e di approfondimento (non solo scientifico) per evitare il rischio di derive: da una parte l’uso indiscriminato di una “conoscenza” con conseguenze disastrose sotto diversi punti di vista (ambientale, ecologia umana fisica e psichica), dall’altra uno sterile e moralismo che precluderebbe l’uso della biotecnologie a fini socialmente e umanamente utili. Si cita, ad esempio, la storia di come Pasteur scopri il vaccino antirabbico. Nella sua ricerca, Pasteur voleva procedere come aveva fatto Koch per la scoperta del bacillo della tubercolosi; ma l'agente infettivo dell'idrofobia era un virus, molto più piccolo e pertanto invisibile ai microscopi dell'epoca. La metodica, quindi, doveva essere un'altra. Pasteur pensò di utilizzare lo stesso midollo infetto, lasciandolo diventare inerte; questo ciclo durava 14 giorni e produceva il materiale necessario per la terapia, iniezioni sempre più virulente inoculate per far sviluppare all'organismo stesso le difese immunitarie atte a sconfiggere la malattia. Questa terapia venne sperimentata con successo sui cani finché un giorno fu provata per la prima volta su Jospeh Meister, un bambino di 9 anni morso da un cane ammalato e a sua volta colpito da idrofobia. Dopo 12 iniezioni ed un'attesa di circa 2 settimane, nonostante l'incredulità delle persone, che rimproveravano a Pasteur l'imprudenza del suo atto, il ragazzo poté lasciare il letto completamente guarito. Fu grazie a questo successo che fu fondato un Istituto di Ricerca intitolato a Pasteur; inoltre, allo scenziato furono tributati numerosi riconoscimenti ufficiali nazionali. Tornando alle biotecnologie, attualmente la raccomandazione del Consiglio d’Europa numero 1046 del 24/09/1986 chiede ai governi di proibire: la creazione di embrioni umani in vitro per scopi di ricerca, la clonazione umana, lo scambio di geni tra uomini e animali. L’industria delle biotecnologie europea ha raccolto in un codice una summa di valori approvati a Bruxelles nel 1998. L’Italia ha istituito il Comitato Nazionale per la Bioetica (CNB) il 28 marzo 1990. Il Comitato svolge sia funzioni di consulenza presso il Governo, il Parlamento e le altre istituzioni, sia funzioni di informazione nei confronti dell’opinione pubblica sui problemi etici emergenti con il progredire delle ricerche e delle applicazioni tecnologiche nell’ambito delle scienze della vita e della cura della salute. Il Comitato esprime le proprie indicazioni attraverso pareri, mozioni e risposte che vengono pubblicati, non appena approvati, sul sito. L’azione del CNB si svolge anche in un ambito sovra nazionale con regolari incontri con i Comitati etici europei e con i Comitati etici del mondo. 8 BIOTECNOLOGIE TRADIZIONALI Riprendendo lo schema del primo paragrafo, le biotecnologie tradizionali si dividono in: Fermentazioni Selezione artificiale di animali e piante In particolare queste tecniche non prevedono l’uso di sofisticate tecnologie ovvero si basano su processi che già avvengono in modo naturale. Tuttavia l’uomo se ne serve per casi o processi specifici. Non si tratta quindi semplicemente di processi “antiquati” rispetto alle biotecnologie innovative, quanto di tecniche meno che si avvalgono di minori livelli di tecnologia. Fermentazioni La fermentazione è un processo che, in molte culture, ha fornito importanti strumenti per la trasformazione degli alimenti aumentandone i valori nutrizionali e la conservabilità. Di seguito i principali processi in cui viene sfruttata la fermentazione. Nella panificazione il lievito (del genere Saccharomyces) fermenta, gli oligosaccaridi che si staccano dall'amido durante la fase di impasto e di riposo della massa in lavorazione. I prodotti della fermentazione alcolica (alcol etilico ed anidride carbonica) passano in fase gassosa formando le caratteristiche bolle durante la lievitazione e la cottura. Il vino viene prodotto a partire da soluzioni zuccherine ottenute dallo schiacciamento del grappolo d'uva lasciate a fermentare con i lieviti unicellulari del genere Saccharomyces presenti sulla buccia dell'acino o provenienti da colture selezionate. A seconda delle condizioni di fermentazione, si differenziano le qualità organolettiche (colore, sapori, aromi...) del vino caratteristiche che si arricchiscono ulteriormente durante le fasi successive di lavorazione. Il lievito in condizioni anaerobiche trasforma 100 grammi di zucchero in 51,1 di alcool etilico con un rendimento in volume del 65.5%. Questo è un rendimento ideale, nella realtà una parte dello zucchero disponibile è utilizzata dal lievito per moltiplicarsi; inoltre durante la fermentazione i lieviti del mosto producono, oltre l'alcol e l'anidride carbonica, anche prodotti secondari (glicerina, acido acetico, acido succinico) che contribuiscono a caratterizzare l'aroma del prodotto finito. Il rendimento reale quindi si approssima al 60% in volume. La birra si ottiene per l'azione di lieviti delle specie Saccharomyces cerevisiae o Saccharomyces pastorianus su di un mosto contenente malto di orzo, ed eventualmente anche quantità variabili di malti di altri cereali (grano, riso o mais). La lavorazione è tale da conservare nel prodotto anche l'anidride carbonica. 9 Sottoprodotti dei birrifici sono il "lievito di birra" venduto disidratato o compresso in panetti (per la panificazione) e l'anidride carbonica. Nella maturazione di alcuni formaggi (riconoscibili dalle "occhiature") gli zuccheri residui vengono degradati con produzione di anidride carbonica. Altri formaggi maturano utilizzando vie metaboliche diverse dalla fermentazione. Lo yogurt è il risultato della fermentazione lattica operata da Lactobacillus bulgaricus e lo Streptococcus thermophilus, sono responsabili del processo di scissione del lattosio in galattosio e glucosio. Questi "fermenti" agiscono con un meccanismo protosimbiotico: lo streptococco lavora per primo, creando le condizioni affinché il lattobacillo compia l'opera della scissione del lattosio Selezione artificiale di animali e piante La selezione artificiale è un metodo esercitato già da tempi molto remoti (operato dagli esseri umani e quindi in contrapposizione alla selezione naturale) con il quale si ottengono nuovi individui basandosi sul fenotipo, cioè sulle caratteristiche visibili esteriormente. Effettivamente, la selezione artificiale agisce nello stesso modo in cui opera la selezione naturale. La selezione artificiale è stata utilizzata per creare delle nuove razze (soprattutto in agricoltura e allevamento) che avessero delle caratteristiche ritenute migliori rispetto a quelle di partenza. L'uomo è capace di operare cambiamenti negli esseri viventi che lo circondano. Gli è possibile scegliere tori e mucche che producono più carne; li usa come riproduttori, e poiché questa caratteristica (la produzione di carne) è ereditabile, i discendenti la presentano più accentuata. Si tornano a selezionare di nuovo gli individui più favorevoli per il carattere, e si utilizzano come riproduttori per la generazione seguente. Col tempo si cambiano gli organismi nella direzione desiderata, incrementando la caratteristica scelta dall'uomo. Le diverse razze di cani, gatti o piccioni sono state ottenute con il suddetto processo. Lo stesso vale per cultivar di fiori, piante, ortaggi, frutta: al fine di ottenere specie più belle, eleganti, profumate, durature, conservabili, saporite, nutrienti. L'uomo è andato selezionando quelle caratteristiche che ha considerato interessanti. In natura, la selezione agisce in quelle varianti che conferiscono un migliore adattamento agli organismi, e che pertanto permetteranno di produrre una migliore discendenza. Nella selezione artificiale, le caratteristiche scelte dall'uomo sono a suo proprio beneficio. Molto probabilmente, questi organismi selezionati artificialmente verrebbero selezionati in maniera inversa in natura. Ad esempio, alcune razze di cane selezionate per servire come animali da compagnia, sarebbero poco adatte a vivere in un ambiente naturale. 10 11 Anche per la razza umana è stata tentata una strada di selezione artificiale. In particolare ci si riferisce all’oscuro periodo storico del nazismo, con le teorie della supremazia della “razza ariana” e comunque a tutte quelle correnti di pensiero che ancora oggi, sostengono la superiorità di una razza rispetto a un’altra. Al di là di queste ideologie oggettivamente errate (se non aberranti) da un punto di vista umano, non bisogna tuttavia dimenticare che i fenotipi umani (le diverse razze) hanno diverse caratteristiche fisiche (es. per una questione strutturale, il fenotipo umano africano, con un colore della pelle scuro, presenta una maggiore densità corporea tale che, ad esempio, non possa eccellere negli sport acquatici. Nel basket viceversa altri fattori giocano a favore della razza africana quali maggior equilibrio, maggiore velocità, vista migliore rispetto agli altri, “scaltrezza”). 12 BIOTECNOLOGIE INNOVATIVE Riprendendo lo schema del primo paragrafo, le biotecnologie innovative si dividono in: 1. DNA ricombinante 2. Clonazione 3. Cellule staminali 4. Terapia genica 5. OGM agricoli e animali 6. Bioremediation DNA ricombinante Il grande “salto” in avanti delle biotecnologie si realizzò solo dopo che Watson e Crick (1953) elaborarono il loro modello della struttura del DNA, identificando in questa molecola la sede delle informazioni genetiche per la produzione di qualunque proteina. La scoperta dei meccanismi che regolano la sintesi proteica ha consentito, dagli anni ’70, lo sviluppo di una tecnologia in grado di far produrre da un organismo microscopico (riproducibile in gran quantità e a un costo relativamente limitato) una proteina di un altro organismo, impossibile da ottenere in altro modo o, comunque, ottenibile (per estrazione o per sintesi industriale) in quantità limitate o solo a costi molto elevati. Questa tecnologia, detta tecnologia del DNA ricombinante o ingegneria genetica, impiega il DNA ricombinante, ossia una molecola di DNA ibrida, ottenuta inserendo il gene della proteina desiderata in una molecola di DNA vettore che si introduce e si replica nelle cellule dell’organismo da cui si vuol far produrre la proteina (cellule ospiti). In pratica, da una cellula di un organismo “donatore” si estrae il gene richiesto (o, meglio, frammenti del DNA tra i quali è compreso anche quello richiesto), lo si lega a un vettore (una molecola particolare di DNA capace di penetrare in una cellula ospite) formando così un DNA ibrido, detto DNA ricombinante, che si inserisce in una cellula “ospite”, appartenente a un altro organismo. La cellula ospite, ricevuto il DNA ricombinante, acquisisce la capacità di produrre la proteina codificata da quel gene, cioè si trasforma, diventa una cellula ricombinante. La trasformazione comporta per la cellula l’acquisizione di una nuova proprietà: la capacità di produrre quella proteina. Essendo stabilmente integrato nel DNA della cellula ospite, il gene si riproduce insieme alla cellula, per cui le cellule figlie manterranno tutte la capacità di produrre la nuova proteina. Stimolando la riproduzione delle cellule ospiti (clonazione), in poco tempo si otterrà una popolazione di milioni di cellule, tutte in grado di produrre la proteina desiderata. Le cellule ospiti più frequentemente utilizzate sono batteri e microrganismi unicellulari eucarioti ma possono essere impiegate cellule provenienti da piante o animali. Ognuna di queste cellule può ricevere nuovo DNA mediante un idoneo vettore, specifico per ogni tipo di cellula. I vettori possono essere: batteriofagi (virus che infettano i batteri) per i batteri; plasmidi (piccole molecole di DNA circolare) per i batteri e altri organismi unicellulari; virus vegetali e virus animali rispettivamente per cellule di piante e di animali. Tecnica del DNA ricombinante La tecnica del DNA ricombinante richiede alcuni passaggi; qui di seguito viene esposto, in modo semplificato, l’esempio che porta alla produzione di insulina umana (utilizzata per i malati di diabete). Vediamo come si ottiene la produzione di questo ormone con questa tecnica. 1) La prima tappa consiste nell’isolamento del gene che codifica per l’insulina, ormone prodotto dalle cellule beta del pancreas: si estrae il DNA di queste cellule e lo si “taglia” in vari pezzi utilizzando dei particolari enzimi, detti enzimi di restrizione, che tagliano il DNA in corrispondenza di specifiche sequenze di 13 nucleotidi. Si ottengono vari frammenti di DNA, uno dei quali corrisponde al gene dell’insulina (esistono oggi tecniche più rapide che consentono di ottenere il gene dell’insulina partendo dall’RNA messaggero). 2) Viene tagliato, sempre con gli enzimi di restrizione, anche il DNA del vettore, che, in questo caso, è un plasmide. I plasmidi sono piccoli filamenti circolari di DNA superavvolto a doppia elica, presenti nel citoplasma e distinguibili dal cromosoma batterico per le loro dimensioni ridotte. Il materiale genetico che li contraddistingue permette all'organismo ospite di svolgere varie funzioni non essenziali, ma conferiscono alla cellula proprietà speciali (a volte proprietà metaboliche uniche). I plasmidi sono capaci di spostarsi tra le cellule (anche non uguali, ma filogeneticamente affini) influendo sulla variabilità genetica. Vi sono anche plasmidi detti Episomi, cioè plasmidi che entrano a far parte del DNA del batterio. 3) Il DNA della cellula (in frammenti) e il plasmide, dopo essere stati tagliati, vengono uniti. 4) Il frammento di DNA e il plasmide vengono legati per mezzo di un enzima specifico, la DNA-ligasi. 5) Si ottengono così delle molecole di DNA ricombinante, costituite da pezzi del plasmide e da pezzi del DNA umano legati insieme. Alcune di queste molecole “ibride” di DNA ricombinante contengono, attaccato al plasmide, il gene dell’insulina, altre invece no. 6) Questi nuovi plasmidi ricombinanti vengono messi a contatto con le cellule di un particolare batterio, l’Escherichia coli, dal quale vengono assorbiti. 7) Si cerca quindi di individuare gli Escherichia coli ricombinanti che hanno assorbito il plasmide ricombinante contenente il gene per l’insulina, li si isola, li si coltiva in modo da ottenere un numero elevato di cellule produttrici di insulina umana. 8) I plasmidi si replicano autonomamente all’interno del batterio (quindi aumentano di numero, portandosi naturalmente dietro anche il gene aggiunto). 9) Il processo, per ottenere il numero di proteine richieste (in questo caso l’ormone dell’insulina umana) richiede un numero elevato di plasmidi. Servono quindi più vettori (batteri di Escherichia coli). La duplicazione del batterio comporta che le due cellule figlie portino con se i plasmidi della cellula madre (trasferimento verticale, cioè da madre a figli). Tuttavia esistono anche altri processi per la diffusione dei plasmidi con il gene acquisito (trasferimento orizzontale): Trasformazione: il DNA viene catturato dall’esterno (per esempio un frammento da un batterio morto. Trasduzione: é il processo dal quale il DNA di un batterio passa ad un altro attraverso un virus batterico (un batteriofago). Coniugazione: un processo dal quale una cellula batterica vivente trasferisce materiale genetico attraverso il contatto con altra cellula mediante un pilo coniugativo (vedere figura a lato). Trasferimento orizzontale e coniugazione sono quindi i processi con cui si sintetizza insulina umana. 14 10) L’ultimo passaggio è l’estrazione della proteina prodotta con la sintesi proteica effettuata leggendo la sequenza del DNA del plasmide che codifica per la proteina stessa (in questo caso l’insulina). Cellule staminali Una cellula staminale è un tipo di cellula non ancora differenziata che, per questa ragione, può dividersi e formare altri tipi cellulari. Le cellule staminali sono presenti negli organismi eucarioti pluricellulari e, vista la natura stessa, non possono essere individuate nei procarioti o negli eucarioti monocellulari. La presenza di poche linee di cellule staminali permette la sintesi di numerose altre cellule; un organismo, infatti, possiede diversi tipi cellulari che originano da poche linee staminali per differenziamento. A titolo di esempio, in un qualsiasi organo possono coesistere diverse decine di cellule differenti sia per morfologia sia per funzionalità che originano da una, o comunque poche, cellule staminali. 15 Lo studio, e la comprensione, dei meccanismi che portano al differenziamento delle cellule staminali è ancora poco chiaro, ma le prospettive, e l'impegno nella ricerca, sembrano offrire buone possibilità per gli sviluppo in questo settore. La comprensione del funzionamento delle cellule staminali può aprire la strada per lo studio e la cura di alcune patologie tra cui, ad esempio, i tumori. Differenze tra cellula staminale e cellula differenziata Le differenze tra le cellule della linea staminale e le cellule già differenziate sono molte e possono essere classificate su due piani: morfologico e funzionale. Una cellula staminale possiede una morfologia molto più semplice rispetto ad una cellula differenziata che si apprezza, ad esempio, nell'assenza di strutture particolari o nell'aliquota di organuli in essa presenti. Anche dal punto di vista funzionale, una cellula staminale è solitamente limitata rispetto ad una strutturalmente formata e differenziata. Cellula staminale a confronto con una cellula parietale della mucosa gastrica dello stomaco. Nell'immagine sopra proposta, volutamente semplificata, si mettono a confronto una cellula parietale (che sintetizza acido cloridrico) a livello della mucosa gastrica, e la cellula staminale dalla quale essa ha origine. Appare subito evidente che, nella cellula staminale, l'espressione degli organuli è minima, nella cellula parietale, invece, i mitocondri e l'apparato del Golgi risultano essere molto sviluppati. Classificazione delle cellule staminali Le cellule staminali possono essere classificate in base all'origine ed alla loro capacità di dividersi in uno o più gruppi cellulari o citotipi. Classificazione in base all'origine Le cellule staminali sono presenti tanto nell'embrione quanto nell'individuo adulto. La classificazione, in tal senso, tiene conto della provenienza: Cellule staminali embrionali, sono presenti nelle prime fasi di divisione dell'embrione dopo la fecondazione solitamente quando il gruppo di cellule embrionali è ancora allo stadio di morula; Cellule staminali embrionali tardive, o cellule staminali germinali, che sono presenti in alcune strutture del feto; Cellule staminali adulte, presenti nell'individuo dopo la nascita. Le staminali embrionali, specialmente quelle prelevate nei primi stadi di divisone, rappresentano delle cellule abbastanza importanti poiché da esse possono originarsi tutti i citotipi presenti nei tessuti adulti. Anche nell'adulto sono presenti alcune linee cellulari di natura staminale; nello strato base dell'epidermide, ad esempio, si trovano delle cellule staminali che si differenziano in tessuto epiteliale. Anche il midollo osseo è ricco di cellule staminali di differente tipo che, ad esempio, serviranno per l'emopoiesi. Classificazione in base alla capacità di differenziamento 16 Una cellula staminale può differenziarsi in uno o più tipi cellulari, secondo un concetto noto con il termine di plasticitià; in base alla capacità di formare differenti citotipi è possibile classificare le cellule staminali in: Cellule staminali unipotenti, capaci di differenziarsi in un solo tipo cellulare, ad esempio le cellule dello strato basale dell'epidermide. Cellule staminali multipotenti, che possono dare origine ad alcuni tipi di tessuto, ma non a tutti; un esempio è dato dalle cellule staminali ematopoietiche del midollo osseo. Cellule staminali pluripotenti, sebbene possano differenziarsi in qualsiasi tipo cellulare non sono "biologicamente" capaci di formare un organismo. La ragione di questa considerazione è da ricercare nelle prime fasi dello sviluppo, dove - solitamente tra il quinto e il sesto giorno di sviluppo dell'embrione si formano due distinti tipi di cellule pluripotenti: il primo è più interno e forma l'embrione vero e proprio e il secondo, localizzato all'esterno, formerà gli annessi embrionali come il cordone ombelicale e la placenta. Cellule staminali totipotenti, sono in grado di formare qualsiasi tessuto e, a differenza delle pluripotenti, possono differenziarsi in cellule formanti l'embrione a anche in cellule formanti gli annessi. Malattie curate con le cellule staminali Il sangue placentare (contenuto nel cordone ombelicale) donato viene conservato per curare gravi patologie del sangue quali malattie tumorali come la leucemia (insieme di malattie maligne, vari tipi di cancri o tumori caratterizzati dalla proliferazione neoplastica di una cellula staminale ematopoietica e si traduce in un numero elevato di globuli bianchi anormali) e i linfomi (tipo di tumore del tessuto linfoide) e patologie non tumorali come: la talassemia (malattia ereditaria che comporta anemia, cioè una diminuzione della presenza di emoglobina utile al trasporto dell'ossigeno nel sangue), l’aplasia midollare (è una forma di anemia caratterizzata dall'insufficiente produzione nel midollo osseo di cellule del sangue di tutti i tipi) e le immunodeficienze congenite in pazienti bambini e adulti. Clonazione Mentre il clonaggio genico consiste nella produzione di numerose copie identiche di un determinato gene, la clonazione comprende una serie di procedure che hanno lo scopo di creare, a partire da un determinato individuo (animale o vegetale), organismi geneticamente identici a lui. Si tratta di una sorta di riproduzione senza l’intervento dei gameti (cellule sessuali maschili e femminili). In sostanza viene prelevato il nucleo da una cellula somatica dell’individuo che si vuole clonare e viene fuso con un ovocita privato del proprio nucleo. Poiché il nucleo diploide della cellula somatica porta nel suo DNA tutto il 17 patrimonio genetico, il nuovo individuo risulta, se non intervengono mutazioni, geneticamente identico al donatore del nucleo: in definitiva è un suo clone. Per molti anni le piante sono state prodotte con la clonazione, prelevando un piccola parte da una piante (solitamente un ramo con alcune gemme) e riproducendo da essa un nuova pianta; la clonazione è stata utilizzata per un certo periodo anche per produrre frutta e verdura su scala commerciale. Utilizzando tecnologie biologiche più sofisticate si è cercato di clonare animali. Nel 1996 un istituto di biotecnologie di Edimburgo riuscì a far nascere la pecora Dolly a partire da una cellula adulta differenziata di un’altra pecora. Dolly è stata un evento particolare non tanto per essere un clone, visto che i tentativi di clonazione di animali si svolgevano da anni, ma perché la fonte genetica utilizzata per produrla era, per la prima volta, una cellula adulta e non una cellula embrionale (quindi una cellula somatica e non una cellula staminale). Lo scalpore suscitato dalla nascita della pecora Dolly fu dovuto alla scoperta che cellule differenziate prelevate da organismi superiori adulti possono riacquistare le caratteristiche di totipotenza, tipiche delle cellule embrionali, necessarie a ricreare un individuo completo. Tecnica di clonazione La tecnica utilizzata oggi per clonare gli animali, chiamata “somatic cell nuclear transfer” (trasferimento del nucleo delle cellule somatiche), è la stessa usata per clonare Dolly. 1. Viene stimolato con un trattamento ormonale un animale e si preleva un ovocita (cellula uovo femminile), a cui viene tolto il nucleo. 2. Dall’animale donatore viene invece prelevata una cellula somatica (nel caso di Dolly una cellula della ghiandola mammaria di una pecora) 3. Viene messa in contatto la cellula somatica con l’ovocita (quindi vengono messe a contatto le due cellule, quella somatica e quella sessuale) 4. Si depolarizza la membrana dell’ovocita e questo si fonde con il nucleo della cellula somatica. 5. La cellula che si ottiene viene infine impiantata nell’utero di una madre surrogata. 18 Delle 277 fusioni cellulari, 29 embrioni si sono sviluppati e sono stati impiantati nelle 13 madri surrogate. Ma solo una gravidanza fu portata a termine, e dopo 148 giorni nacque l'agnello Finn Dorset 6LLS (alias Dolly), pesava 6,600 kg. È nata il 5 luglio del 1996 e quando aveva sei anni e mezzo, il 14 febbraio del 2003, è morta con l'eutanasia. Le pecore possono vivere fino a 11 o 12 anni, ma Dolly soffriva di artrite all'articolazione dell'arto posteriore e di adenomatosi polmonare. ll suo precoce invecchiamento potrebbe essere un'indicazione del fatto che essa è stata riprodotta dal nucleo di una pecora di 6 anni. dal 2000 in poi, la lista delle specie clonate si è allungata e oggi comprende macachi, topi, mucche, gatti, cavalli e cammelli. Vi è stato un esperimento di clonazione umana nel 2001 (Stati Uniti), presso l’istituto di Worcester (nel Massachussetts). Lo sviluppo dell’embrione si è però fermato precocemente, quando ancora era solo un agglomerato cellulare indifferenziato. Oggi è possibile riprodurre in vitro organismi geneticamente identici partendo da cellule embrionali e scindendole nei primi stadi di sviluppo. Cioè si lascia che la cellula fecondata inizi a sviluppare in un ambiente artificiale (“in vitro” appunto) e poco dopo si dividono i due gruppi di cellule ottenendo 2 organismi distinti. Attualmente, in Inghilterra e negli USA, è possibile la clonazione di embrioni umani a scopo di ricerca scientifica. In Italia è vietato. La ricerca scientifica è infatti orientata verso lo studio di tecniche di clonazione per produrre organi che possano sostituire quelli danneggiati. Partendo da cellule del paziente stesso. Terapia genica Per terapia genica (in inglese Gene Therapy) si intende l'inserzione di materiale genetico (DNA) all'interno delle cellule al fine di poter curare delle patologie. Questa procedura di inserzione è nota come trasfezione. Per essere più esatti la terapia genica consiste nel trasferimento di uno o più geni sani in una cellula malata, al fine di curare una patologia causata dall'assenza o dal difetto di uno o più geni (mutati). Dunque, è necessario in primo luogo identificare il singolo gene o i diversi geni responsabili della malattia genetica. Sebbene le terapie siano generalmente sperimentali, si può tentare in secondo luogo - almeno per alcune malattie - la sostituzione dei geni malati sfruttando, ad esempio, come vettore un virus reso inattivo, svuotato preventivamente del suo corredo genetico. Con un meccanismo piuttosto complesso, che richiede l'uso di 'forbici' molecolari enzimatiche, enzimi di restrizione (con cui si preleva il gene "sano") si può poi 'correggere' il DNA, rimpiazzando le sequenze difettose, in modo tale che la cellula sintetizzi correttamente le proteine necessarie al corretto funzionamento metabolico. La terapia genica fu concepita a seguito del grande progresso delle metodiche di biologia molecolare sviluppatesi dagli anni '80. Tali tecniche consentirono il clonaggio ed il sequenziamento di vari geni. Ciò comportò la precisa identificazione di molte alterazioni geniche in diverse patologie e la capacità, grazie alle tecniche del DNA ricombinante, di modificare microorganismi (come batteri o funghi) per poter far loro esprimere delle molecole d'interesse. Il passo successivo consistette nella valutazione della possibilità di trasfettare le cellule somatiche di un individuo avente una malattia genetica con un segmento di DNA contenente l'allele sano. Questo approccio si è successivamente esteso anche alle patologie non mendeliane come tumori, infezione da HIV ed altre patologie in cui non si va a sostituire un gene difettoso ma se ne aggiunge uno che possa mettere in moto un fenomeno terapeuticamente utile. Tipologie di terapia genica Esistono due tipologie di terapia genica: quella delle cellule germinali e quella delle cellule somatiche. La prima si propone di trasfettare le cellule della linea germinale come spermatozoi ed ovociti o le cellule staminali totipotenti dei primissimi stadi dello sviluppo dell'embrione (alla fase di 4-8 cellule), ma attualmente essa non viene messa in pratica sia per ragioni tecniche e, soprattutto, per i grandissimi dilemmi etici che solleva. 19 La seconda tipologia, invece, si propone di modificare solamente le cellule somatiche, senza intaccare, quindi, la linea germinale; oggigiorno è la via più studiata e tentata. La terapia genica delle cellule somatiche, a sua volta, viene suddivisa in due gruppi: la terapia genica ex vivo e quella in vivo. La terapia genica ex vivo È la tipologia che venne messa in pratica per prima e consiste nel prelievo delle cellule somatiche della persona interessata. Esse, successivamente, vengono messe in coltura in laboratorio. Durante questo tempo vengono anche trasfettate con il gene d'interesse, inserito tramite un apposito vettore (spesso vengono usati vettori virali), e successivamente vengono reinfuse o reimpiantate nel corpo del soggetto. Tale procedura è sicuramente la più lunga e la più costosa delle due ma permette di selezionare ed amplificare le cellule d'interesse ed inoltre gode d'una maggior efficienza. È attualmente la modalità più utilizzata ma è riservata solamente a quei casi in cui sia possibile prelevare, mettere le cellule in cultura e reinserirle nell'organismo. La terapia genica in vivo Viene attuata in tutti quei casi in cui le cellule non possono essere messe in coltura, o prelevate e reimpiantate, come quelle del cervello o del cuore e della maggior parte degli organi interni; inoltre, rappresenta un modello terapeutico con elevata compliance e molto economico ma, attualmente, di più difficile applicazione. In questo caso il gene, o oligonucleotide (pochi nucleotidi) d'interesse viene inserito nell'organismo, tramite un opportuno vettore, direttamente per via locale o sistemica (cioè in modo che si diffonda in tutto l’organismo). I sistemi attualmente studiati sono di tre tipi: lipoplessi, poliplessi, lipopoliplessi. Sono sistemi non virali. Potenzialmente tutti i tre tipi di vettori non virali potrebbero sostituire gli attuali vettori virali e fisici. Stato attuale e prospettive Sebbene l’obiettivo di partenza fosse quello di curare le malattie ereditarie monogeniche (che coinvolgono quindi solo un gene), di fatto la modificazione di cellule si è rivelata applicabile anche alla cura di malattie genetiche non ereditarie come i tumori, malattie non monogeniche come il diabete o la sclerosi multipla, o di una malattia virale come l’AIDS. Nonostante gli sforzi degli scienziati in tutto il mondo, la terapia genica ha visto finora un successo limitato. La ragione di ciò risiede nel fatto che la terapia genica pone una delle più grandi sfide tecnologiche nella medicina moderna. Infatti introdurre nuovi geni nelle cellule del corpo si è rivelata un’operazione molto più complessa di quanto si pensasse in linea teorica. 20 OGM agricoli e animali OGM: “organismo il cui materiale genetico è stato modificato in modo diverso da quanto avviene in natura con l'accoppiamento e/o la ricombinazione genetica naturale" (Art. 2, Direttiva 2001/18/CE del 12/03/01). Con il termine Organismo Geneticamente Modificato (OGM) si intendono soltanto gli organismi in cui parte del genoma sia stato modificato tramite le moderne tecniche di ingegneria genetica. Non sono considerati "organismi geneticamente modificati" tutti quegli organismi il cui patrimonio genetico viene modificato a seguito di processi spontanei (modificazioni e trasferimenti di materiale genetico avvengono infatti in natura in molteplici occasioni e tali processi sono all'origine della diversità della vita sulla terra), o indotti dall'uomo tramite altre tecniche che non sono incluse nella definizione data dalla normativa di riferimento (ad esempio con radiazioni ionizzanti o mutageni chimici). Gli OGM vengono spesso indicati come organismi transgenici: i due termini non sono sinonimi in quanto il termine transgenesi si riferisce all'inserimento, nel genoma di un dato organismo, di geni provenienti da un organismo di specie diversa. Sono invece definiti OGM anche quegli organismi che risultano da modificazioni che non prevedono l'inserimento di alcun gene (es. sono OGM anche gli organismi dal cui genoma sono stati tolti dei geni), così come gli organismi in cui il materiale genetico inserito proviene da un organismo "donatore" della stessa specie. In questo secondo caso alcuni studiosi parlano di organismi cisgenici, la tecnica in questione si chiama "miglioramento genetico assistito da marcatori molecolari e la cisgenesi"(MGAMMC), per velocizzare il lento progresso del breeding ed è pronta ad introdurre piante cisgeniche nel mercato. Tecniche principali Ai fini della definizione di OGM data dalla Direttiva 2001/18/CE, sono considerate tecniche che hanno come risultato un organismo geneticamente modificato: tecniche di ricombinazione del materiale genetico che comportano la formazione di nuove combinazioni mediante l'utilizzo di un vettore di molecole di DNA, RNA o loro derivati, nonché il loro inserimento in un organismo ospite nel quale non compaiono per natura, ma nel quale possono replicarsi in maniera continua; tecniche che comportano l'introduzione diretta in un organismo di materiale ereditabile preparato al suo esterno, tra cui la macroiniezione e il microincapsulamento; fusione cellulare (inclusa la fusione di protoplasti) o tecniche di ibridazione per la costruzione di cellule vive, che presentano nuove combinazioni di materiale genetico ereditabile, mediante la fusione di due o più cellule, utilizzando metodi non naturali. Sono esclusi dalla definizione gli organismi ottenuti per mutagenesi o fusione cellulare di cellule vegetali di organismi che possono scambiare materiale genetico anche con metodi di riproduzione tradizionali, a condizione che non comportino l'impiego di molecole di acido nucleico ricombinante. Tecniche di miglioramento genetico I metodi utilizzati tradizionalmente per modificare il patrimonio genetico degli esseri viventi sono essenzialmente due: la mutagenesi e l'incrocio. La mutagenesi è un fenomeno che è strutturalmente presente, anche se a bassa frequenza, in tutti gli esseri viventi ed è basato sulle imprecisioni o gli errori di replicazione del genoma durante i processi di divisione cellulare. Le mutazioni vengono poi sottoposte a selezione o dall'ambiente o dall'uomo e se vantaggiose vengono mantenute nella popolazione. Nei programmi di miglioramento genetico, la frequenza con cui avvengono queste mutazioni viene generalmente amplificata utilizzando radiazioni o agenti chimici mutageni. Le mutazioni, che possono interessare una singola base del DNA o anche intere porzioni di hanno portato nel tempo ad evidenti modifiche fenotipiche negli esseri viventi (si pensi alla diversità tra le varie razze canine). L'uomo, nei secoli, ha 21 sfruttato la variabilità prodotta dalle mutazioni (quale ad esempio l'incapacità di perdere i semi da parte della spiga del frumento) per selezionare e costruire molte cultivar e razze animali oggi fondamentali per la sua sopravvivenza. L'incrocio è invece una tecnica che permette di unire le caratteristiche presenti in due individui diversi, anche non appartenenti alla medesima specie, grazie al rimescolamento dei loro genomi sfruttando la riproduzione sessuale. In tal modo sono stati prodotti il mulo o il bardotto, ma anche gli ibridi oggi utilizzati per le produzioni animali e vegetali. Il vantaggio di tale tecnica è la possibilità, una volta identificata fenotipicamente una caratteristica di interesse in una razza o in una varietà (ad esempio la resistenza ad una malattia), di trasferirla in un'altra attraverso incroci mirati. La differenza sostanziale tra queste due tecniche di miglioramento genetico e l'ingegneria genetica (alla base dello sviluppo degli OGM) sta nella modalità con cui l'uomo induce le modificazioni genetiche. Nel caso della mutazione o dell'incrocio viene infatti effettuata una selezione fenotipica, in base a caratteristiche visibili, all'interno di popolazioni molto grandi (alcune decine di migliaia nelle piante e alcune centinaia negli animali)[5]. Nell'ingegneria genetica invece è possibile "progettare" deterministicamente la modifica genetica da effettuare. Inoltre, una volta ottenuto un certo numero di organismi geneticamente modificati, essendo questi geneticamente distinguibili dagli altri, possono venire selezionati genotipicamente, ovvero in base alle loro caratteristiche genetiche, e non più unicamente fenotipicamente come accade invece per le tecniche tradizionali, per le quali non è possibile conoscere a priori le modificazioni genetiche indotte OGM nel mondo Nel mondo intero, nel 2008, sono stati coltivati oltre 125 milioni di ettari di piante geneticamente modificate[39], oltre la metà delle quali si trovano negli Stati Uniti (51%) mentre ben l'87% di esse è nel continente americano. Il 99% delle coltivazioni, è concentrata in pochi paesi: Stati Uniti, Canada, Sud America (Argentina, Brasile e Paraguay), India, Cina, e Sud Africa. In alcune nazioni europee come Francia, Spagna, Portogallo, Polonia, Germania, Slovacchia, Repubblica Ceca e Romania è permesso coltivare piante transgeniche, mentre in altre (Austria e Grecia) è vietato. Ancora diversa è la situazione in Italia, Regno Unito, Danimarca, Svezia, Finlandia, Ungheria e Slovenia, dove la legge proibisce la coltivazione di piante OGM ma non la loro importazione. Quadro normativo In molti Paesi del mondo esiste un quadro di riferimento normativo che regola il settore OGM, per garantire la biosicurezza, ossia un utilizzo in rispetto dei necessari livelli di sicurezza ambientale, della salute umana e di quella animale. I principi legislativi di riferimento a livello internazionale in tema di biosicurezza sono contenuti all'interno del Protocollo di Cartagena. In Europa il contesto normativo sugli OGM, basato sul principio di precauzione, è oggi costituito dai seguenti testi: Direttiva 2001/18/CE, che, sostituendo la 90/220/CEE, riscrive le regole base per l'autorizzazione al rilascio nell'ambiente di un nuovo OGM; Regolamenti 1829 e 1830/2003/CE, che regolano l'autorizzazione e l'etichettatura/tracciabilità degli alimenti e dei mangimi (food & feed) costituiti o derivati da OGM; Raccomandazione 556/2003, che indica le linee guida sulla coesistenza tra colture OGM e convenzionali, cui le norme nazionali e regionali dovrebbero allinearsi. L'Italia ha recepito la direttiva 2001/18/CE attraverso il decreto legislativo 224/2003. Nel luglio 2013 è stata annunciata la firma di un decreto che proibisce uno dei più diffusi O.G.M.: il mais Monsanto 810. Il decreto, prima della nuova direttiva Ue sugli Ogm che rimanda agli Stati membri il diritto di limitare o vietare le coltivazioni di Ogm, aveva prorogato per 18 mesi il divieto del 12 luglio 2013. 22 Il 6 Febbraio 2015, il Consiglio di Stato ha respinto il ricorso di un agricoltore friulano che chiedeva il permesso di utilizzare questo tipo di sementi. La sentenza ribadisce che in Italia resta un Paese OGM-free in cui è vietato l'impiego di qualsiasi tipo di OGM Bioremediation La BIOREMEDIATION – o biorisanamento – è un insieme di tecnologie che utilizzano microorganismi naturali o ricombinanti per abbattere sostanze tossiche e pericolose attraverso processi aerobici (in presenza di ossigeno) e anaerobici (in assenza di ossigeno). Tali processi possono essere applicati in situ (nel luogo da risanare); sfruttando i microorganismi residenti o attraverso l’introduzione di ceppi batterici o fungini. Oppure ex situ (non nel luogo da risanare, cioè in bioreattori, sistemi ingegnerizzati in cui l’abbattimento può essere catalizzato da enzimi) e possono essere mediati da batteri (consorzi o ceppi microbici puri), da piante (fitorisanamento) o anche per attenuazione naturale (natural attenuation). Il biorisanamento comporta la degradazione di composti tossici attraverso la loro conversione in sostanze innocue, ovvero anidride carbonica e acqua. I microorganismi, infatti, sono ubiquitari e hanno sistemi metabolici in grado di degradare e utilizzare vari composti tossici come sorgente di energia grazie al metabolismo aerobico, anaerobico, alla fermentazione e al cometabolismo. Solitamente la biodegradazione aerobica ha un’efficienza maggiore dei processi anaerobici. I processi aerobi ed anaerobici possono, inoltre, essere utilizzati in serie (sostanzialmente agiscono come in una “staffetta”), per ridurre la complessità o la tossicità del contaminante. L’efficienza di biodegradazione può essere ulteriormente aumentata attraverso l’utilizzo di microorganismi adattati o acclimatati al contaminante o di microorganismi geneticamente modificati. Tale metodo è noto come bioaugmentation. Col termine biorisanamento si indicano varie tecniche: bioventing, biosparging, biostimulation, bioaugmentation, bioleaching, biorisanamento mediato da funghi e biosorption. Rimozione Dei Metalli Fanno parte di questa tecnica alcuni processi (Bioleaching, Biosorption, Phytoremediation) che utilizzano microorganismi o vegetali. I primi demoliscono le sostanze tossiche assorbendo gli ioni metallici oppure mandandole in soluzione come minerali metallici. Si ricorda che alcuni ioni metallici sono già in soluzione nelle acque minerali, tuttavia vi sono altri metalli che sono tossici per l’uomo se ingeriti. In questo caso sarà necessario un altro processo di depurazione o di bioremediation. I vegetali invece assorbono attraverso il proprio apparato radicale i metalli immobilizzandoli nei propri organi (radici, fusto, foglie, ecc. ecc…). La fitodepurazione in situ è una tecnica molto utilizzata sia in Europa che negli Stati Uniti, pur con il limite dovuto al fatto che la contaminazione del suolo non può superare la profondità di crescita delle radici delle piante utilizzate Rimozione di altri composti inorganici La bioremediation di composti inorganici comprende numerose applicazioni (la bioassimilazione, la biodegradazione aerobica e anaerobica, il bioadsorbimento, la biomagnificazione, il bioaccumulo, la biotrasformazione e la biovolatilizzazione). Tra i composti inorganici per i quali la bioremediation ha giocato e gioca un ruolo assai importante ci sono i composti radioattivi. In particolare il batterio del genere Deinococcus è studiato e applicato per la sua capacità di resistere in ambienti estremi per la presenza di radiazioni ionizzanti e elevate temperature. Rimozione di composti organici La bioremediation è in grado di convertire in forme meno tossiche e di degradare moltissimi contaminanti organici, come ad esempio pesticidi, organocloruri, bifenili policlorurati (PCB) idrocarburi policiclici aromatici, coloranti sintetici, conservanti del legno, rifiuti da esplosivi e polimeri sintetici. 23 Tutti questi inquinanti sono per natura estremamente resistenti alla biodegradazione da parte della flora e della fauna selvatiche. La bioremediation di questi composti può essere mediata da batteri, funghi, un cocktail di diversi microorganismi, piante o da una combinazione di tutte queste tipologie. Le specie fungine hanno il vantaggio, rispetto alla maggior parte dei batteri, di mantenere un’elevata efficienza di degradazione anche in suoli aridi o semiaridi Casi di studio Biodegradazione degli idrocarburi: isolato nella laguna di Venezia nel 1996, dal lavoro di un gruppo di ricerca che coinvolge l’Università di Firenze, e l'Istituto di tecnologie biomediche del Consiglio nazionale delle ricerche (Itb-Cnr) di Milano (i risultati dello studio sono stati pubblicati su Research in Microbiology). L‘Acinetobacter venetianus VE-C3’ è un batterio marino che vive nelle acque inquinate e ha sviluppato la capacità di metabolizzare composti come gli idrocarburi (anche il petrolio) rendendoli meno dannosi per l'ambiente; tale processo, quando sfruttato dall'uomo viene chiamato ‘biorisanamento’. Biodegradazione del petrolio: lo studio, al quale ha preso parte anche il Consejo Superior de Investigaciones Científicas (CSIC) è riuscito a decodificare il genoma del batterio antartico Oleispira antarctica RB-8, originariamente isolato nell’Oceano Antartico. Questo batterio, che si trova naturalmente nei mari e degli oceani, è in grado di degradare gli idrocarburi a bassissima temperatura (tra i 4 e i 6 gradi Celsius) e quindi potrebbe essere utilizzato per la decontaminazione dei fondali marini e delle aree polari. Biodegradazione della plastica: stando a uno studio pubblicato sulla rivista 'Environmental Science & Technology', i batteri contenuti nelle viscere di un bruco noto per mangiare gli imballaggi alimentari, infatti, possono degradare il polietilene (PE), cioè la plastica più comune (come quella dei sacchetti di plastica). 24 Progetto Genoma Progetto Genoma Umano (HGP, acronimo di Human Genome Project) è stato un progetto di ricerca scientifica internazionale il cui obiettivo principale era quello di determinare la sequenza delle coppie di basi azotate che formano il DNA e di identificare e mappare i geni del genoma umano dal punto di vista sia fisico sia funzionale. Il progetto è stato completato il 22 giugno 2000. Il "genoma" di qualsiasi individuo (tranne quello dei gemelli monozigoti e degli organismi clonati) è unico; mappare quindi il "genoma umano" significa fare il sequenziamento delle variazioni multiple di ciascun gene. Il progetto non ha studiato il DNA intero contenuto nelle cellule umane; alcune zone eterocromatiche (l'8% del totale circa) non sono ancora state sequenziate. Per portare a termine la ricerca si è lavorato sul DNA offerto da un certo numero di donatori selezionati con criteri di rappresentatività statistica. Nel 2011 è stato portato a termine e il primo essere umano a cui è stato decodificato il genoma è stato James Watson. Principali scoperte del progetto Genoma 1. Gli esseri umani hanno circa 28.000 geni, più o meno lo stesso numero di quelli dei topi e il doppio di quelli di alcune specie di vermi. La comprensione dell'espressione di questi geni potrà fornire degli indizi sulle cause di alcune malattie. 2. Tutte le etnie umane sono uguali al 99,99%, quindi presunte differenze razziali sono geneticamente insignificanti. 3. La maggior parte delle mutazioni genetiche avviene nel maschio della specie, il quale è quindi da considerare un agente del cambiamento. I maschi hanno quindi una responsabilità maggiore nella trasmissione delle anomalie genetiche e nell'evoluzione della specie. 4. La genomica ha portato a progressi nel campo dell'archeologia genetica e ha migliorato la nostra comprensione di come ci siamo evoluti in quanto esseri umani e di come ci siamo separati dai primati 25 milioni di anni fa. Ci aiuta anche a conoscere il funzionamento del nostro corpo, compreso il mistero del funzionamento del gusto. 25