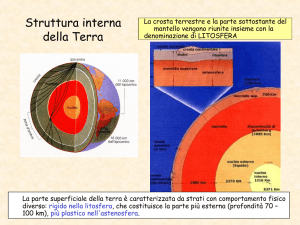
I MINERALI DEL SUOLO
Componenti
inorganici
aria
20-30%
acqua
20-30%
fase
solida
50-60%
Componenti
organici 5%
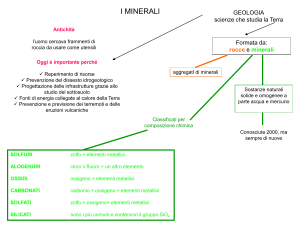
Composizione chimica media della litosfera (% in peso)
50
O
46,7
40
30
Si
27,7
%
Nutrienti
20
10
Al
8,1
Fe
5,1
Ca
3,7
Na
2,8
K
2,6
Mg
2,1
Altri
1,2
0
Gli elementi presenti in percentuale più elevata formano oltre 2000 minerali; solo
una dozzina si rinvengono con frequenza nelle rocce più comuni e nei suoli
I MINERALI
sostanze inorganiche
caratterizzate da composizione
chimica definita, o variabile entro
limiti ristretti, da proprietà fisiche
specifiche e da peculiare struttura
cristallina con disposizione
spaziale ordinata di atomi, ioni o
molecole
minerale
roccia
I MINERALI
Primari:
minerali che si sono formati a temperature elevate
(raffreddamento dei magmi) e derivano, generalmente, da rocce ignee,
metamorfiche o, anche, sedimentarie;
Secondari:
di neogenesi, minerali originatisi per reazioni a più basse
temperature, presenti solamente nelle rocce sedimentarie, o formatisi nel
corso del processo di pedogenesi
Sulla base della composizione chimica
si dividono in:
•SILICATI
•NON SILICATI
•Primari nelle frazioni sabbia e limo
•Secondari nella frazione argilla (∅
∅ < 2 µm)
I MINERALI
Minerali organizzati in strutture ioniche. Ciascun
catione circondato e legato da ioni di carica opposta.
Ione
Raggio
ionico (nm)
Rapporto radiale
catione/anione
Numero di
coordinazione
% legame
ionico
O2-
0.140
-
-
-
Si4+
0.039
0.278
4
51
Al3+
0.051
0.364
4-6
63
Fe3+
0.064
0.457
6
51
Mg2+
0.066
0.471
6
74
Fe2+
0.074
0.529
6
72
Na+
0.097
0.693
8
82
Ca2+
0.099
0.707
8
79
K+
0.133
0.950
8-12
84
I MINERALI
Disposizione nello spazio di ioni, di raggio ionico diverso,
considerati sfere rigide
Valori del rapporto tra Disposizione degli anioni
i raggi ionici
intorno al catione
(anione/catione)
Numero di
coordinazione
del catione
0.225 – 0.414
Vertici di un tetraedro
4
0.414 – 0.632
Vertici di un ottaedro
6
0.732 – 1.000
Vertici di un cubo
8
Disposizione caratterizzata da specifica geometria e da stabilità elettronica
I MINERALI
Cationi possono sostituirsi reciprocamente nella struttura
delle entità cristalline se:
•Il raggio ionico non è molto diverso
•La carica ionica non differisce di più di una unità di
valenza
•Resta inalterata la morfologia della struttura
Sostituzioni isomorfe eterovalenti determinano nel
cristallo eccesso di cariche negative
I MINERALI
A) Unità strutturale tetraedrica formata dalla coordinazione
di quattro ioni ossigeno da parte di uno ione silicio.
(r=0.041nm)
(r=0.050nm)
B) Unità strutturale ottaedrica formata dalla coordinazione
di sei ioni ossidrile da parte di uno ione alluminio.
The Silicon-Oxygen
Tetrahedron
O2 -
Si4+
O2 -
O2 The basis of most rock-forming
minerals, charge - 4
O2
-
I MINERALI
TETRAEDRO DI SILICIO
I MINERALI
P
P’
O
In un triangolo rettangolo, la misura di un cateto è uguale al
prodotto della misura dell’ipotenusa per il seno dell’angolo
opposto (al cateto)
I MINERALI
R = sen 54° 75’ * (R+r)
R = 0.186 * (R+r)
R = 0.816 R + 0.816r
0.816r = R – 0.816 R
0.816r = (1 – 0.816) R
0.816 r = 0.184 R
r = 0.184/0.816 R = 0.225 R
0.225 * 0.140 nm = 0.031 nm
I MINERALI
OTTAEDRO DI ALLUMINIO
I MINERALI
I MINERALI
I MINERALI
Modelli grafici di rappresentazione
a) ad impacchettamento di
sfere
b) a poliedri
c) a cerchi e segmenti
CLASSIFICAZIONE STRUTTURALE DEI SILICATI
NESOSILICATI
TETRAEDRI DI SILICIO INDIPENDENTI
[SiO44-]n
Example OLIVINE
Positive ion
Fe and Mg
[(Mg, Fe)2SiO4]
SiO4 -4 Ion
Tetrahedron
facing down
Tetrahedron
facing up
Independent tetrahedra
SOROSILICATI
Unione di due tetraedri di silicio con legame Si-O-Si
[Si2O76-]n
EPIDOTO
CICLOSILICATI – anelli esagonali di tetraedri di silicio
I ciclosilicati sono strutturalmente formati dalla sovrapposizione di
anelli a 6, più raramente a 3 o a 4, unità tetraedriche.
[Si6O1812-]n
[Be3Al2Si6O18]
INOSILICATI – CATENE SEMPLICI DI TETRAEDRI
Gli inosilicati (dal greco inos, fibra) comprendono i pirosseni e gli anfiboli.
Nei pirosseni i tetraedri sono disposti in catene singole di lunghezza non
definita.
[SiO32-]n
[CaMgSi2O6]
A Pyroxene
Single chains weakly paired
INOSILICATI – CATENE DOPPIE DI TETRAEDRI
Negli anfiboli due catene singole di unità tetraedriche sono unite insieme
a formare cavità esagonali.
[Si4O116-]n
[(Ca,Na)2(Mg,Fe,Al)5(Al,Si)8O22(OH)2])
An Amphibole
Positive
ion
Double chains
(c)
FILLOSILICATI
TETRAEDRI DISPOSTI SECONDO MAGLIE ESAGONALI
[Si4O104-]n
Sheet silicates
Visione dall’alto e di lato di un foglio tetraedrico
rappresentato secondo diversi modelli grafici
TECTOSILICATI reticolo tridimensionale di tetraedri
I tectosilicati (dal greco tectos, edificio) sono caratterizzati da
organizzazione strutturale tridimensionale dei tetraedri che
condividono tutti gli atomi di ossigeno
Quarzo: SiO2
Feldspati:
• ortoclasio, sanidino, microclino (KAlSi3O8)
• plagioclasi: albite [NaAlSi3O8] e anortite [CaAl2Si2O8]
Feldspatoidi:
• nefelina (NaAlSiO4)
• leucite (KAlSi2O6)
Zeoliti
Example: Quartz
SiO2
Framework silicates
(e)
(3-D, also the Feldspars)
Silicate Mineral Appearance
Mica
Feldspar
Olivine
Quartz
Pyroxene
FILLOSILICATI
TETRAEDRI DISPOSTI SECONDO MAGLIE ESAGONALI
[Si4O104-]n
Sheet silicates
Visione dall’alto e di lato di un foglio tetraedrico
rappresentato secondo diversi modelli grafici
FILLOSILICATI
foglio ottaedrico
a)
a)
diottaedrico
[Al2(OH)6]n
b)
b)
triottaedrico
[Mg3(OH)6]n
Fillosilicati primari
pirofillite
talco
Struttura della pirofillite (diottaedrica) e del talco (triottaedrica)
d=spaziatura basale
(distanza tra 2 strati
successivi lungo
l’asse
cristallografico c) =
0.930-0.960 nm
Deboli forze di van der Waals tengono uniti i pacchetti strutturali
Fillosilicati primari
Mica Biotite
Mica Muscovite
MICA MUSCOVITE (diottaedrica)
Al+3Si
6O
0.070 nm
1.0nm
2K
6O
Al+3Si
4O+2OH
4Al
4O+2OH
Al+3Si
6O
Summary
I non silicati
I carbonati: calcite (CaCO3), dolomite [(CaMg(CO3)2]
I fosfati: apatiti (fluoroapatite [Ca10(PO4)6F2], idrossiapatite
[Ca10(PO4)6OH2], etc.) – variscite [AlPO4.2H2O], vivianite
[Fe3(PO4)2.8H2O]
I solfati: gesso [CaSO4.2H2O]
I solfuri: pirite [FeS2], galena [PbS], blenda [ZnS]
Gli alogenuri: salgemma [NaCl]
Gli ossidi: gibbsite [γAl(OH)3], ematite [αFe2O3], goethite
[α FeOOH], magnetite [Fe3O4], quarzo [SiO2], rutilo [TiO2]
Non-silicate Mineral
Examples
Spinel
(Oxide)
Halite
(Halide)
Gypsum
(Sulfate)
Galena
(Sulfide)
Pyrite
(Sulfide)
Calcite
(Carbonate)
Hematite
(Oxide)