Domenico La Sala
INTERAZIONE TRA GLIA E DRG
INTRODUZIONE
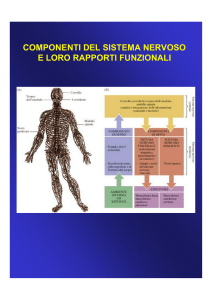
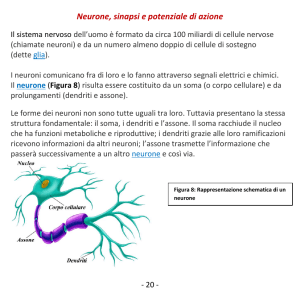
I gangli della radice dorsale (DRG) rappresentano il punto di transito delle afferenze sensitive e
sensoriali. Si compongono di neuroni pseudo unipolari associati strettamente alla glia periferica.
Studi recenti fanno emergere uno specifico “cross-talk” tra le due popolazioni cellulari sia in
condizioni fisiologiche che patologiche. In effetti, appurato che molte neuropatie abbiano una base
infiammatoria, ci si sta interrogando non solo sulle molecole coinvolte ma anche sul ruolo svolto
dalle popolazioni cellulari neuro-gliali. Questo lavoro avrà come scopo quello di chiarire come la
glia periferica partecipi alla nascita e al mantenimento del dolore cronico neuropatico interagendo
chimicamente con i neuroni nocicettivi dei DRG.
DISCUSSIONE
A seguito di una lesione che coinvolga le terminazioni nervose vengono rilasciate le citochine
TNF-α, IL-1β e IL-6. Queste ultime mediano la liberazione di altre citochine e chemochine
(citochine chemotattiche).
E’ stato appurato come alcuni di questi mediatori “a valle” rilasciati dalla glia periferica non solo
richiamino leucociti nel luogo dell’infiammazione ma interferiscano anche con i normali processi
di trasmissione neuronale. La chemochina MCP-1, ad esempio, legandosi ai propri recettori presenti
sui neuroni nocicettori dei DRG, provoca depolarizzazione, mobilizzazione di calcio e, dunque,
ipereccitazione. Si tratta di processi che, se prolungati, conducono alla neuropatia.
La glia è inoltre centrale nello sviluppo della
neuropatia conseguente all’AIDS.
ECCITABILITA’
NEURONALE
AUMENTATA
NEURO
NE
MCP-1 ,SDF1, RANTES
GLIA
HIV attiva le cellule gliali. La chemochina RANTES
rilasciata a seguito di ciò dalle stesse ha come target
nuovamente i neuroni nocicettori dei DRG che
vengono ipereccitati. Qualcosa di analogo avviene in
seguito a trattamento dell’AIDS con la zalcitabina.
Essa ha come effetto collaterale quello di stimolare
la glia alla liberazione della chemochina SDF-1, il
cui effetto secondario è quello di alterare
l’eccitabilità dei neuroni del dolore con la comparsa
di iperalgesia e iperallodinia.
CONCLUSIONE
Le ricerche sui meccanismi di interazione glia-neurone nella fisiologia e nella patologia neuronale
non sono terminate.
Questi primi risultati, tuttavia, sono significativi per un possibile utilizzo della glia come bersaglio
farmacologico nella cura delle neuropatie.
REFERENZE BIBLIOGRAFICHE
Cytokine and chemokine regulation of sensory neuron function.
Miller RJ, Jung H, Bhangoo SK, White FA.Molecular Pharmacology and Structural
Biochemistry, Northwestern University, Chicago, IL, USA. [email protected]