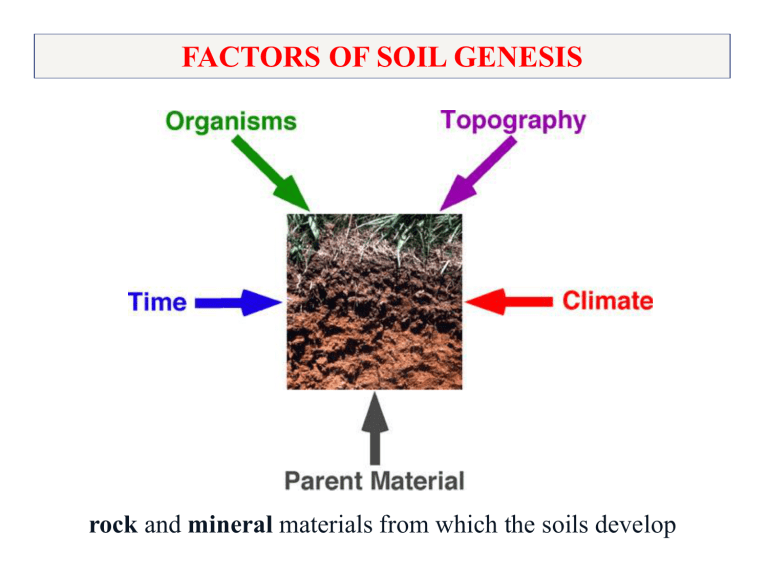
FACTORS OF SOIL GENESIS
rock and mineral materials from which the soils develop
LE ROCCE
Rocks are aggregates of minerals. Many are silicate minerals.
Granite, an igneous rock, has Quartz, an amphibole called Hornblende,
a pink potassium feldspar, and a white Plagioclase feldspar
Le rocce possono essere suddivise genericamente
in tre classi:
Ignee
Sedimentarie
Metamorfiche
Ignee + metamorfiche = 95% crosta terrestre, 25% superficie
Sedimetarie = 5% crosta terrestre, 75% superficie
ROCCE IGNEE O MAGMATICHE
Struttura granulare
Struttura porfirica
Struttura fine-media
Composizione mineralogica media delle rocce ignee (% in peso)
Sialiche
Ferromagnesiache o femiche
% SiO2
<45
45-51
52-66
>66
Correlazione tra la composizione chimica e la
composizione mineralogica delle rocce ignee
Classificazione delle rocce ignee
in base a composizione chimica e struttura
ROCCE SEDIMENTARIE
Processi di formazione:
Alterazione rocce preesistenti
Erosione e trasporto (acque, ghiaccio, vento)
Deposizione
Diagenesi (compattazione, cementazione, neogenesi)
Aree di erosione: Zone continentali interne
Aree di deposizione: Pianure costiere, delta fluviali, fondali
lacustri o marini poco profondi
Composizione mineralogica media
delle rocce sedimentarie (% in peso)
Classificazione delle rocce sedimentarie
basata su considerazioni genetiche
Le rocce sedimentarie clastiche (dal greco klastos: spezzato, rotto,
sminuzzato) derivano dall'accumulo di frammenti litici trasportati da
agenti esogeni diversi (corsi fluviali, correnti marine, venti, ecc.).
classificate in base alle dimensioni dei granuli che le compongono
Conglomerati, > 2 mm
Arenarie
0,0625-2 mm;
siltiti, 0,0625-0,004 mm.
argilliti, < 0,004 mm.
Le rocce sedimentarie di origine chimica si formano in seguito a
fenomeni chimico-fisici, dovuti soprattutto all'azione dell'acqua. Questa,
venendo a contatto con le rocce, scioglie i sali in esse presenti e li
trasporta con sé. Se l'acqua si raccoglie in un bacino chiuso, la
concentrazione dei sali andrà via via aumentando, fino a raggiungere il
punto di saturazione: quando questo punto viene superato (per aggiunta di
altri sali o per evaporazione dell'acqua), i sali cominciano a precipitare e a
depositarsi sul fondo, dando origine, in tempi più o meno lunghi, a vere e
proprie rocce. Con questo meccanismo si formano ad esempio il gesso, il
travertino, l’alabastro, la selce
Travertino, Caucaso, Russia
Gesso, Almería, Spagna
Le rocce sedimentarie di origine organogena si formano in
seguito all'attività degli organismi viventi. Molti organismi marini (alcuni
molluschi, alcune alghe unicellulari, i coralli, le madrepore) sottraggono
all'acqua i suoi sali e con essi costruiscono gusci e 'scheletri': quando
questi organismi muoiono, le loro parti minerali si depositano e si
accumulano sui fondali. Tali attività, tra l'altro, danno origine agli atolli e alle
barriere coralline. Nel corso della storia della Terra, molti depositi corallini
sono stati sollevati dalle forze endogene e sono andati a costituire
formazioni rocciose superficiali. Ne sono esempio le Dolomiti e il Gran
Sasso, formati da calcari di origine organogena.
calcare con bivalve
ROCCE RESIDUALI
Si tratta di rocce che derivano dall’accumulo in situ dei prodotti di alterazione di una
roccia affiorante.
Idrolisi dei silicati, la cui entità dipende dal regime climatico (principalmente
temperatura e precipitazioni), acidità dell’acqua (aumentata in ambiente tropicale
dalla dissoluzione di acidi organici legati alla copertura vegetale), dilavamento e
allontanamento di determinati elementi (ad esempio il silicio per le Lateriti) con
arricchimento di altri (ossidi ed idrossidi di Fe e Al per le Lateriti).
Principali rocce le lateriti e le bauxiti.
bauxite
laterite, India
ROCCE METAMORFICHE
Trasformazioni strutturali e mineralogiche di rocce ignee e
sedimentarie in seguito a condizioni di T e P diverse da quelle
dell’ambiente di genesi
Deformazioni meccaniche (pieghe, fratture) per adattamento dei
costituenti litici alle pressioni di carico (profondità, movimenti tettonici)
Ricristallizzazioni chimiche per aumento di T (fino 800 °C) e P
Ardesia- foliazione scistosa, dal
colore grigio piombo oppure nero.
Ha origine dalle argilliti.
Marmo- rocce calcaree
cristalline e granulari.
Principale minerale la calcite
Gneiss - composizione della roccia da cui
provengono, principalmente il granito:
quarzo e feldspato. Minerali appiattiti e
fasciati da laminette di mica, orientate
parallelamente ai piani di scistosità.
Rapporto tra le classi di rocce formatesi in diversi ambienti geologici
I PROCESSI DI ALTERAZIONE DEI COMPONENTI MINERALI
si dividono in:
FISICI, che portano alla disgregazione del materiale roccioso
senza determinarne variazioni nella composizione chimica e
mineralogica
CHIMICI, che provocano la completa decomposizione della
struttura e dell’associazione ionica dei minerali
Disgregazione e decomposizione si svolgono contemporaneamente
e risulta praticamente impossibile separarne gli effetti
Nelle regioni a clima arido prevalgono i processi di disgregazione,
in quelli a clima umido risultano più importanti i processi di
decomposizione
Nelle rocce come nel suolo
La DISGREGAZIONE delle rocce è generalmente
provocata dall’azione:
• dell’irraggiamento solare
• dei ghiacciai
• dell’acqua
• del vento
• delle entità biotiche
Per abbassamento della temperatura l’acqua presente
all’interno di crepe, spaccature e pori delle rocce tende
a passare dallo stato liquido a quello solido con
aumento di volume (CRIOCLASTISMO)
Le forze di espansione
dell’acqua che congela:
T (°C) P (atm)
0
100
-5
610
-10
1120
-20
1970
Masso glaciale disgregato nel Wallace Canyon
del Sequoia National Park, California
AZIONE DELLE ENTITÀ BIOTICHE
Penetrazione di rizomorfi di un lichene squamuloso in roccia calcarea
AZIONE DELLE ENTITÀ BIOTICHE
Cavità formatesi sulla
superficie rocciosa in
conseguenza
della
crescita di licheni
endolitici
(Garty,
1992)
1 mm
V
(mm)
(mm3 )
0.5-0.8
0.033-0.134
N/cm2
50
Vtot
(mm3 /cm2 )
Quantità di
gesso asportata
(kg/ha)
1.635-6.698
425-1740
La DECOMPOSIZIONE dei minerali disgregati è definita
da reazioni di:
• Idrolisi
• Idratazione e disidratazione
• Scambio ionico
• Solubilizzazione
• Ossidazione
• Chelazione
Le reazioni di decomposizione sono regolate dalle leggi
dell’equilibrio chimico, pertanto possono continuare oltre
lo stato di equilibrio solamente se componenti sono
aggiunti o sottratti al sistema
AREA SUPERFICIALE E VELOCITA’ DI DECOMPOSIZIONE
Lunghezza
del lato
2 cm
2 cm
Superficie totale
24 cm2
1 cm
48 cm2
1 mm
480 cm2
0.1 mm
4800 cm2
0.01 mm
1 m
1 cm
48000 cm2
48 m2
Aumento delle superfici di contatto tra minerali ed agenti di alterazione
INFLUENZA DELL’AREA
SUPERFICIALE
500 m
Particella di sabbia
100 m
Particella di cenere
vulcanica con struttura
porosa
Reazioni di idrolisi
L’acqua in cui possono trovarsi presenti innumerevoli
specie ioniche, reagisce con silicati ed alluminosilicati:
• Silicati + H2O + H2CO3
cationi + OH- + HCO3- + H4SiO4
• Alluminosilicati + H2O + H2CO3
OH- + HCO3- + H4SiO4
minerali argillosi + cationi +
Per azione dell’acqua vengono risolti
i legami tra cationi, Al3+, Si4+ e O2-
H
Si
O
Al
:O
H
H+
O
Si
O
O
H+
Al
O
O
Na+
:O
H
H
OH-
Si
Schematizzazione dell’azione idrolitica dell’acqua e dei
suoi prodotti di dissociazione
Energia di formazione di legami catione-ossigeno
catione
Si4+
Al3+
Fe3+
Mg2+
Ca2+
H+ (in OH)
Na+
K+
kJ mol-1)
13164.9 – 13030.9
7868.8 – 7512.7
3850.6
3821.3
3515.4
2157.8
1349.2
1252.8
Azione della CO2 nell’idrolisi dei silicati contenenti calcio
2CO2 + 2H2O
Ca2+
2H2CO3
2H+
+
2HCO3-
Ca-feldspato
Ca(HCO3)2
CaCO3 + H2O + CO2
Ca sottratto all’equilibrio:
- precipitato come carbonato
(cristallizza come calcite)
- allontanato per lisciviazione
come bicarbonato
Calcite
Reazioni di idratazione e disidratazione
(formazione di nuove entità mineralogiche per addizione o rimozione di
molecole di acqua)
CaSO4 + 2H2O CaSO4 – 2H2O
(anidrite)
(gesso)
Aumento di volume
Importanza limitata:
interessano un numero limitato di minerali
Reazioni di solubilizzazione
NaCl, CaSO4.2H2O
CaCO3 + H2O + CO2 Ca2+ + 2HCO3In assenza di CO2 : 14 mg l-1
In presenza dello 0.03% in volume di CO2: 58 mg l-1
In presenza dello 0.3% in volume di CO2: 127 mg l-1
> decomposizione rocce carbonatiche nelle regioni a clima freddo
SOLUBILIZZAZIONE DEL CALCARE
Reazioni di ossidazione
Fe2+ Fe3+ + eFe2SiO4 + 2H2CO3 + 2H2O 2Fe2+ + 2OH- + 2HCO3- + H4SiO4 (idrolisi)
fayalite
2Fe2+ + 4HCO3- + O2 + 2H2O Fe2O3 + 4H2CO3 (ossidazione)
ematite
Decorrono in fase solida o in presenza di acqua ed hanno
importanza nella decomposizione di molti minerali
REAZIONI DI CHELAZIONE
Molecole organiche donatrici di una o più coppie di elettroni
(leganti) stabiliscono uno o più legami di coordinazione con uno
ione metallico, accettore di elettroni, formando strutture ad
anello più o meno stabili.
Struttura dei chelati che acidi organici di basso peso
molecolare possono formare con Al3+
Disposizione di leganti mono-, bi- ed
esadentati in coordinazione ottaedrica e
schematizzazione tridimensionale di
alcuni complessi
Leganti organici (LMW, essudati
radicali, attività microbica o
decomposizione
della
SO)
formano complessi ionici solubili
con ioni metallici in soluzione.
Leganti anionici influenzano la
distribuzione elettronica di ioni
metallici: < adsorbimento e
precipitazione.
In genere leganti disposti ai vertici
di un ottaedro attorno all'atomo
centrale. Al variare degli insiemi
di
orbitali
utilizzati
nella
formazione
dei
legami
si
realizzano
coordinazioni
a
geometria piana quadrata e
tetraedrica.
Stabilità all’alterazione di alcuni minerali primari
più stabile
Non femici
Anortite
(Ca – plagioclasio)
.
Ca – Na plagioclasio
.
Na – Ca plagioclasio
.
Albite
(Na – plagioclasio)
.
Ortoclasio
(K – feldspato)
.
Muscovite
.
Quarzo
ORDINE DI CRISTALLIZZAZIONE
STABILITA’ CRESCENTE
Femici
Meno stabile
Olivina
.
.
Iperstene
.
Augite
.
Orneblenda
.
.
Biotite
.
.











