Incontri educativo-informativi sul tema della fertilita’
Il laboratorio di analisi ormonale
Prof. Antonio F. Radicioni
Laboratorio di Endocrinologia - Sezione di Fisiopatologia Medica,
Dipartimento di Medicina Sperimentale – Sapienza Università di Roma
L’endocrinologia come scienza autonoma è nata nel 1909, ma solo 50 anni dopo, nel 1960, è iniziata
l’ormonologia, intesa come la possibilità di disporre di dosaggi ormonali di tipo quantitativo. In questo
momento il laboratorio è diventato un ausilio determinante ed irrinunciabile per l’endocrinologo clinico.
Molti ormoni hanno una secrezione pulsatile, in particolare le gonadotropine, legate alla pulsatilità dei
releasing hormone (RH) ipotalamici. Inoltre, la maggior parte degli ormoni prodotti nel nostro organismo,
presenta una caratteristica secrezione ritmica che, in base alla lunghezza del periodo, può essere circadiana,
infradiana o ultradiana. Tali peculiarità secretive, la differente emivita delle diverse molecole oltre ai
differenti quesiti diagnostici, possono condizionare l’orario e le modalità ottimali del prelievo ematico.
La diagnostica dell’infertilità maschile si basa sull’anamnesi personale e sull’esame obiettivo generale e del
sistema genitale, momenti essenziali e imprescindibili ai fini di una corretta gestione del paziente, ma anche
su indagini laboratoristiche e strumentali.
Nei casi di infertilità, lo spermiogramma costituisce il primo accertamento perché permette di avere una
stima diretta della capacità fecondante dell’individuo, ma anche di formulare le diverse ipotesi diagnostiche
in base alle modificazioni dei principali parametri valutati quali la concentrazione, la motilità e la morfologia
nemaspermica. La diagnostica ormonale di primo livello, che prevede il dosaggio di FSH, LH e testosterone
(Te), può permettere di evidenziare quattro possibili quadri:
1. LH, FSH e Te nella norma;
2. LH ed FSH elevati con bassi valori di Te (insufficienza testicolare primitiva);
3. LH ed FSH bassi o normali con bassi valori di Te (insufficienza testicolare secondaria);
4. LH normale, FSH elevato e Te normale (condizioni diverse di sofferenza tubulare).
Successivamente, è possibile utilizzare anche il dosaggio della prolattina (PRL) e dell’estradiolo (E2): la
prima, se elevata, può determinare un’importante interferenza con la secrezione pulsatile di GnRH e di
conseguenza può alterare l’integrità funzionale dell’asse ipotalamo-ipofisi-gonadi, mentre il dosaggio
dell’estrogeno è utile nella valutazione dell’attività aromatasica del testicolo, nella valutazione del rapporto
tra l’E2/Te e nella diagnosi di eventuali patologie sistemiche (epatopatie). In alcuni casi può essere utile
studiare la funzione tiroidea (TSH, fT3 ed fT4).
Una riflessione più approfondita merita il testosterone. Questo steroide è l’androgeno più importante
nell’uomo, viene secreto in modo pulsatile ma, a causa della tappa di deposito post-secrezione e del legame
plasmatico, non corrisponde al ritmo di secrezione dell’LH. Infatti, sebbene un piccolo aumento della
concentrazione di Te si può avere già 2-4 ore dopo il picco di LH, il massimo incremento si ottiene con un
ritardo variabile fra 27-72 ore. Il Te presenta un ritmo circadiano con picchi tra le 04:00 e le 08:00 del
mattino ed un nadir fra le 16:00 e le 20:00 con differenze ematiche di circa il 20-30%. Nell’età adulta i valori
normali sono compresi tra 9,7-38,1 nmol/l (2,8-11,0 ng/ml). Il Te circola nel sangue legato alla SHBG
(legame specifico), all’albumina (legame non specifico) ed in minima parte libero. Si ritiene che la frazione dello
steroide biodisponibile, o Te non legato alla SHBG sia costituita dalla somma della quota libera (fTe) e della
quota legata in maniera aspecifica all’albumina (ATe). La concentrazione di tale frazione sembra
Inquadramento clinico-diagnostico dell'infertilità – 02 luglio 2012
Incontri educativo-informativi sul tema della fertilita’
dimostrare una migliore correlazione con la condizione clinica di reale androgenizzazzione, rispetto ai livelli
del Te totale.
Sono state proposte diverse metodiche per affrontare tale importante problema: il fTe è stato misurato
mediante la metodica della dialisi all’equilibrio; il Te non legato alla SHBG è stato valutato mediante la
precipitazione con ammonio solfato. Data la complessità delle due precedenti metodiche, molti autori
preferiscono il calcolo dell’indice degli androgeni liberi (free androgen index) calcolato come rapporto: FAI =
(Te/SHBG) x 100
Per il dosaggio del fTe è stata utilizzata anche una metodica RIA relativamente semplice, ma secondo la
maggior parte degli autori scarsamente affidabile perché tende a sottostimare la concentrazione
dell’ormone rispetto ai valori ottenuti con la metodica della dialisi.
Per quanto concerne le analisi di secondo livello, nei casi di deficit gonadotropinico, può essere utile
l’esecuzione del test al GnRH, con lo scopo di valutare la riserva ipofisaria di FSH ed LH. Il test si effettua
somministrando 100 μg ev di GnRH sintetico e valutando la risposta delle gonadotropine dal tempo -30 a
+120 minuti. Nel caso di danno ipofisario la risposta risulta ridotta o assente, mentre sarà presente nel caso
di patologia ipotalamica.
Oltre a quelli già citati, altri ormoni permettono di approfondire in maniera specifica lo studio della gonade
maschile. Accenneremo alla fisiopatologia della sintesi e secrezione di questi, perché, a nostro avviso, solo
la reale conoscenza della funzione di un determinato ormone può permetterne un corretto utilizzo nell’iter
diagnostico.
Nel 1932 McCullagh ha dimostrato l’esistenza di una sostanza, prodotta dal testicolo, in grado di inibire la
formazione, nell’ipofisi, delle cellule da castrazione, e per questo da lui chiamata inibina. L’inibina B (InhB)
appartiene alla superfamiglia dei TGF β (trasforming growth factors) che sono fattori di crescita che hanno
un’azione importante nella crescita e differenziazione di diversi tessuti e strutturalmente è un eterodimero
costituito da una catena α ed una β. Nell’adulto la catena α continua ad essere prodotta dalla cellula di
Sertoli, mentre la catena β viene prodotta dalle cellule della linea spermatogenetica, dallo spermatocita in
pachitene fino allo spermatide rotondo. Per tale motivo questo ormone, che inibisce l’FSH, costituisce un
ottimo indice di funzione del distretto tubulare del testicolo e la sua concentrazione correla positivamente
con la concentrazione nemaspermica.
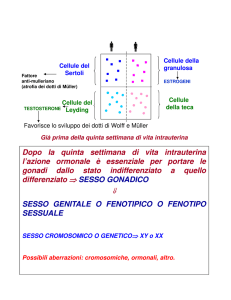
L’ormone antimülleriano (AMH), descritto da Alfred Jost nel 1947, viene prodotto dalle cellule del Sertoli
della gonade fetale e determina la regressione dei dotti del Müller. Durante l’infanzia e la prima parte della
pubertà costituisce un buon indice di funzione del testicolo ed in particolare delle cellule del Sertoli. Con
l’aumentare dei livelli del testosterone il gene per l’AMH subisce una down regulation fino a livelli circolanti
non più diagnostici ed è quindi scarsamente utilizzabile nel paziente adulto.
In conclusione quindi, anche grazie alla diffusione di metodiche sempre più sensibili e riproducibili, il
laboratorio di ormonologia dimostra un ruolo critico nell’iter diagnostico del paziente infertile, ma anche
nella prevenzione di molte patologie dell’infanzia e della pubertà che, se non adeguatamente identificate e
curate, possono compromettere lo sviluppo della gonade e la futura fertilità del soggetto.
Inquadramento clinico-diagnostico dell'infertilità – 02 luglio 2012