PER MANTENERSI, CRESCERE, MOLTIPLICARSI LE
CELLULE NECESSITANO DI:
MATERIA
ENERGIA
INFORMAZIONE
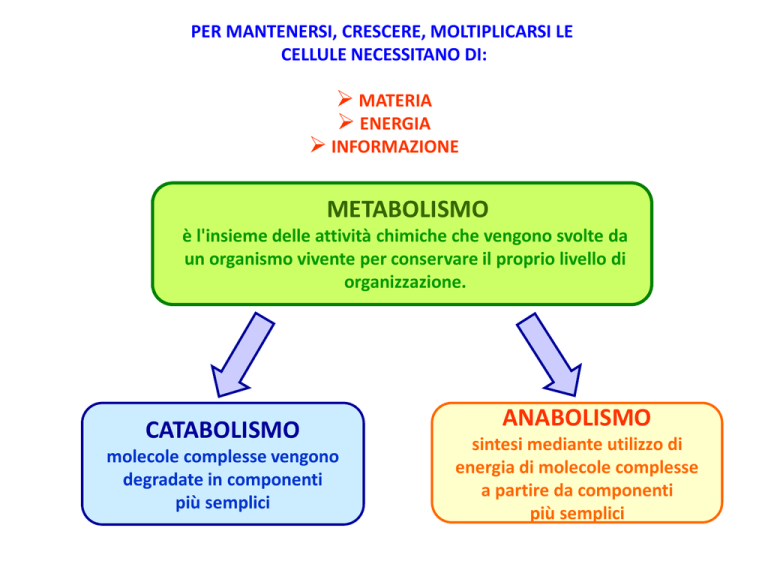
METABOLISMO
è l'insieme delle attività chimiche che vengono svolte da
un organismo vivente per conservare il proprio livello di
organizzazione.
CATABOLISMO
molecole complesse vengono
degradate in componenti
più semplici
ANABOLISMO
sintesi mediante utilizzo di
energia di molecole complesse
a partire da componenti
più semplici
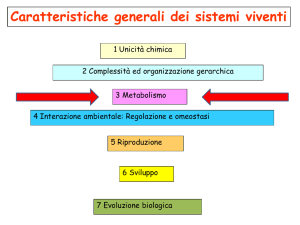
Caratteristiche fondamentali delle cellule sono:
- CAPACITA’ DI DIRIGERE LE REAZIONI CHIMICHE
- DI ORGANIZZARE LE MOLECOLE IN STRUTTURE SPECIFICHE
La cellula batterica deve costruire 4 classi di
macromolecole biologiche
COSTITUENTI PRINCIPALI DELLA CELLULA:
POLISACCARIDI
LIPIDI
ACIDI NUCLEICI
PROTEINE
• Gli organismi viventi devono rispettare le leggi della termodinamica
(una scienza che studia i cambiamenti di energia in una porzione di materia chiamata “sistema” e.s., una cellula)
La seconda legge della termodinamica afferma che tutti i processi
naturali tendono a passare da uno stato di ordine ad uno di
disordine AUMENTO DELL’ENTROPIA
in ogni sistema chiuso (confinato) la quantità di entropia
(disordine) tende ad aumentare
•
Apparentemente la straordinaria complessità degli organismi viventi sembra
contraddire questa legge
•
Perciò i sistemi viventi non sono all’equilibrio (termodinamico)
Il “sistema cellula” è un sistema altamente organizzato
Per raggiungere uno stato di ordine, con diminuzione dell’entropia,
deve essere compiuto un LAVORO fornendo energia al sistema
ENERGIA = capacità di compiere un lavoro
di effettuare delle trasformazioni
…compiere operazioni ordinate (movimento, differenziamento)
MECCANICO
energia richiesta per modificare la posizione
delle cellule oppure di strutture all’interno delle
cellule (motilità cellulare e movimento di strutture
nella cellula)
… mantenere l’organizzazione molecolare e sopramolecolare (omeostasi)
DI TRASPORTO
energia richiesta per introdurre nutrienti,
eliminare prodotti di rifiuto e mantenimento
dei bilanciamenti ionici
…accrescersi e riprodursi
CHIMICO
energia richiesta per aumentare la complessità
molecolare di una cellula (sintesi di macromolecole)
Il “sistema cellula” per compiere un «lavoro» deve trasformare le forme di
energia disponibili nell’ambiente (energia luminosa e sostanze chimiche)
nelle due forme principali di energia metabolica:
ENERGIA CHIMICA (ATP, GTP…)
POTERE RIDUCENTE (NADH, NADPH, FADH)
Ciò avviene mediante una serie di reazioni chimiche
(REAZIONI DI OSSIDO RIDUZIONE) catalizzate dagli ENZIMI
Considerando una reazione chimica:
A+B
C+D
Questa procederà dalla condizione iniziale ad una finale in cui sarà raggiunto
l’equilibrio tra le concentrazioni dei reagenti e dei prodotti
la quantità di reagenti che si trasforma in prodotti equivale
alla quantità di prodotti che si trasforma in reagenti
Equilibrio chimico
il parametro termodinamico che misura l’energia chimica di un sistema
in condizioni standard di concentrazione, pressione, temperatura e pH è
l’Energia libera G
• Per ogni composto si può calcolare l’ENERGIA LIBERA DI FORMAZIONE G0f
(energia richiesta o rilasciata per formare una molecola a partire dagli elementi chimici che la
compongono)
•
Partendo dall’energia di formazione dei reagenti e dei prodottidi una reazione chimica si può
calcolare la:
VARIAZIONE di ENERGIA LIBERA in condizioni standard DG0 (1M, 25°C, 1 atm)
LE REAZIONI CHIMICHE SONO ACCOMPAGNATE
DA VARIAZIONI DI ENERGIA
REAZIONE ESOERGONICA
i reagenti possiedono più energia dei
prodotti; avvengono perciò, secondo i principi
della termodinamica, spontaneamente e
l'energia in eccesso viene liberata durante la
reazione, in genere come calore.
avviene con liberazione di energia
REAZIONE ENDOERGONICA
i prodotti possiedono più energia dei
reagenti, per cui le reazioni avvengono solo
se si fornisce energia dall'esterno.
richiede energia
Reazioni Esoergoniche
Reazioni Endoergoniche
A+B
A+B
C+D
DGo´ è negativo
(la reazione procede
spontaneamente)
C+D
DGo´ è positivo
(la reazione non procede
spontaneamente)
Il calcolo dell’energia liberata o richiesta in una reazione non ci dice
nulla sulla VELOCITA’ della reazione
Non è detto, tuttavia, che le reazioni spontanee
possano procedere con una velocità apprezzabile
CATALIZZATORE = ENZIMI
Diminuisce l’energia di attivazione
Aumenta la velocità della reazione
Gli ENZIMI funzionano in maniera
altamente specifica
Gli enzimi partecipano alle reazioni senza essere consumati o trasformati
Come fanno gli enzimi ad abbassare l’Ea ?
•
•
aumentando le concentrazioni dei substrati al sito attivo dell’enzima
orientando correttamente i substrati l’uno rispetto all’altro per formare il
transition-state complex
PERCORSO AMFIBOLICO
Processi metabolici che contengono una componente anabolica ed una catabolica
La maggior parte delle reazioni
sono reversibili e possono
essere utilizzate sia per
sintetizzare che per degradare
molecole
A
B
La presenza di enzimi separati
consente la regolazione
indipendente della funzione
catabolica e anabolica
D
F
CATABOLISMO
E1
Le poche reazioni irreversibili nei
processi catabolici possono essere
superate, nelle biosintesi da enzimi
specifici che catalizzano la reazione
inversa
C
ANABOLISMO
E2
G
J
LE REAZIONI CHIMICHE NEGLI ORGANISMI VIVENTI
SONO REAZIONI DI OSSIDO-RIDUZIONE (trasferimento di elettroni)
OSSIDAZIONE = rimozione di uno o più elettroni da una sostanza
RIDUZIONE = aggiunta di uno o più elettroni ad una sostanza
L’ossidazione e la riduzione coinvolgono il trasferimento di elettroni sotto
forma di atomi di idrogeno (1 elettrone e 1 protone):
DEIDROGENAZIONE / IDROGENAZIONE
AH2 + B
BH2 + A
Il componente AH2 DONATORE, trasferisce H2 (si OSSIDA) al
componente B ACCETTORE (che si RIDUCE)
PER OGNI OSSIDAZIONE OCCORRE CHE AVVENGA UNA
CONSEGUENTE RIDUZIONE (COPPIA REDOX)
DONATORE DI ELETTRONI - RIDUCENTE => SOSTANZA OSSIDATA
ACCETTORE DI ELETTRONI - OSSIDANTE => SOSTANZA RIDOTTA
Le sostanze variano nella propria tendenza ad ossidarsi o
ridursi, tale tendenza viene detta:
POTENZIALE DI RIDUZIONE E0
(misura quantitativa della tendenza di una sostanza a cedere
elettroni nei sistemi biologici)
PIU’ E’ NEGATIVO > TENDENZA A CEDERE e-
E0 più negativo miglior donatore di elettroni
E0 più positivo miglior accettore di elettroni
La reazione di ossidazione avviene
con RILASCIO di energia
MAGGIORE E’ LA DIFFERENZA DI
POTENZIALE DI RIDUZIONE TRA
DONATORE ED ACCETTORE, MAGGIORE
E’ L’ENERGIA RILASCIATA
In alto i riducenti più forti, in basso gli ossidanti
Quando gli e- vengono donati (dalla cima
della torre) possono essere “catturati” dagli
accettori dei vari livelli
La torre degli elettroni
MIGLIORI DONATORI
DI ELETTRONI
MAGGIORE E’ LA DIFFERENZA DI
POTENZIALE DI RIDUZIONE TRA
DONATORE ED ACCETTORE, MAGGIORE
E’ L’ENERGIA RILASCIATA
NEL CATABOLISMO IL DONATORE DI
ELETTRONI VIENE ANCHE DETTO
FONTE DI ENERGIA
MIGLIORI ACCETTORI
DI ELETTRONI
Un composto chimico per essere una buona «fonte di energia»
deve avere una notevole capacità di OSSIDARSI, ossia deve
avere una elevata capacità di ridurre un altro composto:
deve essere cioè un FORTE RIDUCENTE
RIDUCENTI INORGANICI
RIDUCENTI ORGANICI
NH4+
NO3-
C6H1206
2CH300H
Fe2+
Fe3+
glucosio
Acido piruvico
CO
CO2
S2-
S
SO22-
SO42-
Nella cellula, in una reazione di ossido-riduzione, il trasferimento di elettroni
(e di protoni) da un donatore primario ad un accettore terminale, NON avviene
in un unico passaggio ma mediante reazioni di ossido riduzioni intermedie che
coinvolgono delle molecole dette TRASPORTATORI
TRASPORTATORI
CITOPLASMATICI =
(Liberi, diffusibili
COENZIMI)
NUCLEOTIDI PIRIDINICI
- NAD Nicotinamide Adenina Dinucleotide
- NADP Nicotinamide Adenina Dinucleotide Fosfato
- FAD Flavin Adenina Dinucleotide
NADH deidrogenasi
FLAVOPROTEINE contengono nucleotidi flavinici
- FMN Flavin Mononucleotide
I COENZIMI SONO TRASPORTATORI DI PROTONI
DI MEMBRANA =
PROTEINE FERRO-ZOLFO
CHINONI
CITOCROMI
•
•
NAD
– nicotinamide adenin dinucleotide
NADP
– nicotinamide adenin dinucleotide fosfato
•
FAD
– flavin adenin dinucleotide
•
FMN
– flavin mononucleotide
PROTEINE FERRO-ZOLFO
Proteine che contengono 2, 4 oppure 8
atomi di zolfo e ferro
2Fe-2S
4Fe-4S
8Fe-8S
CITOCROMI
Proteine associate a un gruppo eme
(componente non proteica)
che contiene ferro che può trovarsi
nella forma ridotta (Fe++) o nella forma
ossidata (Fe+++) e che può legare ossigeno
- Citocromo a
- Citocromo b
- Citocromo c
CHINONI: Coenzimi Q
Trasportatori non proteici
Molto lipofilico con catena laterale
isoprenica di lunghezza variabile nei
vari organismi
SOSTANZE
CHIMICHE
FONTI DI ENERGIA
CHEMIOTROFI
composti chimici
come fonte di energia
SOSTANZE
ORGANICHE
FOTOTROFI
Utilizzano la luce
come fonte di energia
SOSTANZE
INORGANICHE
CHEMIOLITOTROFI
(ossidano composti
inorganici)
FONTI DI CARBONIO
CHEMIORGANOTROFI
(ossidano composti organici)
FOTOAUTOTROFI
C=CO2
CHEMIOLITOTROFI
AUTOTROFI
C=CO2
CHEMIORGANOTROFI
ETEROTROFI
C=Organico
FOTOETEROTROFI
C=Organico
METABOLISMO
CATABOLISMO
molecole complesse vengono
degradate in componenti
più semplici
RILASCIO DI ENERGIA
CALORE
ANABOLISMO
sintesi mediante utilizzo di
energia di molecole complesse
a partire da componenti
più semplici
ATP
La sintesi di ATP è una reazione
ENDOERGONICA (richiede energia)
pertanto viene accoppiata con altre
reazioni che rilasciano energia
(ESOERGONICHE) e che avvengono
durante il catabolismo dei donatori di
elettroni.
L’energia rilasciata come risultato delle reazioni di ossido-riduzione
deve essere conservata per le funzioni cellulari
L’energia chimica liberata viene conservata sotto forma di
LEGAMI CHIMICI AD ALTA ENERGIA LA CUI IDROLISI
LIBERA UNA NOTEVOLE QUANTITA’ DI ENERGIA
ATP (Adenosintrifosfato)
coenzima A (acetil-CoA)
GRUPPO FUNZIONALE -O-PO2-O-PO2-O-
DUE LEGAMI FOSFOANIDRIDICI
AD ALTA ENERGIA
SINTESI DELL’ATP: aggiunta di un fosfato inorganico (Pi) all’ADP
+ Pi + ENERGIA
ADP
IDROLISI DELL’ATP
+PPi
+ Pi
ADP
AMP
SINTESI DELL’ATP: aggiunta di un fosfato inorganico (Pi) all’ADP
FOSFORILAZIONE A LIVELLO DEL SUBSTRATO:
trasferimento diretto di un gruppo fosfato ad
alta energia da un substrato fosforilato
all’ADP
SINTESI DELL’ATP: aggiunta di un fosfato inorganico (Pi) all’ADP
FOSFORILAZIONE A LIVELLO DI
MEMBRANA:
quando la reazione di aggiunta di un Pi è
catalizzata da un enzima di membrana che si
chiama ATP sintasi (o ATPasi)
ALTRE MOLECOLE CON ALTO
POTENZIALE DI TRASFERIMENTO
DEL GRUPPO FOSFORICO
L’energia viene immagazzinata in questo legame tioestere
In aggiunta ai composti fosfati ad alta
energia esistono altri composti che possono
conservare energia prodotta dalle reazioni
esoergoniche: DERIVATI DEL COENZIMA A
acetil-CoA contiene un legame sulfo-anidridico (tioestere)
invece che fosfo anidridico e nell’idrolisi sviluppa energia
sufficiente per condurre la sintesi di un legame fosfato ad
alta energia (ATP)
chemiotrofia
Fonte di energia
(Donatore di elettroni)
Accettore di elettroni
chemiotrofia
SOSTANZE
CHIMICHE
OSSIDAZIONE
SOSTANZE
ORGANICHE
OSSIDAZIONE
CHEMIOTROFI
composti chimici
come fonte di energia
SOSTANZE
INORGANICHE
CHEMIORGANOTROFI
(composti organici)
CHEMIOLITOTROFI
(composti inorganici)
FONTE DI C = sostanze organiche
CHEMIOETEROTROFI
FONTE DI C = CO2
CHEMIOAUTOTROFI
Alcuni sono eterotrofi facoltativi
FERMENTAZIONE
PROCESSI CHEMIOTROFICI suddivisi in:
RESPIRAZIONE
FERMENTAZIONE
PROCESSI CHEMIOTROFICI suddivisi in:
RESPIRAZIONE
FERMENTAZIONE parziale ossidazione di un substrato ORGANICO
gli elettroni ceduti sono ceduti ad un’altra molecola organica
interna al processo (che deriva dalla ossidazione parziale dello
stesso substrato di partenza)
- NON RICHIEDE OSSIGENO (anaerobi obbligati, anaerobi facoltativi)
- NON RICHIEDE ACCETTORI DI ELETTRONI ESTERNI AL PROCESSO
FERMENTAZIONE
PROCESSI CHEMIOTROFICI suddivisi in:
RESPIRAZIONE
RESPIRAZIONE ossidazione TOTALE di un substrato ORGANICO O INORGANICO
gli elettroni ceduti sono giungono ad un ACCETTORE FINALE
che è una MOLECOLA INORGANICA OSSIDATA
- AEROBIA accettore finale OSSIGENO
- ANAEROBIA accettore finale molecola inorganica ossidata diversa
chemiotrofia
SOSTANZE
CHIMICHE
OSSIDAZIONE
OSSIDAZIONE
CHEMIOTROFI
composti chimici
come fonte di energia
SOSTANZE
ORGANICHE
SOSTANZE
INORGANICHE
CHEMIORGANOTROFI
(composti organici)
CHEMIOLITOTROFI
(composti inorganici)
FONTE DI C = sostanze organiche
CHEMIOETEROTROFI
FONTE DI C = CO2
CHEMIOAUTOTROFI
Alcuni sono eterotrofi facoltativi
RESPIRAZIONE
FERMENTAZIONE
RESPIRAZIONE
AEROBICA:
Accettore finale O2
ANAEROBICA:
Accettore finale DIVERSO
dall’ O2:
composto inorganico
ossidato
Non c’è un accettore
finale esterno.
L‘ossidazione è associata alla
riduzione di un
composto
organico prodotto durante il
processo
IN ANAEROBIOSI
AEROBICA:
Accettore finale O2
CHEMIORGANOTROFI
(composti organici)
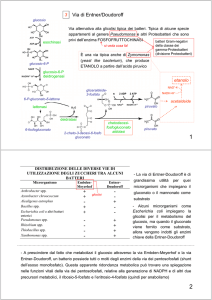
IL GLUCOSIO E’ UN SUBSTRATO UNIVERSALE PER TUTTE
LE CELLULE ETEROTROFE
Qual è il destino del GLUCOSIO in una cellula batterica?
GLUCOSIO
GLICOLISI
(via di Embden-Meyerhof)
Pathway dei
PENTOSO-FOSFATI
Pathway di
ENTNER-DOUDOROFF
PIRUVATO
RESPIRAZIONE
AEROBICA
RESPIRAZIONE
ANAEROBICA
FERMENTAZIONE
Lattica, eterolattica
alcolica, acido mista
In condizioni anaerobiche
GLICOLISI
(via di Embden-Meyerhof)
Fase I
Reazioni di preparazione:
il glucosio viene fosforilato e scisso
in due molecole di
gliceraldeide-3-fosfato
In questo processo vengono utilizzate
due molecole di ATP
Fase II
Reazioni di ossidazione: le due molecole di gliceraldeide-3-fosfato
vengono trasformate in due molecole di piruvato con contestuale
produzione di quattro molecole di ATP
BILANCIO ENERGETICO DELLA GLICOLISI
CHEMIORGANOTROFI
(composti organici)
IL GLUCOSIO E’ UN SUBSTRATO UNIVERSALE PER TUTTE
LE CELLULE ETEROTROFE
Qual è il destino del GLUCOSIO in una cellula batterica?
GLUCOSIO
GLICOLISI
(via di Embden-Meyerhof)
Pathway dei
PENTOSO-FOSFATI
Pathway di
ENTNER-DOUDOROFF
PIRUVATO
RESPIRAZIONE
AEROBICA
RESPIRAZIONE
ANAEROBICA
FERMENTAZIONE
Lattica, eterolattica
alcolica, acido mista
In condizioni anaerobiche
Via dei PENTOSO-FOSFATI
- può decorrere
contemporaneamente alla via
glicolitica
- può operare sia in modo
anaerobio che aerobio
- è importante sia per le
biosintesi che per il catabolismo
Via dei PENTOSO-FOSFATI
- il glucosio-6-fosfato viene ossidato a 6-fosfogluconato
- seguito dalla ulteriore ossidazione a ribulosio 5-fofato e CO2
Si ha produzione di NADPH
Il ribulosio 5-P viene utilizzato
come precursore dei nucleotidi
Il ribulosio 5-fosfato viene convertito in
una miscela costituita da due zuccheri
fosforilati:
zucchero a 7 atomi di carbonio
(sedoeptulosio 7-fosfato)
gliceraldeide 3-fosfato
I due enzimi chiave di questo processo sono:
TRANSCHETOLASI e TRANSALDOLASI
che portano alla formazione di 2 molecole di
fruttosio 6-fosfato e di gliceraldeide 3-fosfato
Il fruttosio 6-fosfato può essere
riconvertito a glucosio 6-fosfato
e la gliceraldeide 3-fosfato viene
convertita ad acido piruvico dagli
enzimi glicolitici
VIA METABOLICA:
- utilizzata per la produzione di ATP
- il NADPH viene utilizzato come
fonte di elettroni per la riduzione
delle molecole durante le biosintesi
- produce zuccheri a 4 e 5 atomi di
C (sintesi acidi nucleici, fotosintesi)
CHEMIORGANOTROFI
(composti organici)
IL GLUCOSIO E’ UN SUBSTRATO UNIVERSALE PER TUTTE
LE CELLULE ETEROTROFE
Qual è il destino del GLUCOSIO in una cellula batterica?
GLUCOSIO
GLICOLISI
(via di Embden-Meyerhof)
Pathway dei
PENTOSO-FOSFATI
Pathway di
ENTNER-DOUDOROFF
PIRUVATO
RESPIRAZIONE
AEROBICA
RESPIRAZIONE
ANAEROBICA
FERMENTAZIONE
Lattica, eterolattica
alcolica, acido mista
In condizioni anaerobiche
In alcuni batteri la via glicolitica è sostituita dalla via di
Entner-Doudoroff:
Gram Gram +
Pseudomonas
Enterococcus faecalis
Rhizobium
Azotobacter
Agrobacterium
alcuni Archaea
Svolge un ruolo simile alla via glicolitica:
conversione degli esosi in acido piruvico
inizia con le stesse reazioni della via dei pentosofosfati:
il 6-fosfogluconato viene DISIDRATATO
per formare KPDG
(2-cheto-3-deossi-6-fosfogluconato)
una ALDOLASI forma ACIDO PIRUVICO e
gliceraldeide 3-fosfato quest’ultima viene
trasformata in piruvato nella via glicolitica
DEGRADAZIONE DEL GLUCOSIO
ACIDO PIRUVICO
ACIDO PIRUVICO
IN CONDIZIONI
AEROBICHE
RESPIRAZIONE
AEROBICA
IN ANAEROBIOSI
FERMENTAZIONE
RESPIRAZIONE ANAEROBICA
RESPIRAZIONE AEROBICA DEI BATTERI CHEMIOETERTROFI
ACIDO
PIRUVICO
CICLO DI KREBS
(CICLO DEGLI ACIDI
TRICARBOSSILICI)
• OSSIDAZIONE COMPLETA DEL
PIRUVATO
• GENERAZIONE DI INTERMEDI UTILI
NELLE BIOSINTESI
GENERAZIONE DI POTERE RIDUCENTE
(NADH/FADH)
RIOSSIDAZIONE DEL NADH
ATTRAVERSO LA CATENA DI TRASPORTO
DEGLI ELETTRONI
SINTESI DI ATP
TRASPORTO
DEGLI ELETTRONI
FOSFORILAZIONE
OSSIDATIVA
BILANCIO GENERALE del CICLO
Il substrato organico viene completamente mineralizzato
3 molecole di CO2
3 molecole di NADH
1 molecola di NADPH
1 molecola di FADH
1 molecola GTP per fosforilazione
a livello del substrato
Decarbossilazione del
piruvato e formazione
dell’ACETIL-CoA
Si forma:
1 molecola di NADH
L’acetil-CoA si combina
con l’ossalacetato entrando
nel ciclo
Il NADH prodotto durante la glicolisi e il ciclo di Krebs deve essere riossidato
Rilascia quindi il suo potere riducente alla CATENA DI TRASPORTO DEGLI ELETTRONI
costituita da TRASPORTATORI di natura proteica o non proteica associati alla membrana
Diversi microrganismi hanno catene di trasporto degli elettroni differenti
FMN accettano atomi di H e
cedono elettroni
FERRO-ZOLFO PROTEINE
trasportano
solamente elettroni
CITOCROMI
CHINONI molecole
idrofobiche, non
contengono proteine
accettori di atomi di H e
donatori di elettroni
NADH deidrogenasi associata alla superficie interna della membrana
cellulare; accettano atomi di H dal NADH e li cedono alle
FLAVOPROTEINE
I trasportatori sono orientati nella membrana in modo che durante il trasporto avvenga una separazione degli e - e dei
protoni.
Gli atomi di idrogeno rimossi dal NADH vengono separati in elettroni e protoni:
1) Gli e- vengono trasferiti lungo la catena di trasporto fino ad un ACCETTORE FINALE – O2 che si riduce a H2O
2) I protoni vengono pompati fuori dalle cellule (o nel periplasma se si tratta di Gram-)
L’uso di H+ per la sintesi di H2O e l’estrusione dei protoni determina una separazione di cariche ai due lati della
membrana con la formazione di un gradiente di pH e di un potenziale elettrochimico
Lo stato “energizzato” della membrana costituisce la FORZA PROTON MOTRICE che può essere utilizzata per compiere un
lavoro utile (rotazione flagello), per trasportare ioni, per SINTETIZZARE ATP
alcuni aspetti sono comuni a tutte le catene di trasporto:
1)
presenza dei trasportatori di membrana disposti in modo crescente
verso un potenziale di riduzione più positivo
2)
un’alternanza fra trasportatori di soli elettroni e di soli atomi di
idrogeno
3)
la generazione di una forza proton-motrice come risultato della
separazione di cariche attraverso la membrana
COME FA LA FORZA PROTON-MOTRICE A
DETERMINARE LA SINTESI DI ATP?
TEORIA CHEMIOSMOTICA
Catalizzatore della forza proton-motrice in ATP:
ATP sintetasi (ATPasi)
H+
Due porzioni principali:
-testa F1 dominio catalitico
con subunità multiple
5 polipeptidi differenti a3, b 3, g,e, d
H+
H+
ESTERNO
-canale conduttore di protoni F0
3 polipeptidi differenti a, b2, c12
Il movimento del protone attraverso
la subunità a di F0 provoca la rotazione
delle proteine c
INTERNO
La torsione viene trasmessa alla testa
attraverso le subunità g,e, determinando
un cambiamento della conformazione delle
subunità b che diventano capaci di legare
ADP e Pi che viene convertito in ATP
quando la subunità b ritorna nella sua
conformazione originale
ADP + Pi
3 – 4 H+ 1 ATP
ATP
H+
H+
H+
RESA ENERGETICA DELLA OSSIDAZIONE AEROBICA
DI GLUCOSIO
VIA GLICOLITICA
Fosforilazione a livello del substrato (ATP)
Fosforilazione ossidativa con 2 NADH
(1 NADH 3ATP)
2ATP
6ATP
Acido piruvico ad AcetilCoA
Fosforilazione ossidativa con 2 NADH
(1 NADH 3ATP)
6ATP
CICLO DEGLI ACIDI TRICARBOSSILICI
Fosforilazione a livello del substrato (GTP)
Fosforilazione ossidativa con 6 NADH
Fosforilazione ossidativa con 2 FADH2
(1 FADH 2ATP)
1ATP
18ATP
4ATP
RESA AEROBICA TOTALE
38ATP
chemiotrofia
SOSTANZE
CHIMICHE
OSSIDAZIONE
SOSTANZE
ORGANICHE
OSSIDAZIONE
SOSTANZE
INORGANICHE
CHEMIOTROFI
composti chimici
come fonte di energia
CHEMIORGANOTROFI
(composti organici)
CHEMIOLITOTROFI
(composti inorganici)
FONTE DI C = sostanze organiche
CHEMIOETEROTROFI
FONTE DI C = CO2
CHEMIOAUTOTROFI
Alcuni sono eterotrofi facoltativi
RESPIRAZIONE
FERMENTAZIONE
RESPIRAZIONE
AEROBICA:
Accettore finale O2
ANAEROBICA:
Accettore finale
DIVERSO dall’ O2:
composto inorganico
ossidato
Non c’è un accettore
finale esterno.
L‘ossidazione è associata alla
riduzione di un composto
organico prodotto durante il
processo
IN ANAEROBIOSI
AEROBICA:
Accettore finale O2
IL GLUCOSIO E’ UN SUBSTRATO UNIVERSALE PER TUTTE
LE CELLULE ETEROTROFE
Qual è il destino del GLUCOSIO in una cellula batterica?
GLUCOSIO
GLICOLISI
(via di Embden-Meyerhof)
Pathway di
Pathway dei
ENTNER-DOUDOROFF
PENTOSO-FOSFATI
PIRUVATO
RESPIRAZIONE
AEROBICA
RESPIRAZIONE
ANAEROBICA
FERMENTAZIONE
Lattica, eterolattica
alcolica, acido mista
In condizioni anaerobiche
CHEMIOTROFI (utilizzano sostanze chimiche come donatori di e-):
sono conosciuti due meccanismi destinati alla conservazione dell’energia
FERMENTAZIONE
RESPIRAZIONE
SINTESI
DELL’ATP
Nella FERMENTAZIONE l’ossidazione è accoppiata alla riduzione di un
composto generato dal substrato iniziale;
ACCETTORE ORGANICO ENDOGENO DI ELETTRONI
Nella RESPIRAZIONE è presente l’ossigeno molecolare o un altro accettore
di elettroni come ACCETTORE TERMINALE;
FERMENTAZIONE
Processo metabolico anaerobico tipico dei microrganismi ANAEROBI OBBLIGATI
(Clostridium), oppure ANAEROBI FACOLTATIVI (E. coli) che svolgono la respirazione in
presenza di ossigeno e la fermentazione in assenza di ossigeno
Resa energetica inferiore a quella dei processi respiratori, per ricavare dal
substrato grandi quantità di ATP gli organismi ne usano grandi quantità
Il NAD+ e’ sempre ridotto a NADH e svolge il ruolo di trasportatore di elettroni
l’eccesso di NADH e’ un fattore limitante del processo fermentativo e
il pool di NAD+ viene rigenerato con la riduzione di una molecola organica
interna al processo
L’ATP è prodotta per fosforilazione a livello del substrato
RIOSSIDAZIONE DELL’ NADH
CATENA DI TRASPORTO DEGLI ELETTRONI
FERMENTAZIONE
processo catabolico anaerobio in cui un substrato
organico ridotto cede elettroni al NAD producendo ATP
mediante fosforilazione a livello del substrato
Il NADH così ottenuto si riossida riducendo un’altra
molecola organica, un intermedio dello stesso processo
metabolico
Possono essere fermentate numerose sostanze:
-Zuccheri (principalmente glucosio)
- Acidi organici ( es. acidi degli zuccheri, gluconato, malato, tartrato,ecc.)
-Aminoacidi
- Purine, pirimidine, ecc.
DESTINO DEL PIRUVATO:
formazione dei prodotti
di fermentazione
Riduzione del PIRUVATO
Ossidazione del NADH
Quasi sempre le varie vie
fermentative sono caratteristiche
di ben definiti gruppi
microbici, che dimostrano
un’elevata specificità di processo
FERMENTAZIONE ALCOLICA
- Lieviti (Saccharomyces cerevisiae) anaerobi facoltativi
- Batteri (Zymomonas mobilis)
CH3
C=O
COOH
PIRUVATO
CH3
PIRUVICO
DECARBOSSILASI
NADH + H+
NAD+
CH3
C=O + CO2
H
ALCOOL
DEIDROGENASI
ACETALDEIDE
CH2OH
ETANOLO
-Dal piruvato per decarbossilazione si ottiene acetaldeide
- Acetaldeide funge da accettore di elettroni riducendosi ad etanolo tramite
il NADH prodotto dalla glicolisi
FERMENTAZIONE OMOLATTICA:
Batteri lattici omofermentanti (o omolattici)
anaerobi obbligati o ossigeno tolleranti
appartenenti ai generi Gram+
Lactobacillus, Streptococcus, Pediococcus
Fibre muscolari in condizioni di sforzo
GLICOLISI acido piruvico, ATP, NADH
NADH + H+
NAD+
CH3
CH3
C=O
HCOH
COOH
PIRUVATO
LATTICO
DEIDROGENASI
COOH
LATTATO
In questa fermentazione è lo stesso acido piruvico di origine
glicolitica a fungere da accettore di e- per la riossidazione del
NADH, riducendosi così ad acido lattico
Non ci sono intermedi
FERMENTAZIONE
ETEROLATTICA
Tipica di alcuni batteri lattici eterofermentanti
Viene prodotto oltre all’acido lattico, anche
ETANOLO ed ANIDRIDE CARBONICA
Non fanno la glicolisi per degradare il glucosio
ma usano la via dei pentoso fosfati
FERMENTAZIONE ACIDO-MISTA
Enterobatteri Escherichia,Salmonella, Shigella e i
generi Proteus, Vibrio e Photobacterium sono
microrganismi Gram negativi anaerobi facoltativi
- in anaerobiosi fermentano il glucosio secondo
questa via.
Numerosi prodotti finali
Acidi organici a basso peso molecolare quali
acido formico (in E. coli e Proteus scisso in CO2 e
H2 dalla FORMICO IDROGENOLIASI la cui
presenza assume una rilevante importanza
tassonomica e diagnostica), acido acetico, acido
lattico e acido succinico e piccole quantità di
etanolo.
le proporzioni variano da microrganismo a
microrganismo e secondo le condizioni
colturali
FERMENTAZIONE BUTANDIOLICA
(Enterobacter, Serratia, Erwinia, alcune specie di Bacillus)
Oltre ai prodotti della acido-mista,
l’acido piruvico viene convertito ad
acetoino e poi ridotto, con l’utilizzo del NADH
a 2,3-butandiolo
Coloro che si occupano di analisi microbiologica
dell’acqua possono distinguere i coliformi fecali
(ferm. acidomista) dai non fecali (ferm. Butandiolica
tipica dei generi come Klebsiella) andando a svelare
la presenza di acetoino ed un pH più alto
I batteri appartenenti ai due diversi gruppi possono essere distinti sulla base di test che rilevano
l’acidità del mezzo di coltura e in base alla produzione di gas (CO2 e H2) oppure ricercando la
presenza di acetoino
Voges-Proskauer
terreno utilizzato
reagenti
procedimento
RMVP
a-naftolo
KOH 40%
Prelevare 1 ml di brodocoltura
0,2 ml di soluzione KOH 40%
0,6 ml di sol. a-naftolo
Dopo 15-20 minuti compare un anello
rosso cardinale
Reazione + anello rosso cardinale
Reazione - assenza di colore
“Phenol Red Fermentation medium”
contiene peptone, rosso fenolo (indicatore
pH) e il carboidrato da testare.
Il rosso fenolo è giallo a pH < 6.8 and
rosso a pH of > 7.4
Quindi se un batterio fermenta lo zucchero in
un acido si svilupperà un colore giallo.
Inoltre I tubi di crescita possono contenere
un tubo di Durham capovolto, se si sviluppa
gas durante la fermentazione si formerà una
bolla nel tubo capovolto
Nei batteri che fanno fermentazione
butandiolica si forma più CO2 che è
più solubile dell’H2 nel mezzo di coltura e non
forma bolle.
Non rilevabile con la provetta di Durham
Provetta di
Durham
FERMENTAZIONE PROPIONICA
Propionibacterium Gram+ microaerofili, catalasi +
isolati dall’Emmenthal, fermentano l’acido lattico
prodotto dai batteri lattici dando:
acido propionico, acido acetico e CO2
FERMENTAZIONE secondaria
FERMENTAZIONE BUTIRRICA
Si ritrova nei batteri del genere Clostridium,
sporigeno anaerobio obbligato
ossigeno-intollerante, in grado di fermentare
il glucosio.
Caratteristica di questa via è la produzione di
CO2 e H2 nella reazione del coenzima A
(CoASH) con il piruvato.
Il principale prodotto finale è l’acido butirrico
(acetone, butanolo, isopropanolo)
C. acetobutylicum
C. butylicum
C. butyricum
butanolo
acido butirrico
FERMENTAZIONE DEGLI AMINOACIDI
C. perfringens, C. botulinum, C. tetani sono in
grado di fermentare gli aminoacidi
Responsabili dei processi di putrefazione (decomposizione anaerobia delle proteine) con produzione di
H2S, acidi grassi e ammoniaca
RESPIRAZIONE ANAEROBICA
Accettore finale di elettroni è un composto
INORGANICO DIVERSO dall’OSSIGENO
Potenzialmente può essere usato qualunque OSSIDANTE INORGANICO
(NO3- nitrati, S elementare, SO42- solfati, ossidi ferrici, molecole organiche come
il fumarato che vengono trasformati nelle corrispondenti forme ridotte)
sistemi di trasporto di elettroni analoghi a quelli degli aerobi, i trasportatori
terminali sono specifici
in alcuni casi (batteri denitrificanti) il processo di respirazione anaerobica
affianca il processo di respirazione aerobica
Nel caso di E.coli l’accettore finale di elettroni può essere il nitrato o un
composto organico come il fumarato che viene ridotto a succinato
(da notare che a differenza del processo fermentativo, la molecola organica
che funge da accettori di elettroni è esterna alla via metabolica)
altri organismi che utilizzano la respirazione anaerobica sono ANAEROBI OBBLIGATI
CATENE DI TRASPORTO DI E. coli
IN AEROBIOSI
DIVERSI TRASPORTATORI TERMINALI
IN ANAEROBIOSI
Il passaggio di elettroni dal NADH all’accettore finale
attraverso i trasportatori genera gradiente protonico e
forza proton-motrice. La quantità di ATP prodotta
dipende dalla differenza di potenziale tre donatore e
accettore finale.
Tali composti hanno un potenziale
di riduzione più basso dell’ossigeno
Minore tendenza ad accettare elettroni
differenza di potenziale rispetto al
donatore primario inferiore
Tale processo libera meno energia
RESPIRAZIONE ANAEROBICA
MENO EFFICIENTE
Da 1 molecola di glucosio:
Resp. Aerobica (38ATP) >
Resp. Anaerobica (34 ATP) > Fermentazione (2 ATP)
*
RIDUZIONE di
NO3SO42-
NH2 gruppo amminico
SH gruppo sulfidrilico
CO2
Carbonio organico
FONTI DI N, S, C
METABOLISMO ASSIMILATIVO
Quando un composto inorganico
viene ridotto per essere utilizzato
come nutriente
(ASSIMILAZIONE)
COMUNE A MOLTI
ORGANISMI
ACCETTORI DI ELETTRONI
PER LA PRODUZIONE
DI ENERGIA
METABOLISMO DISSIMILATIVO
viene ridotta una quantità molto maggiore
del composto che viene utilizzato come
accettore di elettroni e il prodotto di
riduzione viene escreto dalla cellula
nell'ambiente esterno
TIPICO DI UN
RISTRETTO GRUPPO
DI PROCARIOTI
NITRATO come accettore finale di
elettroni – DENITRIFICAZIONE
Riduzione dissimilativa del NITRATO
Uno degli accettori di e- alternativi più
comuni è il nitrato NO3- che viene convertito
nelle forme più ridotte NO2- NO, N2O ed N2
I prodotti gassosi vengono facilmente
allontanati dall’ambiente per tale motivo
il processo viene chiamato
DENITRIFICAZIONE
Principale processo di
produzione di N2 per via
biologica
BATTERI CHE SVOLGONO
LA PRIMA PARTE DELLA RIDUZIONE
DEL NITRATO
Sono in grado di ridurre nitrato
NO3- a nitrito NO2-
- Escherichia
- Aeromonas
- Enterobacter
- Bacillus
- Staphylococcus…
BATTERI DENITRIFICANTI
Svolgono interamente la reazione
di riduzione fino ad N2
- Paracoccus
- Pseudomonas
- Utilizzano la denitrificazione in alternativa alla respirazione aerobica
- Anaerobi facoltativi
In presenza di O2 la sintesi della NITRATO REDUTTASI è repressa
MECCANISMI DI TRASPORTO DI ELETTRONI IN E. coli
in grado di compiere soltanto la prima parte del processo:
riduzione da nitrato a nitrito
O2
NO3-
NO3- + 2e- + 2H+
NO2-+ H2O
M
PERIPLASMA
INTERNO
MECCANISMO DI TRASPORTO
DEGLI ELETTRONI di Pseudomonas stutzeri
La riduzione dissimilativa del nitrato avviene
in diverse tappe fino ad azoto molecolare
NAR Nitrato reduttasi
NIR Nitrito reduttasi
NOR Ossido Nitrico Reduttasi
NOS Ossido Nitroso Reduttasi
MEMBRANA
CITOPLASMATICA
PERIPLASMA
SOLFATO come accettore finale di
elettroni
(Riduzione dissimilativa del solfato)
Diversi composti inorganici dello zolfo
possono fungere da accettori di elettroni nella
respirazione anaerobica
Il SOLFATO (SO42- ) è utilizzato dai
batteri solfato riduttori
RIDUZIONE ASSIMILATIVA e DISSIMILATIVA
Il solfato è un accettore di elettroni meno
favorevole dell’ossigeno e del nitrato
organismi con resa di crescita inferiore!
BATTERI SOLFATO-RIDUTTORI
Desulfovibrio
Desulfonema
Desulfosarcina
Desulfuromonas
- Batteri anaerobi obbligati diffusi sia in ambienti
acquatici che terrestri in cui si creano condizioni
anossiche per la presenza di materiale in
decomposizione (suoli e sedimenti anossici marini)
- Ampiamente diffusi in natura, tuttavia in alcuni
ambienti anossici la loro attività è limitata dai bassi
livelli di solfato presenti
- Si possono trovare anche nell’intestino degli animali e
dell’uomo (coinvolgimento nell’Inflammatory Bowel
Disease a causa dei solfuri prodotti)
-Essi utilizzano come donatore di elettroni soprattutto H2
lattato, piruvato;
-Le catene di trasporto non sono ben caratterizzate
- Sono note diverse specie sia da un punto
di vista morfologico che fisiologico
CATENE DI TRASPORTO
NON IDENTIFICATE
Lo ione solfato è molto stabile
ed è un cattivo accettore di eper poter essere ridotto deve
essere ATTIVATO
REDUTTASI TERMINALI
CITOPLASMATICHE
RIDUZIONE DISSIMILATIVA DEL
SOLFATO: richiede 8 elettroni
SO42- + 10H+ + 8e-
H2S + 4H2O
1
l’enzima ATP sulfurilasi catalizza
l’attacco del solfato ad un fosfato
dell’ATP formando l’ APS
(ADENOSINA FOSFO SOLFATO)
nel metabolismo dissimilativo.
2
Il gruppo solfato dell’APS viene
ridotto direttamente a solfito con
rilascio di AMP
AMP
+ SO32-
3
Il solfito poi viene
ulteriormente ridotto
dalla solfito riduttasi
RIDUZIONE ASSIMILATIVA
DEL SOLFATO
Nel metabolismo assimilativo l’enzima APS chinasi fosforila
l’APS formando il PAPS
(FOSFO-ADENOSINA FOSFOSOLFATO)
In entrambi i casi il primo prodotto è il solfito che poi
viene ulteriormente ridotto dalla solfito riduttasi
I MICRORGANISMI SONO IN GRADO DI
METABOLIZZARE DIVERSI COMPOSTI
CATABOLISMO DI CARBOIDRATI DIVERSI DAL GLUCOSIO
CATABOLISMO DEI LIPIDI
CATABOLISMO DI PROTEINE E AMMINOACIDI
CATABOLISMO DEI CARBOIDRATI DIVERSI DAL GLUCOSIO
INTERCONVERSIONE DEI MONOSACCARIDI
Il galattosio deve modificato a
glucosio-6-fosfato con un processo
a tre tappe
Altri zuccheri entrano facilmente
nella via glicolitica
DEMOLIZIONE DEI DISACCARIDI
I DISACCARIDI possono essere scissi negli zuccheri che li costituiscono
direttamente o mediante FOSFOROLISI (attacco del fosfato sul legame
che lega i due zuccheri)
I POLISACCARIDI vengono scissi grazie alla secrezione di enzimi specifici da parte di
alcuni batteri (Mixobatteri, Clostridi , Attinomiceti) e funghi
DEMOLIZIONE DEI DISACCARIDI
DEGRADAZIONE DI POLIMERI COMPLESSI
Presenti nella cellula come materiale di riserva o extracellulari
GLICOGENO, AMIDO, CELLULOSA, PECTINA, CHERATINA
All’interno della cellula…
FOSFOROLIASI
glucosio n + Pi
glucosio n-1 + glucosio-1-P
Acido poli-b-idrossibutirrico
L’enzima catalizza una reazione di
fosforolisi, accorciando la catena
di una unità e liberando glucosio-1-P
Acetil-CoA
CICLO TCA
All’esterno della cellula…
le macromolecole devono essere progressivamene frammentate per poter essere utilizzate
dai microrganismi enzimi diversi
AMIDO
AMILOSIO
a AMILASI
a 1,4-glicosidici
b AMILASI
AMILOPECTINA
a 1,6-glicosidici
a GLUCOSIDASI
PULLULANASI
a AMILASI
a GLUCOSIDASI
idrolizzano corti
oligosaccaridi liberando
a-glucosio
b AMILASI
Idrolizzano i legami
a 1,4-glicosidici esterni
producendo maltosio
PULLULANASI
Idrolizzano i legami
a 1,6-glicosidici interni
Idrolizzano i legami
a 1,4-glicosidici interni
CELLULOSA
polimero di unità di glucosio (100-10.000) unite tramite legami b 1,4 glicosidici
Batteri CELLULOSOLITICI sono in grado di idrolizzare la cellulosa
secondo diverse strategie:
- produzione extracellulare di un unico enzima degradativo
- produzione di più polipeptidi con domini cellulosolitici
- CELLULOSOMA
gli enzimi cellulosolitici sono:
- 1,4 b glucanasi he rompono i legami interni rilasciando cellobiosio e
oligosaccaridi
exo 1,4 b glucanasi che agiscono rilasciando cellobiosio dall’estremità
non riducente e attaccano i legami tre catene parallele
b glucosidasi che idrolizzano il cellobiosio a glucosio
CATABOLISMO DEI LIPIDI
TRIGLICERIDI
LIPASI
GLICEROLO
ACIGI GRASSI
DI-IDROSSIACETON
FOSFATO
VIA GLICOLITICA
ESTERI DEL coA
b-OSSIDAZIONE
CATABOLISMO DEGLI AMMINOACIDI
Alcuni batteri (patogeni, responsabili del deterioramento degli alimenti, batteri
del suolo) possono utilizzare le proteine come fonte di carbonio ed energia
TRANSAMMINAZIONE
Biorisanamento
Le proprietà metaboliche dei microrganismi sono sfruttate
per ripulire ambienti contaminati da:
Idrocarburi
Metalli pesanti
Sostanze Xenobiotiche
Radionuclidi
In che modo?