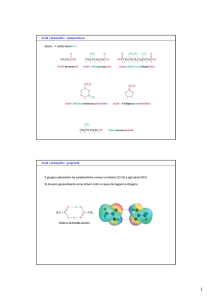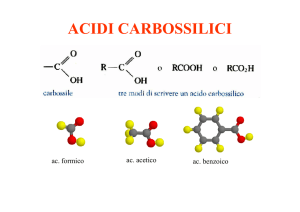
Reattività degli acidi carbossilici e derivati
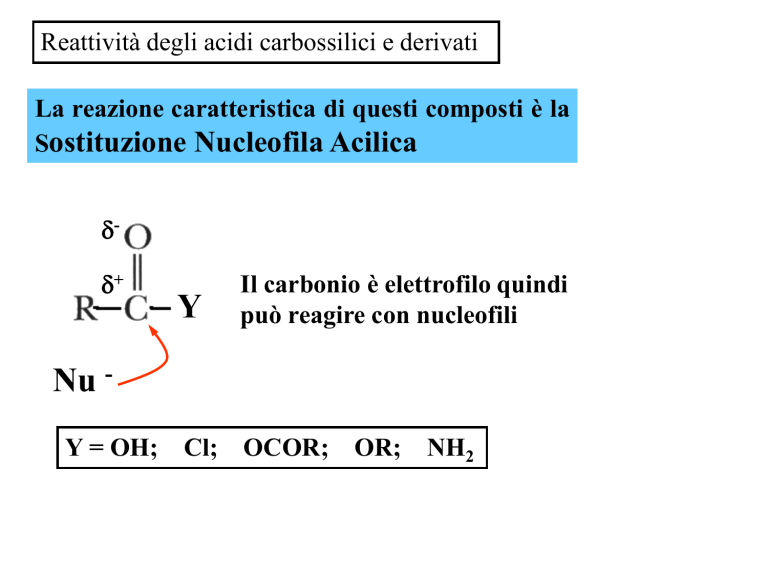
La reazione caratteristica di questi composti è la
Sostituzione Nucleofila Acilica
dd+
Y
Il carbonio è elettrofilo quindi
può reagire con nucleofili
Nu Y = OH; Cl;
OCOR; OR;
NH2
Mecanismo generale della Sostituzione Nucleofila Acilica
Stadio 1:
il nucleofilo si addiziona al carbonile
Stadio 2:
l’intermedio tetraedrico riforma il carbonile
ed espelle il gruppo uscente (eliminazione)
Nel complesso si ha una reazione di sostituzione
La forza del nucleofilo attaccante influenza la velocità del 1° stadio
La “bontà” del gruppo uscente (facilità della sua eliminazione)
determina la velocità del 2° stadio
Gruppo uscente
Capacità come gruppo uscente
Basicità crescente
La scala di reattività dei derivati degli ac. carbossilici sarà:
Reattività crescente
Perché aldeidi e chetoni danno l’addizione nucleofila al C=O
mentre i derivati degli acidi carbossilici danno la sostituzione
nucleofila al C=O ?
Addizione
Sostituzione
La differente reattività è dovuta al fatto che aldeidi e chetoni non
posseggono un buon gruppo uscente. Non possono eliminare un
carbanione o uno ione idruro (H-) che sono fortissime basi.
Una reazione degli acidi carbossilici: Esterificazione di Fischer
Etanoato di etile
(acetato di etile)
È una reazione catalizzata da acidi ed è
una Sostituzione Nucleofila Acilica
Meccanismo dell’esterificazione di Fischer
7
5
Esteri come aromatizzanti
Reazione con l’acqua: idrolisi dei derivati degli ac. carbossilici
Si riforma l’acido carbossilico
Cloruro di etanoile
Anidride acetica
Idrolisi degli esteri in ambiente acido
L’idrolisi di un estere in ambiente basico è detta saponificazione
Sale dell’ac. carbossilico
Meccanismo dell’idrolisi basica di un estere
Idrolisi di una ammide in ambiente acido
Le ammidi si idrolizzano più difficilmente di un estere (sia in
ambiente basico che acido). In genere si preferisce utilizzare una
idrolisi in ambiente acido.
2-fenilbutanammide
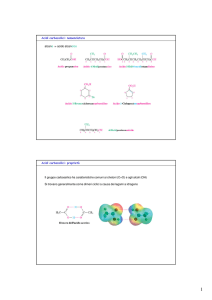
Reazioni con gli alcoli: Formazione di un estere
Cloruri degli acidi
Anidridi
L’Aspirina si ottiene da una esterificazione
Ac salicilico
Anidride
acetica
Acido acetilsalicilico
(Aspirina)
Reazione con l’ammoniaca ed ammine
Cloruri degli acidi
1
2
3
meccanismo
Reazione con l’ammoniaca ed ammine
Anidridi degli acidi
Esteri
Reattività decrescente
Reattività dei derivati degli acidi carbossilici ed interconversioni
Gli esteri reagiscono con i reattivi di Grignard
Sale
dell’alcol
Sale
dell’alcol
Alcoli
Meccanismo
1)
Sale
dell’alcol
2)
Riduzione degli esteri
Alcoli primari
1. LiAlH4
Riduzione delle ammidi
Ammine
Penicilline e Cefalosporine
Antibiotici con attività battericida
Le penicilline furono scoperte nel 1928 dal batteriologo scozzese A.
Fleming. Furono introdotte nella pratica medica nel 1943.
Penicillina G
(un antibiotico b-lattamico)
anello b-lattamico
Cefalosporina
(un antibiotico b-lattamico)