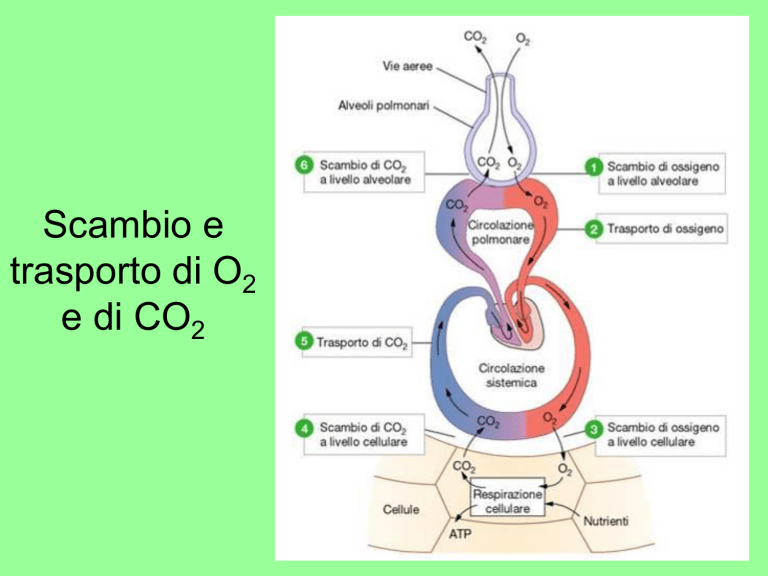
Scambio e
trasporto di O2
e di CO2
Leggi dei gas: legge di Boyle
• PV = nRT
• In cui P è la pressione del gas (Atm), V è il
volume che lo contiene (lt), n è il numero di
molecole del gas, R è la costante universale dei
gas, T è la temperatura assoluta
• Da cui:
• P = nRT/V
• Poiché, data una certa quantità di gas in un
contenitore, ad una certa temperatura n e T sono
costanti, la P sarà inversamente proporzionale al
V del contenitore, cioè:
• P = 1/V
Ciò è dovuto al fatto che le molecole di un gas sono in costante
agitazione termica e, sbattendo contro le pareti del contenitore,
esse esercitano su di esse una forza: la forza totale esercitata
dalla collisione di tutte le molecole sulle pareti darà la P del gas.
Quindi, se n è costante, ma il V diminuisce, aumenterà la densità
delle molecole e quindi il numero di collisioni e, di conseguenza,
la P. E viceversa.
Inoltre, se, a parità di V, aumenta n, di nuovo aumenterà il
numero di collisioni e quindi la P.
Leggi dei gas: Legge di Dalton
• La P esercitata da una miscela di gas è pari alla
somma delle pressioni esercitate dai singoli gas
che occupano lo stesso volume
• La pressione esercitata dai singoli gas di una
miscela viene chiamata pressione parziale di
quel gas
• Quindi la Ptot esercitata da una miscela di gas è
pari alla somma delle pressioni parziali
esercitate da ciascun gas che compone la
miscela:
• Ptot = P1 + P2 + P3 + P4 +….Pn
• Dove n è il numero di gas che costituisce la
miscela
Pressioni parziali dei gas nell’aria atmosferica
a 0°C e 760 mmHg (in condizioni di secchezza)
GAS
%
Patm
mmHg
Pgas
O2
20.95 di
760 =
159
PO2
CO2
0.04 di
760 =
0.3
PCO2
N2
79,01 di
760 =
596
PN2
Variando la temperatura ambiente e la percentuale di vapore acqueo si
avranno valori diversi delle P parziali
Pressioni parziali dei gas nell’aria alveolare
(satura di vapore acqueo e a 37°C)
A 37°C il vapore acqueo ha una P = 47mmHg, quindi se la P totale dei
gas negli alveoli è 760 mmHg, O2, CO2 e N2 eserciteranno una P = 760
- 47 = 713 mmHg.
Ma le percentuali dei tre gas nell’aria alveolare saranno diverse rispetto
a quelle dell’aria atmosferica perché il sangue attraversando i capillari
polmonari assume continuamente O2, diminuendone la concentrazione
negli alveoli e cede CO2 aumentandone la concentrazione negli alveoli.
Vale a dire che, nell’aria alveolare, le percentuali dei gas saranno
rispettivamente di circa 15% per l’O2, 5% per la CO2 e 80% per l’N2.
Quindi i valori delle P parziali dei gas saranno circa pari a:
PO2 = 100 mmHg
PCO2 = 40 mmHg
PN2 = 573 mmHg
Pressioni parziali nei liquidi
• I gas mantengono gran parte delle loro
caratteristiche molecolari quando si
trovano in soluzione
• Quindi anche nel sangue si possono
valutare le pressioni parziali dell’O2 e della
CO2 (N2 non partecipa agli scambi
respiratori)
• Se la pressione totale deve rimanere
costante, quando aumenta una pressione
parziale, l’altra deve ridursi
Leggi dei gas: Legge di Henry
• La solubilità di un gas in un liquido dipende dalla T, dalla P
parziale del gas nella miscela gassosa all’interfaccia con il
liquido, dalle proprietà chimiche del gas e dalle proprietà
chimiche del liquido. Quindi, a T = K
• c = KP
• In cui c = concentrazione del gas disciolto, P è la pressione
parziale del gas e K è la costante ad una data temperatura
• Quindi a T = K la concentrazione di un gas in un liquido è
proporzionale alla sua pressione parziale
• Inoltre, se un gas si trova sopra un liquido, tale gas si
scioglierà nel liquido finché non viene raggiunto l’equilibrio
• In condizioni di equilibrio, le concentrazioni del gas nell’aria
e nel liquido non saranno le stesse. Infatti, la concentrazione
del gas nel liquido dipende dalla solubilità specifica di quel
gas in quel particolare liquido: più è solubile, maggiore è la
concentrazione del gas nel liquido
• Quindi, quando aumenta la
pressione parziale del gas
aumenta anche la sua
concentrazione nel liquido
• Ma per gas diversi, a parità
di pressione parziale, la
concentrazione nel liquido
sarà diversa in base alla
diversa solubilità di ciascun
gas nel liquido
• Così, la concentrazione di
CO2 nel plasma, a parità di
pressione parziale, sarà
superiore a quella della O2,
perché superiore è la sua
solubilità
La diffusione semplice di una sostanza attraverso
una membrana obbedisce alla legge di Fick
Fattori che regolano la velocità di diffusione di O2 e
di CO2 tra polmoni e sangue e tra sangue e cellule
• La diffusione dei due gas attraverso le membrane obbedisce
alla legge di Fick
• Se si assume che la resistenza che offre la membrana alla
migrazione dei due gas sia = K, la diffusione dei polmoni sarà
direttamente proporzionale a:
– 1) Gradiente di concentrazione (pressione parziale)
– 2) Area della superficie di scambio
• e sarà inversamente proporzionale a:
– 3) Spessore della membrana
– 4) Distanza di diffusione (la diffusione è più rapida su brevi distanze)
• Poiché 2, 3 e 4 sono da considerarsi costanti, il fattore che più
influisce sugli scambi è il gradiente di concentrazione
Meccanismo degli scambi gassosi alveolari
• Gli scambi gassosi sono dovuti a gradienti di pressione parziale
dei singoli gas fra l’aria alveolare e il sangue
• I gas si spostano dal luogo dove hanno pressione maggiore a
quello dove la loro pressione è minore fino a raggiungere
l’equilibrio
• In particolare, nel polmone: l’O2 abbandona l’aria alveolare dove
ha una PO2 di 100 mmHg e passa nel sangue polmonare dove la
PO2 è di 40 mmHg; la CO2, invece, passa dal sangue polmonare,
dove ha una P di 46 mmHg all’aria alveolare, dove ha una P di
40 mmHg
• Viceversa, a livello tissutale: l’O2 abbandona il sangue dove ha
una PO2 di 100 mmHg e passa nelle cellule dove la PO2 è di 40
mmHg; la CO2, invece, passa dalle cellule dei tessuti, dove ha
una PCO2 di 46 mmHg, al sangue dove ha una PCO2 di 40 mmHg
Gradiente pressorio e solubilità
• Nel caso dell’O2 il gradiente pressorio necessario
perché avvengano gli scambi gassosi (sia a livello
polmonare, sia a livello tissutale) è di 60 mmHg
• Nel caso della CO2 il gradiente pressorio necessario
perché avvengano gli scambi gassosi (sia a livello
polmonare, sia a livello tissutale) è di soli 6 mmHg
• Ciò è dovuto al fatto che la solubilità della CO2 è 25
volte maggiore di quella dell’O2: pertanto lo scambio
gassoso sarà sempre più veloce per la CO2 che non
per l’O2 e quindi, per ottenere lo spostamento del gas,
sarà sufficiente un gradiente pressorio di pochi mmHg
Area della superficie di scambio
• La ramificazione sequenziale dell’albero
arterioso polmonare culmina con la
formazione di una densa rete di capillari
che avvolge gli alveoli
• Questa rete alveolo-capillare ha un’area di
superficie di circa 70 m2 (circa le
dimensioni di un campo da tennis)
Spessore della membrana e
distanza di diffusione
• Lo spessore della membrana è dato dalla
matrice e dalle componenti tissutali della rete
alveolo-capillare
• Questa barriera comprende:
le cellule epiteliali dell’alveolo di I tipo
le cellule endoteliali dei capillari
le loro rispettive membrane basali (che sono
a contatto tra loro)
• La distanza per lo scambio dei gas attraverso
questa barriera è di circa 1-2 μm
A = alveolo; c = capillare; col = collagene; el = elastina; e = endotelio capillare
con nucleo (nu); I = epitelio di I tipo; * = interstizio
Trasporto dei gas nel sangue
• Poiché i gas non sono molto solubili nel plasma, oltre al
loro dissolvimento, devono esistere dei sistemi di trasporto
più efficienti
• Infatti, ad es., a PO2 pari a 100 mmHg, il sangue contiene
solo 3 ml di O2 per litro. Poiché, a riposo, i tessuti
necessitano di 250 ml di O2/min, per sopperire alle
necessità tissutali, la gittata cardiaca dovrebbe essere di
circa 83 l/min anziché di 5 l/min come è in realtà
• Quindi è chiaro che esistono altri sistemi di trasporto dei
gas che garantiscono ai tessuti l’apporto necessario
• I meccanismi di trasporto devono essere reversibili, in
modo da consentire di legare l’O2 a livello polmonare e
rilasciarlo a livello tissutale, e viceversa per quanto
riguarda la CO2
Trasporto dell’ossigeno
• Ciascun litro di sangue arterioso contiene
circa 200 ml di ossigeno:
– 3 ml disciolti nel plasma o nel citosol degli
eritrociti (1,5%). Solo questo ossigeno
disciolto contribuisce alla PO2 sanguigna
– 197 ml (98,5%) trasportati legati
all’emoglobina, proteina che si trova negli
eritrociti
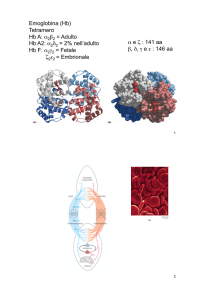
L’emoglobina
Cromoproteina costituita da 4 subunità proteiche, due α e due β. Ciascuna
subunità contiene una globina (catena polipeptidica globulare) fissata con
un legame covalente ad un gruppo eme (protoporfirina) che contiene Fe++
Concentrazione dell’emoglobina nel sangue
• Varia con l’età: nel neonato è pari a circa 20
g/100 ml di sangue, nell’adulto ha un valore di
circa 15 g/100 ml nel maschio e 14g/100 ml
nella femmina
• Si ha anemia quando la concentrazione di
emoglobina scende sotto i 13 g/100 ml nel
maschio e sotto i 12 g/100 ml nella femmina
• In alcune situazioni, come l’adattamento ad alta
quota, si può avere un aumento dei globuli rossi
(policitemia) e della concentrazione di
emoglobina per assicurare un adeguato apporto
di ossigeno ai tessuti anche in presenza di una
diminuita PO2
Emoglobina e ossigeno
• Ciascun gruppo eme della emoglobina è in grado di
legare una molecola di ossigeno
• Quindi ogni molecola di emoglobina può trasportare
fino a 4 molecole di ossigeno
• Ogni legame di una molecola di O2 con l’Hb
aumenta l’affinità dell’Hb per l’ O2 e quindi aumenta
la probabilità che altro O2 si leghi (cooperazione
positiva)
• Il complesso costituito da emoglobina e ossigeno è
detto ossiemoglobina (HbO2)
• Una molecola di emoglobina priva di ossigeno è
detta desossiemoglobina
Nei polmoni
• L’ossigeno si
sposta dall’aria
alveolare al
sangue capillare e
si lega
all’emoglobina
Nei tessuti
Quando il sangue
raggiunge i tessuti, le
molecole di ossigeno
si dissociano
dall’emoglobina e
diffondono alle
cellule
Reversibilità di legame
• Affinché l’emoglobina sia utile al trasporto
di ossigeno, è necessario che essa si leghi
all’ossigeno in maniera reversibile
• Il legame deve quindi essere
sufficientemente forte da poter legare
grandi quantità di ossigeno a livello
polmonare, ma non così forte da non
poterlo cedere ai tessuti
Il legame emoglobina-O2 dipende
dalla PO2
• Il legame o il rilascio di ossigeno dipende
dalla PO2 del sangue:
– un’elevata PO2 facilita il legame dell’O2 con
l’emoglobina
– una bassa PO2, ne facilita il distacco
Saturazione dell’emoglobina
Nel sangue arterioso la PO2 è di 100 mmHg e
l’emoglobina è saturata al 98,5%, cioè quasi tutti i
siti di legame sono occupati dall’O2. Pochissimo
ossigeno è disciolto nel citosol degli eritrociti
Saturazione dell’emoglobina
Nel sangue venoso misto la PO2 è di 40 mmHg e
l’emoglobina è saturata al 75%, cioè ogni 4 siti di
legame, 3 sono occupati dall’ossigeno
Curva di dissociazione dell’emoglobina
• A pressioni parziali basse,
poco O2 si lega all’Hb.
• All’aumentare della PO2 la
quantità di O2 che si lega
all’Hb prima aumenta
rapidamente, poi tende a
stabilizzarsi quando la
saturazione si avvicina al
100%.
• Come mostra la tabella,
alle normali pressioni
parziali nelle arterie e nelle
vene sistemiche, a riposo,
la percentuale di
saturazione dell’Hb varia
solo del 25% circa.
Variazioni dell’affinità dell’Hb per l’O2
• Esistono per lo meno altri quattro fattori (T, pH, 2,3-DPG,
PCO2) che possono influenzare l’affinità dell’Hb per l’O2
• Tali cambiamenti si riflettono in uno spostamento verso
destra o verso sinistra della curva di dissociazione dell’Hb
• Lo spostamento della curva verso destra indica una
diminuzione di affinità, cioè indica che l’O2 viene liberato
più facilmente dall’Hb, rendendolo disponibile ai tessuti
• Viceversa, uno spostamento della curva verso sinistra
indica che l’O2 viene caricato più facilmente dall’Hb per via
di una maggiore affinità
• Quindi, per uno spostamento verso destra è necessaria
una PO2 più alta di 45mmHg per ottenere una saturazione
dell’80%, per uno spostamento verso sinistra è sufficiente
una PO2 inferiore ai 45mmHg per determinare la stessa
percentuale di saturazione
Effetti della modificazione dell’affinità dell’Hb
per l’O2 sulla curva di dissociazione
Il legame emoglobina-O2 è influenzato
dalla Temperatura
La T influenza l’affinità dell’Hb per
l’O2 alterando la struttura dell’Hb
(come fa per la struttura terziaria di
tutte le proteine, quindi effetto non
specifico)
Poiché all’aumentare del
metabolismo la T aumenta,
diminuendo l’affinità dell’Hb per l’O2,
l’O2 viene rilasciato più facilmente ai
tessuti, soprattutto se molto attivi
Viceversa, la diminuzione della T del
sangue durante il passaggio nei
polmoni, promuove il legame tra Hb e
O2
Il legame emoglobina-O2 è influenzato
dal pH (effetto Bohr)
Quando la concentrazione
degli H+ aumenta, l’affinità
dell’Hb per l’O2 diminuisce,
viene rilasciato più O2 e la
curva si sposta verso destra
Ad es. nel corso del
metabolismo anaerobio delle
fibre muscolari si produce
acido lattico che rilascia H+
nel citoplasma e nel liquido
extracellulare con
abbassamento del pH
Il legame emoglobina-O2 è influenzato
dalla PCO2
Nel sangue pH e PCO2 sono
strettamente correlati: un
aumento della PCO2 si
accompagna ad una
diminuzione del pH (con
spostamento verso destra della
curva e diminuzione dell’affinità
per l’O2) e viceversa
Ma le modificazioni della curva
dovute ad una variazione della
PCO2, non sono totalmente
spiegabili sulla base della
variazione del pH perché esiste
anche un fattore specifico
regolato esclusivamente dalla
PCO2
Il legame emoglobina-O2 è influenzato
dal 2,3-DPG (2,3-difosfoglicerato)
• Il 2,3-DPG è prodotto dagli
eritrociti come prodotto
intermedio della glicolisi
• L’ossiemoglobina ad alte
concentrazioni inibisce l’enzima
che forma il 2,3-DPG e quindi i
livelli di 2,3-DPG sono bassi ed
hanno poco effetto sull’affinità
dell’Hb
Ma se i livelli di ossiemoglobina sono bassi (come quando i
rifornimenti di O2 sono ridotti), interviene la sintesi del 2,3-DPG
che diminuisce l’affinità dell’Hb per l’O2 favorendone il rilascio
nei tessuti che ne hanno bisogno (anemia, altitudine)
Il legame emoglobina-O2 e il monossido di C
Il monossido di carbonio
(gas inodore, incolore
prodotto nella combustione
incompleta dei materiali
organici) è tossico in quanto
si lega più velocemente
dell’O2 all’Hb formando
carbossiemoglobina
Esso impedisce il legame
dell’O2 con l’Hb e ne
diminuisce, di conseguenza,
la capacità di trasportare O2
del sangue
Il legame mioglobina-O2
• La mioglobina è il pigmento
rosso del muscolo che ha
una struttura simile a quella
di una delle catene di
emoglobina
• Possiede un solo gruppo
eme e può quindi legare una
sola molecola di ossigeno
La sua curva è spostata a sinistra rispetto a quella dell’Hb,
quindi: l’O2 ha una maggiore affinità per la mioglobina, viene
caricato più facilmente e ceduto ai tessuti con maggiore
difficoltà rispetto all’Hb
Trasporto della CO2
• Ciascun litro di sangue arterioso contiene
circa 490 ml di anidride carbonica:
– 27 ml disciolti nel plasma o nel citosol degli
eritrociti (5,5%).
– 24 ml (5%) trasportati legati all’emoglobina come
carbaminoemoglobina
– 439 ml (90%) disciolto nel sangue sotto forma di
bicarbonato. Il bicarbonato viene formato a
partire dalla CO2 negli eritrociti dei capillari
sistemici (dove i livelli di CO2 sono più alti) grazie
alla presenza dell’enzima anidrasi carbonica
L’anidrasi carbonica
Nell’eritrocita avviene la seguente reazione:
CO2 + H2O anidrasi carbonica H2CO3
H+ + HCO3-
Un aumento di CO2 (o di PCO2) sposta la reazione
verso destra (producendo più ioni idrogeno e
bicarbonato)
Una diminuzione della CO2 (o della PCO2) sposta la
reazione a sinistra, (producendo più anidride
carbonica a partire da ioni H+ e HCO3-)
Scambio della CO2 a livello tissutale
• Respirando, a riposo le cellule producono circa
200 ml/min di CO2 che diffonde nell’interstizio e
poi nel plasma, grazie al gradiente pressorio
• La CO2 nel plasma aumenta e quindi aumenta
la PCO2 che risulterà maggiore della PCO2 degli
eritrociti
• Quindi la CO2 diffonde dal plasma agli eritrociti
per gradiente pressorio e solo una piccola parte
resta disciolta
Negli eritrociti una parte si
lega all’emoglobina e la
maggior parte viene
trasformata in ioni
bicarbonato e idrogeno
grazie all’anidrasi carbonica
In tal modo la PCO2 del
plasma diminuisce in modo
da mantenere un gradiente
che consenta alla CO2 di
continuare a spostarsi dai
tessuti al plasma
Anche la CO2 negli eritrociti,
trasformata in ioni HCO3-,
diminuisce: quindi essa può
continuare a spostarsi dal
plasma agli eritrociti
• Se gli ioni H+ e HCO3- si accumulassero negli eritrociti,
la reazione tra anidride carbonica e acqua potrebbe
raggiungere un equilibrio
• In tal caso, la CO2 non verrebbe più convertita in ioni
idrogeno e bicarbonato e si accumulerebbe nelle
cellule in forma disciolta determinando un aumento
della PCO2 dentro gli eritrociti
• Il sangue, quindi, non potrebbe più trasportare CO2
sotto forma di bicarbonato
• Per impedire questo, è necessario che gli ioni
idrogeno e bicarbonato vengano rimossi dagli eritrociti
• Quando il livello degli ioni
bicarbonato negli eritrociti
aumenta, essi vengono
trasportati nel plasma e
scambiati con gli ioni Cl
grazie ad una proteina di
trasporto che si trova nella
membrana plasmatica
degli eritrociti (scambio dei
cloruri)
• Gli ioni idrogeno vengono
tamponati
dall’emoglobina, con
formazione di emoglobina
ridotta (HHb)
• Il legame degli idrogenioni
all’Hb è alla base dello
spostamento a destra
della curva di saturazione
dell’Hb con cessione di O2
ai tessuti da parte dell’Hb
Riassumendo:
Carbaminoemoglobina
(piccola quantità)
Scambio della CO2 a livello polmonare
A livello alveolare, la CO2 passa dal plasma agli alveoli, per gradiente di
concentrazione, per essere espirata
La perdita di CO2 fa sì che gli ioni HCO3- ed H+ negli eritrociti, si ricombinino
ad H2CO3 che, per effetto dell’anidrasi carbonica, viene riconvertito in H2O e
CO2 che diffonde negli alveoli per essere espirata
Man mano che gli ioni HCO3- degli eritrociti vengono utilizzati, i loro livelli
dentro gli eritrociti diminuiscono e nuovi ioni HCO3- entrano dal plasma in
scambio con il ClLa CO2 che diffonde negli alveoli per essere espirata, favorisce la formazione
di altra CO2
Riassumendo:
Curva di saturazione della CO2
• Così come la PCO2 del
sangue influenza l’affinità
dell’Hb per l’O2, anche la PO2
influenza l’affinità dell’Hb per
la CO2
• In particolare, un aumento
della PO2 determina uno
spostamento a destra della
curva, diminuendo l’affinità
dell’Hb per la CO2 e quindi la
sua capacità di trasportare
CO2 (effetto Haldane)
La diminuita affinità dell’Hb per la CO2 (effetto Haldane) è dovuta
al fatto che, quando la PO2 aumenta, l’Hb trasporta più O2 e si
riduce la quantità di CO2 che può legarsi all’Hb
Riassunto del trasporto dei gas
Nei tessuti
Nei polmoni