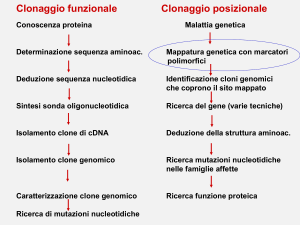
Clonaggio funzionale
Conoscenza proteina
Clonaggio posizionale
Malattia genetica
Determinazione sequenza aminoac.
Mappatura genetica con marcatori
polimorfici
Deduzione sequenza nucleotidica
Identificazione cloni genomici
che coprono il sito mappato
Sintesi sonda oligonucleotidica
Ricerca del gene (varie tecniche)
Isolamento clone di cDNA
Deduzione della struttura aminoac.
Isolamento clone genomico
Ricerca mutazioni nucleotidiche
nelle famiglie affette
Caratterizzazione clone genomico
Ricerca di mutazioni nucleotidiche
Ricerca funzione proteica
Clonaggio funzionale
L’identificazione del gene e della sua posizione nel
genoma avviene a partire dalla conoscenza della proteina
Se la proteina è nota si frammenta in peptidi e si
determina la struttura amminoacidica
Dalla sequenza amminoacidica si deduce la possibile
sequenza codificante, considerando la degenerazione del
codice
Esempio di clonaggio funzionale del gene per il fattore VIII
della coagulazione
Sonde degenerate corrispondenti a una porzione di sequenza amminoacidica del
fattore VIII.
Ibridazione con cloni di una libreria di cDNA ; il clone di cDNA isolato si usa come
sonda per individuare un clone in una libreria di DNA genomico
Clonaggio funzionale
Conoscenza proteina
Clonaggio posizionale
Malattia genetica
Determinazione sequenza aminoac.
Mappatura genetica con marcatori
polimorfici
Deduzione sequenza nucleotidica
Identificazione cloni genomici
che coprono il sito mappato
Sintesi sonda oligonucleotidica
Ricerca del gene (varie tecniche)
Isolamento clone di cDNA
Deduzione della struttura aminoac.
Isolamento clone genomico
Ricerca mutazioni nucleotidiche
nelle famiglie affette
Caratterizzazione clone genomico
Ricerca di mutazioni nucleotidiche
Ricerca funzione proteica
MARCATORI GENETICI
Un marcatore genetico è paragonabile ad un cartellino
colorato che serve a “marcare” i cromosomi degli individui in
un pedigree.
Un marcatore genetico per essere tale deve essere polimorfico
ed i suoi diversi alleli possono essere utilizzati per seguire la
segregazione di alleli per un altro gene quando si effettuano
incroci.
MARCATORI GENETICI
Caratteristiche:
- Trasmissione mendeliana
- Neutralità
- Elevato livello di polimorfismo
- Tipizzazione facile ed economica
- Posizione nota nel genoma
TIPI DI MARCATORI POLIMORFICI
- Polimorfismi immunologici (es: gruppi sanguigni, rilevabili con
tecniche sierologiche)
- Polimorfismi genetici a livello proteico (rilevabili attraverso
l’elettroforesi ed altre tecniche di caratterizzazione degli isozimi)
- Polimorfismi genetici a livello del DNA
VARIABILITA’ GENETICA SEMPLICE
POLIMORFISMO: presenza di 2 o più fenotipi alternativi
(morfi) a trasmissione mendeliana
MORFI: generalmente determinati da alleli diversi ereditati
in modo mendeliano
POLIMORFISMO GENETICO
Carattere monogenico presente in una popolazione con
una frequenza 1%
f(A) = p
f(B) = q
ETEROZIGOSITA’ (H)
H = 2pq
H aumenta in relazione al numero di alleli del locus
TIPI DI MARCATORI GENETICI NELL’UOMO
Tipo di marcatore
n° loci
Caratteristiche
Gruppi sanguigni
1910-1960
20
sangue fresco, dominanza
Varianti proteiche
1960-1975
30
siero fresco, saggi specialistici,
polimorfismo limitato
RFLP del DNA
1975-
>105
2 alleli, eterozigosità massima 0,5
VNTR del DNA
(minisatelliti)
1985-
>104
Molti alleli, altamente informativi
VNTR del DNA
(microsatelliti)
1989-
>105
Molti alleli, altamente informativi
SNP del DNA
1998-
>106
Meno informativi dei microsatelliti
LIVELLO DI POLIMORFISMO
- Eterozigosità
- Contenuto d’informazione del polimorfismo (Polymorphism
Information Content = PIC)
TASSO DI MUTAZIONE
Singola Sostituzione Nucleotidica (SNS): 10-9
Variable Number of Tandem Repeat (VNTR): minisatelliti 10-2 - 10-3
microsatelliti 10-3 - 10-4
Il genoma è un serbatoio potenziale di polimorfismi così vasto da
consentire di individuare i marcatori più adatti per affrontare un
ampio spettro di problematiche della genetica delle popolazioni
umane.
MAPPAGGIO GENETICO DEI CARATTERI MENDELIANI
1
2
Analisi della segregazione degli alleli per il locus A e degli alleli del locus B
Dalle meiosi di II-1 è possibile stabilire: 5 combinazioni parentali e
2 ricombinanti
Dopo quante meiosi si può stabilire se i loci A e B sono associati o
indipendenti?
LA MAPPATURA GENETICA PRIMA DEI MARCATORI
MOLECOLARI DEL DNA
Gruppi di associazione tra loci (marcatori proteici) noti
e loci responsabili di malattie:
ABO - adenilatochinasi
ABO - sindrome unghia- rotula
Duffy - cataratta congenita
Rh - ellissocitosi
Collinesterasi - transferrina
Lutheran - secretore
G6PD - emofilia
G6PD - daltonismo
c daltonico
*
enzimopenico
Locus Daltonismo: D = allele normale;
d = allele daltonismo
Locus gene G6PD: A2 = allele normale;
A1 = allele enzimopenia G6PD
A3 Y
A1 /A2
D
c
D/d
*
A2 Y A1 Y
d
D
A2 Y
d
MEIOSI INFORMATIVE E NON INFORMATIVE
A) NON INFORMATIVA
A1 A1
A2 A2
Gli alleli del marcatore in omozigosi
nel padre non possono essere
distinti
A1 A2
B) NON INFORMATIVA
A1 A2
A1 A2
A1 A2
La figlia può aver ereditato A1 dal
padre e A2 dalla madre o viceversa
MEIOSI INFORMATIVE E NON INFORMATIVE
C) INFORMATIVA
A1 A2
A1 A2
La figlia ha ereditato A1 dal padre
(fratria A1 A1 alternativa a A1 A2 della
famiglia B)
A1 A1
D) INFORMATIVA
La figlia ha ereditato A1 dal padre
A1 A2
A3 A4
A1 A4
UNA MEIOSI E’ INFORMATIVA, OVVERO UTILE PER GLI STUDI DI
ASSOCIAZIONE (LINKAGE), QUANDO SI PUO’ IDENTIFICARE LA
FASE DEI 2 LOCI E QUINDI STABILIRE SE IL GAMETE E’ O MENO
RICOMBINANTE
PERCHE’ LA MEIOSI SIA INFORMATIVA IL GENITORE DEVE
ESSERE DOPPIO ETEROZIGOTE PER I DUE LOCI
Es: genotipo locus malattia:
Allele normale (+)/ Allele mutato (-)
genotipo locus marcatore: A1/A2
+/A1/A2
Marcatore
Alleli (Frequenze
alleliche)
H
PIC
A
1
0
0
A
2 (0,5; 0,5)
0,50
0,375
A
2 (0,4; 0,6)
0,48
0,365
A
2 (0,3; 0,7)
0,42
0,332
A
2 (0,1; 0,9)
0,18
0,164
A
4 (0,25;0,25;0,25; 0,25)
0,75
0,703
A
10 (tutti = 0,1)
0,90
0,891
X
2 (0,5; 0,5)
0,5
0,5
X
4 (0,25;0,25;0,25; 0,25)
0,75
0,75
MAPPATURA GENETICA A DUE PUNTI
1) Raccolta famiglie con diagnosi certa di una specifica
malattia il cui locus genico è ignoto
2) Costruzione degli alberi genealogici di tutte le famiglie
3) Determinazione del genotipo di tutti gli individui per uno
o più marcatori polimorfici
4) Se la famiglia è informativa, si classificano gli individui
in ricombinanti o non ricombinanti tra il locus della
malattia ed il marcatore analizzato
………
MAPPAGGIO GENETICO DEI CARATTERI MENDELIANI
1
2
Dalle meiosi paterne: i loci A e B sono indipendenti o associati?
Non si possono classificare II-2 e tutti gli individui della III generazione
rispetto a II-2 (omozigote A1A1B1B1)
Sacchetto con monete di tre possibili tipi: TT (monete con T su
entrambe le facce), oppure TC, oppure CC
4 lanci: T, T, T, T
E’ possibile capire da che tipo di monete è fatto il sacchetto?
Ipotesi che siano CC = Scartata
Ipotesi possibili: A: che siano TT
B: che siano TC
Se non si fossero fatti lanci
Ipotesi A: Ipotesi B 1:1
Si intende per VEROSIMIGLIANZA di un’ipotesi A, rispetto ad una
serie di fatti che costituiscono il risultato R, la probabilità con cui
si sarebbe verificato R se A fosse stata vera.
Si confrontano le VEROSIMIGLIANZE di tutte le ipotesi per
accertare se una è risultata MOLTO PIU’ VEROSIMILE delle
altre
Verosimiglianza dell’Ipotesi A = 1 (che siano TT)
Verosimiglianza dell’ipotesi B = (1/2)4 = 1/16
1
Rapporto -------- = 16 :1
1/16
Quanti lanci bisogna fare prima di assumere che siano TT?
Si decide una soglia per 2 motivi:
1) ridurre al minimo i casi in cui si accetta per buona
un’ipotesi che invece è sbagliata;
2) ridurre al minimo i casi in cui si lascia senza risposta il
problema in esame
UN ESEMPIO DI CALCOLO DI LOD SCORE
Caso in cui
II 1 ha fase nota
NR
NR
NR
NR
NR
R
R
R
R
R
R
R
Probabilità di meiosi ricombinante =
Probabilità di meiosi non ricombinante = (1- )
Probabilità 5 NR e 1R = (1- )5 x 1
Probabilità totale in assenza di associazione = (0,5)6 = (1/2)6
Rapporto della verosimiglianza = (1-)5 x 1 / (1/2)6
Calcolo del log10 degli ODD
(1-)5 x 1
Lod score Z = log10 --------------------(1/2)6
Odd
Z
0
0
-
0,1
3,779
0,577
0,2
4,287
0,623
0,3
4,194
0,509
0,4
0,5
1,991
0
0,299
0
LE CURVE DEI LOD SCORE
Z = lod score
1000
Z = log 10 -------- = 3
(p=0,05)
1
Z > 3 EVIDENZA DI LINKAGE
1
Z = log 10 -------- = - 2
100
Z < - 2 ESCLUSIONE DI LINKAGE
3 > Z > - 2 NON CONCLUSIVI PER
IL LINKAGE
SENZA RICOMBINANTI MASSIMO
DI LOD SCORE E’ PER = 0
INTERVALLO DI CONFIDENZA (95%):
LOD SCORE - 1
es. curva 2 max lod score = 3.7
per = 0.23 limiti fiduciali: 0.17 - 0.32
COME SI OTTENGONO I VALORI DEL LOD SCORE
Per ogni famiglia si calcola:
- la verosimiglianza ‘a posteriori’ (sulla base del risultato osservato
nelle meiosi) per una serie di ipotesi di associazione (linkage), cioè di
valori di ricombinazione
- il valore che si ottiene per ciascun dell’ODD ratio (= verosimiglianza
dell’ipotesi / verosimiglianza dell’ipotesi di indipendenza)
- il Logaritmo degli ODD (= LOD)
- i calcola il Lod score complessivo sommando quello di ogni singola
famiglia per ogni
- si costruisce il grafico dei Lod score e si individua il valore di per cui
la verosimiglianza è massima
(1-)5 x 1
Lod score Z = log10 --------------------(1/2)6
0.7
0.6
0.5
0.4
0.3
0.2
0
Z
-
0.1
0
0
0.2
0.4
0.6
0,1
0,2
0,3
0,4
0,577
0,623
0,509
0,299
0,5
0
(1-)5 x 1
(1-) 1 x 5
Z = log10 --------------------- + --------------------(1/2)6
(1/2)6
NR
R
NR
R
NR
R
NR
R
NR
R
R
NR
0.35
0.3
0.25
0.2
0.15
0.1
0.05
0
0
0.1
0.2
0.3
0.4
0.5
0.6
0
Z
-
0,1
0,2
0,3
0,4
0,276
0,323
0,222
0,074
0,5
0
MAPPATURA GENETICA A DUE PUNTI
1) Raccolta famiglie con diagnosi certa di una specifica
malattia il cui locus genico è ignoto
2) Costruzione degli alberi genealogici di tutte le famiglie
3) Determinazione del genotipo di tutti gli individui per uno
o più marcatori polimorfici
4) Se la famiglia è informativa, si classificano gli individui
in ricombinanti o non ricombinanti tra il locus della
malattia ed il marcatore analizzato
………
MAPPATURA GENETICA A DUE PUNTI
......
5) Nel caso di meiosi non informative non è possibile stabilire
con certezza gli individui ricombinanti e non ricombinanti e
quindi se i due loci sono associati
6) Estensione della tipizzazione a più famiglie
Come si stabilisce se i due loci sono associati?
7) Analisi dell’associazione tra il marcatore ed il locus attraverso
il calcolo del lod score per ogni singola famiglia
8) Valutazione del lod score complessivo e utilizzazione del
criterio statistico per decidere l’associazione o l’esclusione di
associazione
STIMA DELLA DISTANZA GENETICA TRA MARCATORI
1
2
Rispetto alla combinazione parentale (II-1): 5 NR, 2 R
Frequenza di ricombinazione = 2/7 = 28,6%
IL LINKAGE A DUE O PIU’ PUNTI E’ ESSENZIALE PER LA
COSTRUZIONE DELLE MAPPE MARCATORE - MARCATORE
QUESTO E’ STATO OTTENUTO CON:
- COLLEZIONE DI FAMIGLIE CON STRUTTURA IDEALE RACCOLTE A
QUESTO SCOPO DAL CEPH DI PARIGI (CENTRE POUR L’ETUDE DES
POLYMORPHISMES HUMAINES): 40 famiglie con 3 generazioni e almeno
6 figli)
- ANALISI DI MARCATORI POLIMORFICI (SOPRATTUTTO
MICROSATELLITI) LOCALIZZATI SU TUTTI I CROMOSOMI IN FAMIGLIE
CEPH (1998: mappati 8325 loci microsatelliti) ED ISTITUZIONE DI UNA
BANCA DATI
- DETERMINAZIONE DELL’ORDINE DEI LOCI NELLE MAPPE
MARCATORE – MARCATORE E DEFINIZIONE DELLE DISTANZE IN
CENTIMORGAN
ESEMPIO DI FAMIGLIA CEPH
Famiglia 12
10
11
12
1
3
4
13
2
5
6
7
8
9
IL PROGETTO GENOMA UMANO
PER LA MAPPATURA DEL GENOMA UMANO SONO STATI UTILIZZATI
NUMEROSISSIMI MARCATORI POLIMORFICI (RFLP E VNTR), NON
NECESSARIAMENTE CORRELATI A GENI ESPRESSI, CON
MODALITA’ DI TRASMISSIONE MENDELIANA
Utilizzi:
1) Mappatura genetica di loci sconosciuti responsabili di malattie
genetiche;
2) Clonaggio genico;
3) Diagnosi prenatale e presintomatica.
23 GRUPPI DI ASSOCIAZIONE (22 AUTOSOMI E CROMOSOMA X)
STIMA DELLA DISTANZA GENETICA TRA MARCATORI
NEL CROMOSOMA 12
% Ricombinazione
3
5
2
Analisi della segregazione degli alleli
nelle famiglie CEPH.
Lod score a due o più punti per stabilire
associazione tra marcatori e stimare la
distanza genetica in percentuali di
ricombinazione che equivalgono ai cM.
1% ricombinazione = 1 unità di mappa
= 1 centiMorgan (cM)
Totale % ricombinazione convertito in 133 cM e quindi in Mb
STIMA DELLA RELAZIONE TRA DISTANZA
GENETICA E FISICA
Stima della distanza genetica totale nella specie umana:
somma della lunghezza totale dei cromosomi ottenuta dalla
mappatura genetica attraverso meiosi di origine paterna o
materna
= 2644 cM (maschio)
= 4481 cM (femmina)
Per 3000 Mb = 3 x 109 bp di genoma
Maschio
1 cM = 1.13 Mb = 1.13 x 106 bp
Femmina
1 cM = 0.67 Mb = 0.67 x 106 bp
Media : 1 cM = 0.9 Mb = 0.9 x 106 bp
Il tasso di ricombinazione non è identico lungo il cromosoma
La distribuzione dei ricombinanti lungo il cromosoma non è
casuale e dipende dal sesso
Distribuzione dei
chiasmi negli
spermatociti (blu)
e negli oociti
(rosso)
Mappatura
genetica
Mappatura
Mappatura
fisica bassa fisica alta
risoluzione risoluzione
Mappatura
del trascritto
Sequenziamento
del gene
Esempio di analisi di associazione tra marker M e malattia AD
Stima della frequenza di ricombinazione = 2/6 = 0,33
Associazione (linkage) tra il locus marcatore A e locus ignoto di una
Malattia Autosomica Dominante in 3 famiglie con la stessa patologia
A1
D
A2
A2
d
d
A3
d
A3
D
A2
A2
d
A3
d
d
A1
A2
A2
A3
A1
A3
A3
A2
D
d
d
d
D
d
D
d
A2
D
A4
d
A3
A3
D
d
A2
A3
d
d
A2
A3
d
d
L’associazione è tra loci !
A2
A2
A4
A3
A2
A3
A4
A2
D
d
d
d
D
d
d
d
MALATTIE PER LE QUALI E’ STATO IDENTIFICATO IL GENE
CAUSATIVO TRAMITE CLONAGGIO POSIZIONALE
Corea di Huntington
Fibrosi cistica
Distrofia Muscolare di Duchenne
Acondroplasia
Tumore del seno (BRCA1, BRCA2)
Malattia del rene policistico
Atassia spinocerebellare di tipo I, etc
Distrofia miotonica
Poliposi familiare del colon
ESEMPIO DI CLONAGGIO POSIZIONALE:
L’INDIVIDUAZIONE DEL GENE BRCA1
Frequenza tumore al seno in
Inghilterra: 1 su 12 donne
Casi familiari per mutazione
BCRA1
1994: clonaggio di BRCA1. Gene
responsabile dell’80-90% dei casi di
famiglie affette sia da tumore
mammario che alle ovaie.
Tumor suppressor gene, mutato
anche in altri tipi di cancro
1995: clonaggio di BRCA2.
Frequente anche nei casi di tumore
mammario nei maschi
Comunque solo il 20-25% dei tumori
mammari familiari dovuti a questi 2
geni: altri geni con effetto modesto?
(eredità poligenica)
Distribuzione di marcatori associati sul cromosoma 1 e distanza in cM