Il ciclo di Krebs, o ciclo degli acidi carbossilici, è una via metabolica centrale negli eucarioti che prende posto all'interno dei mitocondri. In tale
processo si assiste alla fase centrale della degradazione degli zuccheri, dei grassi, delle proteine per fornire, sotto forma di composti
eterogenei, energia. Il ciclo di Krebs, inoltre, è un ciclo anfibolitico poichè gli intermedi di catalisi servono per la sintesi di costituenti essenziali
della vita biologica.
Le tappe del ciclo di Krebs.
Il ciclo di Krebs è regolato da dieci tappe nelle quali si assistono a diversi tipi di reazioni. Ogni tappa è mediata da almeno un enzima.
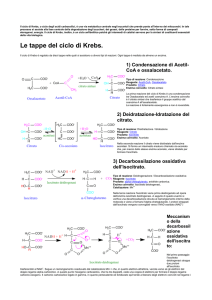
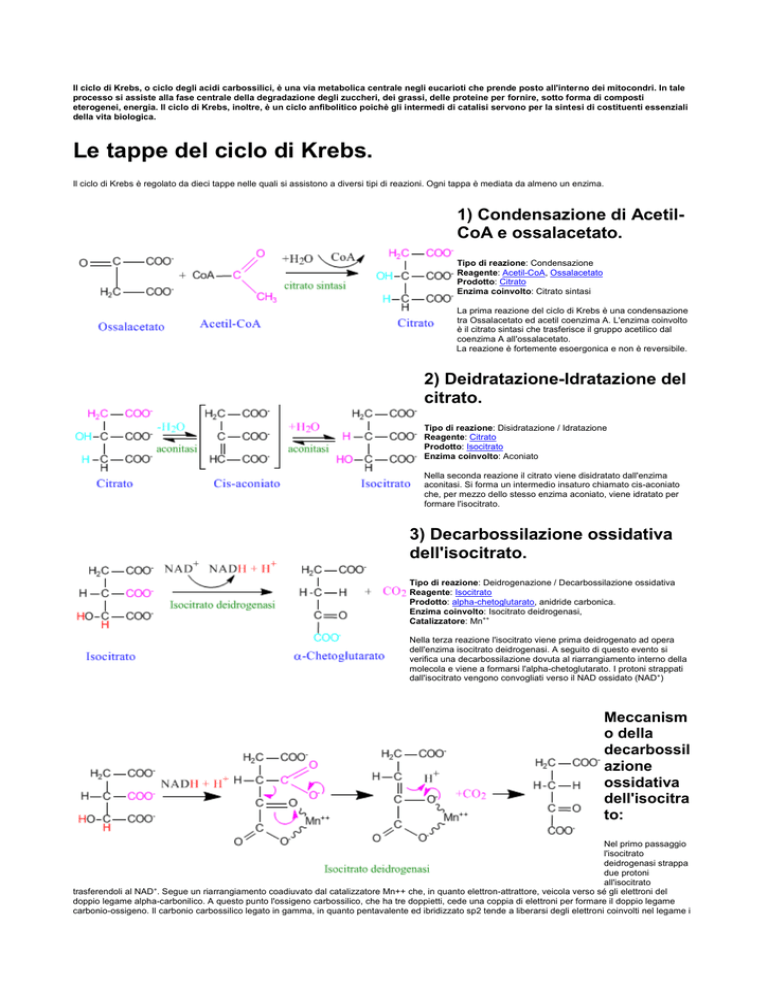
1) Condensazione di AcetilCoA e ossalacetato.
Tipo di reazione: Condensazione
Reagente: Acetil-CoA, Ossalacetato
Prodotto: Citrato
Enzima coinvolto: Citrato sintasi
La prima reazione del ciclo di Krebs è una condensazione
tra Ossalacetato ed acetil coenzima A. L'enzima coinvolto
è il citrato sintasi che trasferisce il gruppo acetilico dal
coenzima A all'ossalacetato.
La reazione è fortemente esoergonica e non è reversibile.
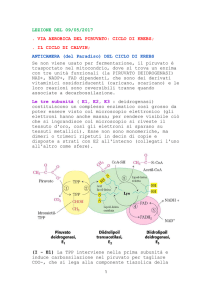
2) Deidratazione-Idratazione del
citrato.
Tipo di reazione: Disidratazione / Idratazione
Reagente: Citrato
Prodotto: Isocitrato
Enzima coinvolto: Aconiato
Nella seconda reazione il citrato viene disidratato dall'enzima
aconitasi. Si forma un intermedio insaturo chiamato cis-aconiato
che, per mezzo dello stesso enzima aconiato, viene idratato per
formare l'isocitrato.
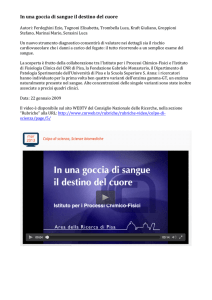
3) Decarbossilazione ossidativa
dell'isocitrato.
Tipo di reazione: Deidrogenazione / Decarbossilazione ossidativa
Reagente: Isocitrato
Prodotto: alpha-chetoglutarato, anidride carbonica.
Enzima coinvolto: Isocitrato deidrogenasi,
Catalizzatore: Mn++
Nella terza reazione l'isocitrato viene prima deidrogenato ad opera
dell'enzima isocitrato deidrogenasi. A seguito di questo evento si
verifica una decarbossilazione dovuta al riarrangiamento interno della
molecola e viene a formarsi l'alpha-chetoglutarato. I protoni strappati
dall'isocitrato vengono convogliati verso il NAD ossidato (NAD+)
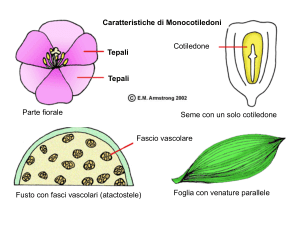
Meccanism
o della
decarbossil
azione
ossidativa
dell'isocitra
to:
Nel primo passaggio
l'isocitrato
deidrogenasi strappa
due protoni
all'isocitrato
+
trasferendoli al NAD . Segue un riarrangiamento coadiuvato dal catalizzatore Mn++ che, in quanto elettron-attrattore, veicola verso sé gli elettroni del
doppio legame alpha-carbonilico. A questo punto l'ossigeno carbossilico, che ha tre doppietti, cede una coppia di elettroni per formare il doppio legame
carbonio-ossigeno. Il carbonio carbossilico legato in gamma, in quanto pentavalente ed ibridizzato sp2 tende a liberarsi degli elettroni coinvolti nel legame i
quali si localizzano tra i carboni alpha e beta. A questo punto si forma un doppio legame tra carbonio alpha e beta che attrae un protone, fortissimo
elettrofilo, per formare un legame covalente con il carbonio gamma. La molecola così formata e stabile e prende il nome di alpha-chetoglutarato.
4) Decarbossilazione ossidativa
dell'alpha-chetoglutarato.
Tipo di reazione: Deidrogenazione / Decarbossilazione ossidativa
Reagente: Alpha-chetoglutarato, Coenzima A
Prodotto: Succinil-CoA, anidride carbonica, NADH
Enzima coinvolto: Complesso di deidrogenasi dell'alphachetoglutarato
Nella quarta reazione avviene una decarbossilazione ossidativa
preceduta da una deidrogenazione dell'alpha-chetoglutarato
operata dal complesso di deidrogenasi dell'alpha-chetoglutarato.
Contemporaneamente alla decarbossilazione una molecola di
Coenzima A viene addizionata per formare Succinil-CoA. L'anidride
carbonica viene liberata dal sistema.
5) Fosforilazione a livello del
substrato del Succinil-CoA.
Tipo di reazione: Fosforilazione a livello del substrato.
Reagente: Succinil-CoA, Fosfato inorganico, GDP
Prodotto: Succinato, CoA
Enzima coinvolto: Succinil-CoA sintetasi
La quinta reazione avviene al livello del substrato. L'enzima SuccinilCoA sintetasi toglie dal Succinil-CoA il CoA e coadiuva la formazione
di un gruppo carbossilico. Il Coenzima A viene reso disponibile e la
molecola di GTP è immediatamente disponibile per la sintesi di ATP a
partire da ADP.
Meccanismo di sintesi del succinato:
L'enzima Succinil-CoA sintetasi nel
residuo di Istidina è capace di
catturare il fosfato inorganico e
veicolarslo verso il CoA legato al
Succinile. A questo punto avviene
una prima sostituzione e si forma
un intermedio fosfosuccinico ad
alta energia. L'enzima stesso
catalizza il trasferimento del
gruppo fosforico dal succinilfosfato
al GDP formando GTP. Dopo
questa reazione l'enzima è libero e viene rilasciato, proprio come viene rilasciato il GTP appena formato assieme al succinato.
6) Deidrogenazione del Succinato.
Tipo di reazione: Deidrogenazione reversibile
Reagente: Succinato, FAD
Prodotto: Fumarato, FADH2
Enzima coinvolto: Succinato deidrogenasi
Nella sesta reazione il succinato viene ossidato a fumarato. Interviene l'enzima
succinato deidrogenasi che strappa dal succinato due protoni trasferendoli al FAD
che diventa FADH2. Il fumarato viene, dunque, sintetizzato.
La reazione è modestamente esoergonica per cui è reversibile.
7) Idratazione del fumarato.
Tipo di reazione: Idratazione, reversibile
Reagente: Fumarato, acqua
Prodotto: L-Malato
Enzima coinvolto: Fumarato idratasi
La settima reazione vede la sintesi dell' L-Malato a partire dal fumarato. L'enzima fumarato idratasi
addizione al doppio legame acqua per formare la molecola di L-Malato.
La reazione è modestamente esoergonica per cui è reversibile.
8) Deidrogenazione del L-Malato.
Tipo di reazione: Deidrogenazione, reversibile
Reagente: Malato, NAD+
Prodotto: Ossalacetato
Enzima coinvolto: Malato deidrogenasi
L'ottava tappa vede la deidrogenazione del malato per formare
ossalacetato. Gli idrogeni strappati vengono trasferiti, mediante l'aiuto
fornito dall'enzima malato deidrogenasi, al NAD+ che diventa NADH. A
questo punto l'ossalacetato può ripartire dalla tappa numero uno con la
condensazione del Coenzima A.
La reazione è modestamente esoergonica per cui è reversibile
Bilancio energetico globale.
Di per sé il ciclo di Krebs non produce energia liberamente utilizzabile, se non nella reazione tra Succinil-Coa e
Succinato dove si assiste alla formazione di GTP facilmente scambiabile in ATP.
Il ciclo, però, fornisce due tipi di cofattori ridotti capaci di trasportare elettroni ad alta energia ovvero il NADH ed
il FADH2 che possono essere agilmente utilizzati nella catena respiratoria.
Tenendo conto che per ogni molecola di NADH e FADH2, possono essere sintetizzate circa 2,5 molecole di ATP
e che una molecola di ATP è facilmente sintetizzabile da GTP nel ciclo di Krebs vengono formate un numero di
molecole sufficienti per sintetizzare ben 11 molecole di ATP.